血液1滴から難病サルコイドーシスを診断
血清エクソソームを用いたバイオマーカー開発
研究成果のポイント
- 原因不明の難病とされるサルコイドーシスの患者血清中の細胞外小胞(エクソソーム)の解析により診断に有用なバイオマーカーを同定。
- 既にサルコイドーシスのバイオマーカーはいくつか存在するが、感度、特異度ともに十分とは言えないため新規のバイオマーカー開発が望まれている。
- 今回同定したバイオマーカーを既存のバイオマーカーと組み合わせる事により診断率の向上が期待される。
概要
大阪大学大学院医学系研究科の大学院生の二見 悠さん(博士課程)と武田吉人准教授(呼吸器・免疫内科学)らの研究グループは、サルコイドーシスにおいて、血中を流れるエクソソームに含まれるタンパク質の網羅的解析により新規バイオマーカーを同定しました。
サルコイドーシスは肺、眼、心臓、皮膚などを中心に全身に非乾酪性肉芽腫が形成される原因不明の難病とされています。原因として細菌感染や環境因子、遺伝、ストレスなどの関与があることは分かっていますが詳細な病態解明には未だ至っておりません。無治療で自然に軽快する症例もありますが、線維化を起こし不可逆となり重篤な臓器障害をきたす予後不良例も存在し、非常に多彩な臨床経過を辿ります。実臨床ではすでに2つの血清バイオマーカーが用いられていますが、診断、予後予測という点においては満足できるものではなく新規バイオマーカーの開発が望まれています。
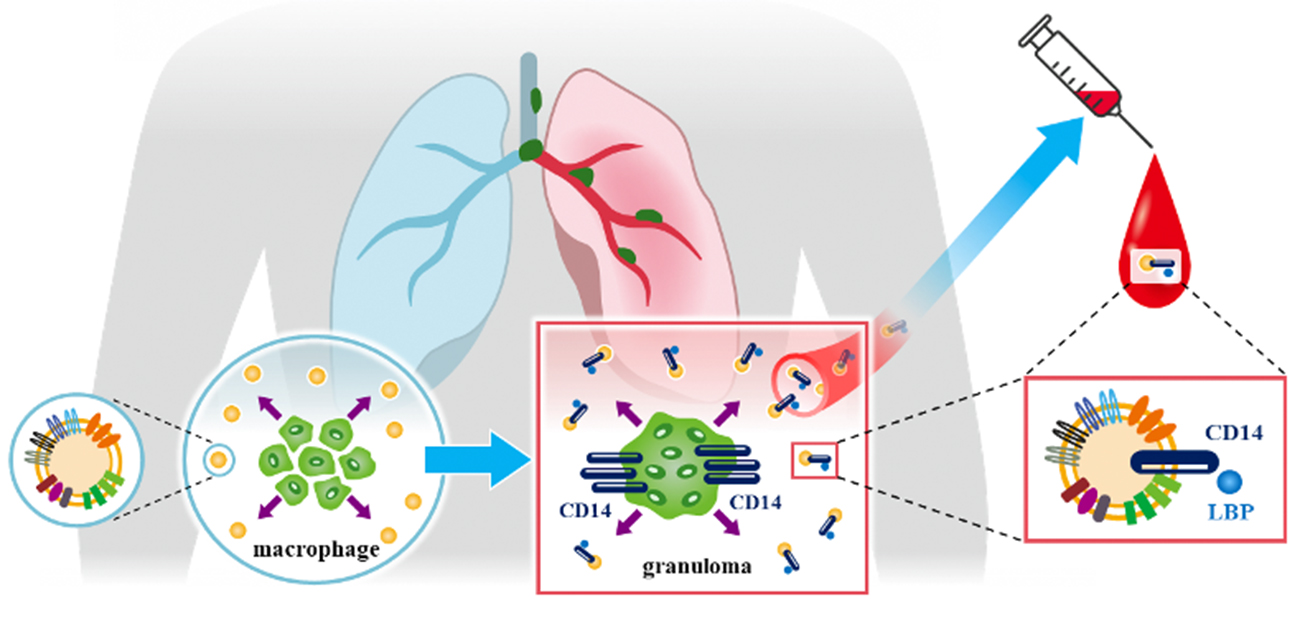
今回、研究グループはサルコイドーシスの新規バイオマーカーを同定するため、血清エクソソームに着目し、サルコイドーシス患者と健常者の血清エクソソームに発現しているタンパク質を網羅的解析により測定、比較し、バイオマーカーとしての精度や病態への関与も含めて検証を重ねました。その結果、CD14、LPS-binding protein (LBP) という2種類のタンパクを新規バイマーカーとして同定しました(図1)。既存のバイオマーカーと組み合わせる事でサルコイドーシスの診断率が向上することが期待されます。またサルコイドーシスの特徴である肉芽腫形成にこれらのタンパク質が深く関わる事が示唆され、病態の解明や新規治療薬開発に繋がる事も期待されます。
本研究成果は、英国科学誌「International Immunology」に、3月16日(水)に公開されました。
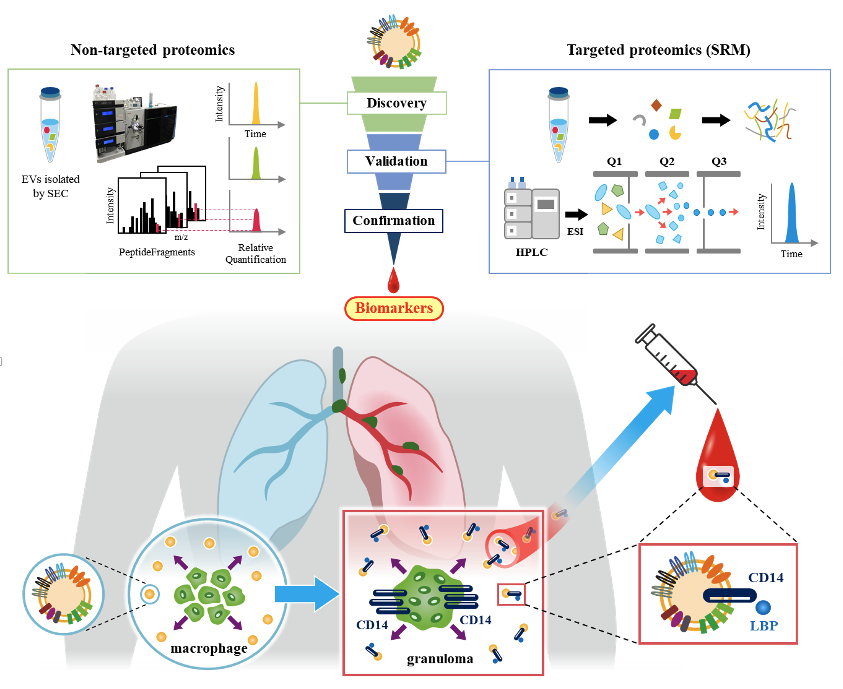
図1. 血清エクソソームからサルコイドーシスの新規バイオマーカーCD14、LBPを同定
研究の背景
サルコイドーシスは肺、眼、心臓、皮膚などを中心に全身に非乾酪性肉芽腫が形成される原因不明の難病とされています。自然に軽快する症例もありますが、線維化を起こし不可逆となり重篤な臓器障害をきたす予後不良例も存在し多彩な臨床経過を辿ります。診断には低侵襲な検査として血液検査で血清バイオマーカー(ACEや可溶性IL2レセプターなど)の上昇を確認する他、臓器病変に対する生検での病理組織診断が必要で、比較的侵襲度の高い検査を要する事もあります。既存の血清バイオマーカーは、病勢はある程度反映していますが、診断や予後予測という点においては満足できるものではなく、組織診断が困難な症例では診断に苦慮します。
また、サルコイドーシスの発症原因についても研究が進められていますが細菌感染などの抗原暴露という単一の環境因子のみでは説明できず、複数の遺伝的要因が関連します。このような多遺伝子の関わる多様な表現型を示す疾患に対して近年ではオミクスを用いた研究が行われています。オミクスの中でもタンパク質を対象としたプロテオミクスはその複雑性からまだ課題の多い分野でもあります。課題の一つに、血液(血清)にはアルブミンをはじめとした夾雑物が大量に含まれるため、病態を反映するようなごく微量の分子を探索するにあたってプロテオミクスは困難とされています。一方、エクソソームは単離の際に夾雑物が除去される事、脂質二重膜で囲まれていてタンパクの情報が保持されている事からプロテオミクスに有利な理想的サンプル(リキッドバイオプシー)と考えられたので、血清エクソソームを対象として難病の新規バイオマーカーの探索を試みました。
研究の内容
研究グループでは、血清からサイズ排除クロマトグラフィーを用いてエクソソームを単離し、そのエクソソームに発現しているタンパクに対する網羅的解析(プロテオミクス)を駆使することでCD14,LBPがサルコイドーシスのバイオマーカーになり得る事を見出しました。
まず、血清エクソソームに対してノンターゲットプロテオミクスで2292種類ものタンパクを同定しました。さらにそれらのタンパクの中でサルコイドーシス患者さんの血清で優位に上昇しているタンパクを42種類見出しました。さらに別のサンプルを対象として、次世代プロテオミクスとされるターゲットプロテオミクスにより、これら候補蛋白の発現量を測定しCD14,LBPという2種類のタンパクをバイオマーカーとして同定しました。
バイオマーカーの精度をROC曲線(Receiver Operating Characteristic curve)で評価すると、従来のACEのAUC (Area Under the Curve)=0.5程度ですが今回見出したバイオマーカーはCD14はAUC=0.81、LBPはAUC=0.84と上回っており、従来のバイオマーカーと組み合わせて使用する事でAUC=0.96まで改善したことから、診断率の向上が期待されます。本研究で登録されたサルコイドーシス患者さんのうち59.6%の方はACEが正常範囲でしたが、新規のバイオマーカーを用いる事でそのうち約45%の患者さんを新たに診断できると考えられました。
これらのタンパクはサルコイドーシス患者さんの血清エクソソーム中だけでなく、生検で得られた病理組織の肉芽腫、多核巨細胞にも発現が亢進している事が確認されました。さらに、マクロファージの細胞株から多核巨細胞を誘導するin vitroの肉芽腫形成モデル実験において、LPSによる肉芽腫誘導刺激が、マクロファージだけでなく、細胞上清中のエクソソームでもこれらのタンパクの発現亢進が確認されました。
以上のことから血清エクソソーム中のCD14やLBPが、肉芽腫、多核巨細胞形成というサルコイドーシスの病態を反映しているため、従来のバイオマーカーに優る可能性が示唆されました。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、サルコイドーシスの診断率の向上、さらには治療介入の一助になる事が期待されます。また他の難病においても同様の手法を用いて新規のバイオマーカー開発、さらには新規薬物開発、個別化医療へ繋がる可能性があリます。
特記事項
本研究成果は、2022年3月16日に米国科学誌「International Immunology」(オンライン)に掲載されました。
タイトル:“CD14 and lipopolysaccharide-binding protein as novel biomarkers for sarcoidosis by proteomics of serum extracellular vesicles”
著者名:1Yu Futami, 1Yoshito Takeda*,1Taro Koba, 2Ryohei Narumi, 3Yosui Nojima, 3Mari Ito, 1Mana Nakayama, 2Mimiko Ishida, 1Hanako Yoshimura, 1Yujiro Naito, 1Kiyoharu Fukushima, 4Takayuki Takimoto, 1Takanori Matsuki, 1Ryuya Edahiro, 1Yoshitomo Hayama, 1Kiyoharu Fukushima, 1Ryuya Edahiro, 1Tomonori Matsuki, 5Satoshi Nojima, 1Haruhiko Hirata, 1Shohei Koyama, 1Kota Iwahori, 1Izumi Nagatomo, 1Yuya Shirai, 1Yasuhiko Suga, 1Shingo Satoh, 1Shinji Futami, 1Kotaro Miyake, 1Takayuki Shiroyama, 4Yoshikazu Inoue, 2Jun Adachi, 2Takeshi Tomonaga, 6Koji Ueda, 3Kenji Mizuguchi, and 1Atsushi Kumanogoh (*責任著者)
所属:
1. 大阪大学大学院医学系研究科 呼吸器・免疫内科学
2. 国立研究開発法人 医薬基盤・健康・栄養研究所 プロテオームリサーチプロジェクト
3. 国立研究開発法人 医薬基盤・健康・栄養研究所 バイオインフォマティクスプロジェクト
4. 国立病院機構 近畿中央呼吸器センター 呼吸器内科
5. 大阪大学大学院医学系研究科 病態病理学講座
6. 公益財団法人がん研究所 がんプレシジョン医療研究センター
DOI:https://doi.org/10.1093/intimm/dxac009
参考URL
用語説明
- サルコイドーシス
サルコイドーシスは肺、眼、心臓、皮膚などを中心に全身に非乾酪性肉芽腫が形成される原因不明の難病です。発病時の臨床症状は多彩で肺門縦隔リンパ節、肺、眼、皮膚の罹患頻度が高いとされています。神経、筋、心臓、腎臓、骨、消化器など全身のほとんどの臓器で罹患し、経過中にも他の臓器にも出現し得ます。病理学的特徴は乾酪壊死を伴わない類上皮細胞肉芽腫が認められることですが、確定診断のためには肉芽腫を形成する他疾患を除外する必要があり困難なケースもあります。その後の臨床経過はきわめて多様で、ごく短い期間で自然改善するものから治療の有無によらず慢性に持続するもの、ときには著しい QOLの低下をきたして難治化するものまであります。以前は検診で発見される無症状のものが多く自然改善例も多かったが、近年は自覚症状で発見されるものが増加し経過も長引く例が増えています。治療の基本は副腎皮質ステロイドホルモン薬と免疫抑制薬で、肺、心臓、眼、神経、腎臓など生命予後・機能予後を左右する臓器・組織では十分な治療と管理が必要となります。 女性に多い傾向があり発病年齢は女性では20代と50代以降にピークがある2峰性を示し、男性では20代のみにピークがある1峰性とされていましたが、最近は男女で若年発症が減少し高齢者発症の増加がみられています。上記を踏まえ厚生労働省において指定難病と定められており重症度Ⅲ, Ⅳのものは医療費助成の対象となっています。(2020年 サルコイドーシス診療の手引き)
- エクソソーム
エクソソーム(Exosome)はあらゆる細胞から分泌される直径50-150 nmの細胞外小胞です。その表面は脂質二重膜で囲まれていて、内部には核酸、タンパク質、脂質などを含んでいます。細胞から分泌されたエクソソームは種々の体液(血液、尿など)に存在し、細胞間・組織間の情報伝達に関わるという事がわかっています。癌領域では早期診断だけでなく、治療や薬剤輸送法として臨床応用が検討されており、癌以外の領域においても理想的なリキッドバイオプシーの一つとして期待されています。 (当科HP参照、エクソソームによる呼吸器疾患の新規BM探索|大阪大学大学院医学系研究科 呼吸器・免疫内科学 (osaka-u.ac.jp)
- 非乾酪性肉芽腫
肉芽腫とはマクロファージ系の細胞を中心として炎症細胞が集積して形成される境界明瞭な慢性炎症病巣を意味します。生体内で長期間存在する外来性異物に対する反応として生じます。結核菌に反応して生じる中心部に壊死を伴う肉芽腫を乾酪性肉芽腫と呼びますが、これとは対照的に壊死を伴わない肉芽腫を非乾酪性肉芽腫と呼びサルコイドーシスの特徴の一つとされています。
- CD14、LPS binding protein(LBP)
ヒトの免疫機能は主に自然免疫と獲得免疫に分類されます。リンパ球の働きによる獲得免疫は抗原特異的な抗体を作ることで、病原体を特異的に認識し排除します。他方、自然免疫を担うマクロファージにおいてはToll様受容体(TLR)が病原体を特異的に認識し、排除します。
CD14はマクロファージなどに発現する分子で、グラム陰性細菌の細胞壁成lipopolysaccharide(LPS)を認識してTLR4/MD2複合体にシグナルを誘導し、炎症性サイトカインや一酸化窒素などの炎症性生理活性物質の産生を誘導します。さらにLPSは血清中のLPS binding protein (LBP)と複合体を形成し、この複合体がマクロファージの細胞表面のCD14と結合した後、LPSはTLR4と結合しシグナルが細胞質内に伝えられます。その結果インターロイキン6やインターフェロン-βを誘導する事が分かっています。いずれもサルコイドーシスとの関連が報告されているものであり、今回CD14、LBPがバイオマーカーとして同定された事はエクソソームが病態を反映しているという事を示唆する結果だと言えます。
- ROC曲線(Receiver Operating Characteristic curve)
スクリーニング検査等の精度の評価や従来の検査と新しい検査の比較に用いられる2次元曲線です。異常と正常を区別するカットオフ値を設定し、これを連続的に変化させた際の真陽性率(感度)と偽陽性率(1―特異度)の関連を表す曲線の事を意味します。
- Area Under the Curve (AUC)
ROC曲線を作成した際のグラフの曲線より下の部分の面積を指します。AUCは0から1までの値をとり、値が1に近いほど判別能が高いことを示しバイオマーカーとしての精度が高い事を示します。
