パーキンソン病の原因タンパク質凝集体を脳脊髄液から検出
脳脊髄液検査による臨床診断、治療開発への応用に期待
研究成果のポイント
・超音波を用いた全自動装置により、パーキンソン病の患者の脳脊髄液中から、原因タンパク質であるα-シヌクレイン凝集体の検出を実現した。
・脳脊髄液中のα-シヌクレイン凝集体の程度が実臨床で用いられている指標と相関することを示し、これは既存の知見と併せて、脳内のα-シヌクレイン凝集体蓄積量を推定する指標となり得ることを示した。
・パーキンソン病の臨床診断や重症度評価ならびに治療開発への活用が期待される。
概要
大阪大学大学院医学系研究科の角田渓太医員、池中建介助教(望月秀樹教授 神経内科学)らの研究グループは、大阪大学蛋白質研究所の後藤祐児教授らとの共同研究で、超音波を用いた全自動蛋白質凝集検出装置を用いてパーキンソン病 患者の脳脊髄液中から原因タンパク質α-シヌクレイン 凝集体の検出に成功しました。
これまで、脳内のα-シヌクレイン凝集体の蓄積の程度を知る検査方法はなく、パーキンソン病の治療開発の妨げとなっていました。
今回、池中助教らの研究グループは、超音波を用いた全自動蛋白質凝集検出装置を用いて、パーキンソン病患者の脳脊髄液中のα-シヌクレイン凝集体の検出を実現しました。さらにパーキンソン病患者の脳脊髄液中のα-シヌクレイン凝集体の程度と、実臨床で用いられている指標(MIBG心筋シンチグラフィ の取り込み低下)の相関を示しました。この実臨床で用いられている指標と脳内のα-シヌクレイン凝集体蓄積量は相関することが知られていることから、本手法を用いて検出した脳脊髄液中のα-シヌクレイン凝集体の程度は、脳内の凝集体蓄積量を反映する指標となり得ることを示しました。今後、パーキンソン病の診断・重症度評価・治療開発への応用が期待されます。
本研究成果は、英国科学誌「Scientific Reports」に、4月12日(金)午後6時(日本時間)に公開されました。
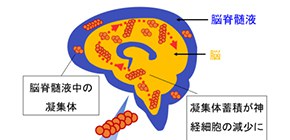
図1 パーキンソン病患者の脳内のα-シヌクレイン凝集体の蓄積。
青色箇所は脳脊髄液、オレンジ色箇所は脳を示している。α-シヌクレインタンパク質が凝集し脳内(オレンジ色)に蓄積すると、神経細胞の減少に繋がる。
研究の背景
これまで、神経難病の一つであるパーキンソン病の原因としてα-シヌクレインというタンパク質の凝集体が脳内に蓄積することが注目されてきました (図1) 。重症な患者さんほどα-シヌクレイン凝集体が多く蓄積していることが亡くなられた後の病理解剖から分かっていますが、生前にその程度を検査する方法はこれまでにありませんでした。またパーキンソン病の発症時点では蓄積がかなり進んだ段階にあることも知られています。
現在、この凝集体の蓄積を抑えることが根本的な治療に繋がるのではないかと期待され、世界中で治療開発が進められています。しかし脳内の凝集体の蓄積量を知る術がないため、治療開発にあたって、より治療の効果が期待できる発症早期の患者さんを正確に選出できない、治療の効果を直接判定できない等の課題がありました。
本研究の成果
研究グループでは、後藤教授らと共同開発したHANABI(HANdai Amyloid Burst Inducer) を用いて、脳脊髄液中のα-シヌクレイン凝集体の検出に成功しました。
HANABIは、凝集体を増幅するための超音波照射装置と凝集体測定器を組み合わせた機械で、リアルタイムに多数の試料で凝集体が増幅されていく過程を観察することができます。一度にたくさんの患者さんの脳脊髄液を測定することができ、凝集体が増幅される速さ(凝集活性)から個々の患者さんの脳脊髄液中に存在する凝集体量を推定することができます。
池中助教らはまず、人工的に作成した凝集体や細胞モデルから放出された凝集体をHANABIで極めて短時間で検出できることを示しました。さらに、パーキンソン病の患者さんの脳脊髄液の凝集活性が、実臨床で用いられている指標であるMIBG心筋シンチグラフィの取り込み低下の程度と相関することを示しました。MIBG心筋シンチグラフィの取り込み低下はパーキンソン病の診断を支持する重要な所見であり、重症な患者さんほど低下していて、心臓の末梢神経での凝集体蓄積を反映する指標と考えられています。これらの結果からHANABIによる脳脊髄液のα-シヌクレイン凝集活性が、脳内の凝集体蓄積を反映する指標となり得ることを示しました。
図2 パーキンソン病が重度である(MIBG心筋シンチの取り込みが低い)患者の脳脊髄液ほど凝集活性が高い
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、脳脊髄液検査によるパーキンソン病の臨床診断、重症度評価への応用が期待されます。また今後、発症早期あるいは発症リスクが高い患者さんの検査を行うことやα-シヌクレイン凝集抑制治療の効果判定を、動物モデルを用いて行うことで、パーキンソン病の根本治療開発に活用できると期待されます。
特記事項
本研究成果は、2019年4月12日(金)午後6時(日本時間)に英国科学誌「Scientific Reports」(オンライン)に掲載されました。
【タイトル】“Ultrasonication-based rapid amplification of α-synuclein aggregates in cerebrospinal fluid”
【著者名】Keita Kakuda , Kensuke Ikenaka 1 , Katsuya Araki 1 , Masatomo So 2 , César Aguirre 2 , Yuta Kajiyama 1 , Kuni Konaka 1 , Kentaro Noi 3 , Kousuke Baba 1 , Hiroshi Tsuda 1 , Seiichi Nagano 1 , Takuma Ohmichi 4 , Yoshitaka Nagai 5 , Takahiko Tokuda 6 , Omar M.A. El-Agnaf 7 , Hirotsugu Ogi 3 , Yuji Goto 2 , Hideki Mochizuki 1* (*責任著者)
【所属】
1.大阪大学 大学院医学系研究科 神経内科学
2.大阪大学 蛋白質研究所
3.大阪大学 大学院工学研究科 精密科学・応用物理学専攻
4.京都府立医科大学 大学院医学研究科 神経内科学
5.大阪大学 大学院医学系研究科 神経難病認知症探索治療学
6.京都府立医科大学 大学院医学研究科 分子脳病態解析学
7.カタール ハマド・ビン・ハリーファ大学, Life Sciences Division, College of Science and Engineering
なお、本研究は、日本医療研究開発機構(AMED)医療分野研究成果展開事業先端計測分析技術・機器開発プログラムの一環として行われ、大阪大学蛋白質研究所後藤祐児教授の協力を得て行われました。
研究者のコメント 角田渓太医員
本研究は当院を受診された多くの患者様のご協力により実施することができました。ご協力頂いた患者様ならびに御関係者の皆様に心より御礼申し上げます。当教室では他にもパーキンソン病の治療開発のための基礎研究や治験を実施させて頂いております。本研究の成果が一日でも早くパーキンソン病の根本治療の実現に繋がるよう今後も尽力いたします。
参考URL
大阪大学 大学院医学系研究科 神経内科学
http://www.med.osaka-u.ac.jp/pub/neurol/myweb6/Top.html
用語説明
- パーキンソン病
手の震え、動きの遅さ、身体のこわばり、転びやすさなどの症状が見られる神経難病。日本では10万人あたり100~150人が罹患している。症状を和らげる治療薬は数多くあるが、病気の進行を食い止める根本的な治療方法は未だに得られていない。
- α-シヌクレイン
パーキンソン病の原因として注目されている脳内のタンパク質。病理検討では異常構造をとったこのタンパク質の凝集体がパーキンソン病に特徴的なレビー小体として確認される。重症な患者ほどこの凝集体の蓄積量が多い。また、この凝集体が脳内の正常なα-シヌクレインを変性させて次の凝集体が形成され、次第に脳内を広がっていく仕組みが注目されている。
- MIBG心筋シンチグラフィ
心筋交感神経への核種の取り込みの程度を測定し、同神経の脱落の程度を評価する臨床検査。パーキンソン病患者ではこの取り込みが低下していることが診断に有用であり、また重症な患者ほど低下している。脱落する心筋交感神経にはα-シヌクレイン凝集体が見られるため、末梢神経でのα-シヌクレイン凝集体の程度を反映すると考えられる。
- HANABI
HANdai Amyloid Burst Inducer:
蛍光測定プレートリーダーと超音波照射装置を組み合わせた全自動蛋白質凝集検出装置。超音波照射によるタンパク質凝集の促進は従来法よりも格段に迅速であり、リアルタイムに多検体の測定が可能である。
