ヒトiPS細胞から高機能な腸管オルガノイドを作製!
薬物の動態評価に応用し、簡便・迅速な医薬品開発へ
研究成果のポイント
- ヒトiPS細胞から1年以上継代培養できる腸管オルガノイド(ヒトiPS細胞由来腸管オルガノイド)を開発。
- オルガノイドとは、試験管内で臓器・器官を模して形成される3次元培養体。今回はヒトiPS細胞から分化誘導して作製した腸管オルガノイドを単層膜化した。
- 作製した単層膜はヒト腸管に近い高い機能を有していた。
- 腸管上皮の薬物動態を正確に予測可能とし、医薬品の効率的な開発を加速すると期待。
概要
大阪大学大学院薬学研究科の水口裕之教授(国立研究開発法人医薬基盤・健康・栄養研究所 招へいプロジェクトリーダー併任)らの研究グループは、ヒトiPS細胞から1年以上培養できる腸管オルガノイドを作製しました。また、それを経口投与医薬品の腸管におけるin vitro薬物動態評価系として応用し、その有用性を示すことに成功しました。
経口投与医薬品は最初に腸管において吸収・代謝・排泄を受けます。こうした一連の反応は医薬品の体内動態に大きな影響を及ぼすため、創薬研究の前臨床段階において、医薬品候補化合物の腸管での動態を試験管内で評価することが重要です。これまで、そうした予測にはがん細胞株や実験動物等が用いられてきましたが、機能不足や種差が原因で正確な予測が困難であるとされてきました。そこでヒトiPS細胞から腸管上皮細胞を作製する研究が進んでいますが、約1ケ月間の長期にわたる分化誘導が必要で実用化に向けて製造面での課題があるだけでなく、機能面でも課題があるのが実情でした。
今回水口教授らの研究グループは、ヒトiPS細胞から腸管オルガノイド(ヒトiPS細胞由来腸管オルガノイド)を作製し、本オルガノイドを単層膜化するプロトコールを確立し、薬物動態評価系に応用しました。その結果、腸管評価系としての高い機能や生体類似性に加え、培養系としての優れた安定性と汎用性を実証しました。この結果は、ヒトiPS細胞由来腸管オルガノイドが、従来系より高機能な腸管上皮細胞を迅速かつ大量に安定して供給可能であることを示しており、医薬品の安全で効率的な開発のみならず、in vitro腸管モデルが必要な様々な分野の研究を加速することが期待されます。
本研究成果は、科学誌「Stem Cell Research & Therapy」に、2月29日(木)に公開されました。
図1. 本研究の概要
研究の背景と内容
錠剤やカプセル剤として投与される経口医薬品は、腸管(小腸)で吸収されると同時に代謝・排泄されます。そのため、腸管における薬物動態を評価することは、創薬研究において重要な検討項目です。現在、そのような評価には、入手や培養が困難なヒト生体由来小腸上皮細胞に代わって、Caco-2細胞などのがん細胞株や、マウス、ラットなどの実験動物を用いられています。しかし、がん細胞株では薬物代謝能が低いこと、実験動物ではヒトとの種差があること等が原因で、医薬品候補化合物の正確な動態を評価・予測することは困難とされてきました。
近年、ヒトiPS細胞から分化誘導される腸管上皮細胞が疾患基礎研究や生理学的研究において広く応用されており、薬物動態評価系としての応用も進んでいます。しかしながら、作製まで長期間を要する上、作製された細胞は継代培養できないため、迅速かつ大量に同細胞を供給することが困難で製造面での課題がありました。
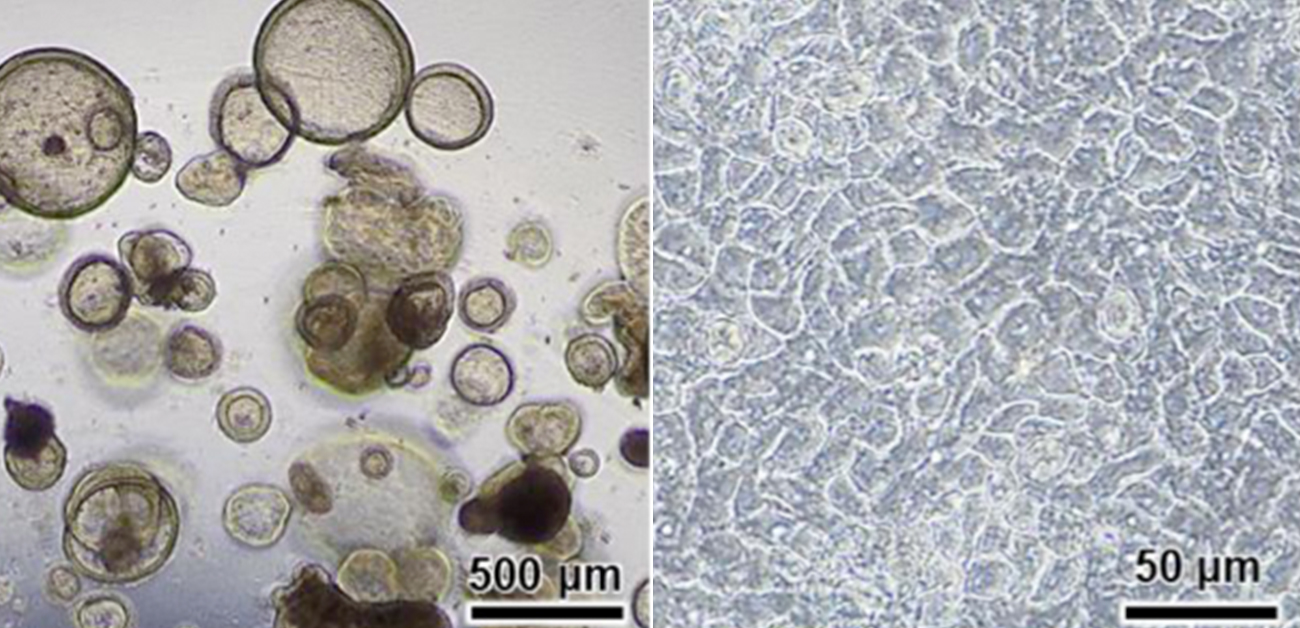
今回、水口教授らの研究グループはヒトiPS細胞から長期培養可能なヒト腸管オルガノイド(図2A)を作製し、それを単層膜化することで(図2B, オルガノイド単層膜)、in vitro腸管評価系としての安定性と汎用性を高めた上で、その機能等を評価しました。その結果、オルガノイド単層膜は微絨毛構造(図2C白矢印)やタイトジャンクション構造(図2C黒矢印)といった、生体の腸管にも見られる形態学的な特徴が観察されました。また、腸管に発現する主要な薬物代謝酵素であるCYP3A4は単層膜中で広域的に発現しており(図2D緑)、CYP3A4や排出トランスポーターのMDR1、腸管上皮細胞マーカーのVIL1の遺伝子発現レベルは成人小腸と同程度であり(図2E)、各種薬物代謝酵素分子種の活性は成人小腸(ヒト初代培養腸管上皮細胞)に近い傾向を示していることが分かりました(図2F)。また、ヒト腸管オルガノイド(図2A)は1年以上増幅させながら継代培養が可能であり、1年以上培養を続けたヒト腸管オルガノイドを単層膜化しても、腸管機能には変化がなく、高い機能をもった腸管細胞の供給が可能でした。こうした結果により、本培養系は従来系と比較してヒト生体に近い機能を有していることに加え、培養系としての安定性と汎用性を兼ね備えていると考えられます。以上のことから、今後、ヒトiPS細胞由来腸管上皮細胞を使用した医薬品の吸収・代謝・排泄試験が加速していくことが期待されます。
図2. 本研究で得られた結果
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、医薬品候補化合物のヒト腸管における吸収・代謝・排泄を試験管内の実験によって正確かつ簡便・迅速に予測できるようになり、臨床試験等の成功率が高まる可能性があります。これにより、医薬品の研究・開発にかかる金銭的・時間的コストが抑えられ、効率的な新薬創出に繋がると考えられます。また、今回開発されたヒト腸管オルガノイド単層膜に関連する技術は、各種の実験基盤として腸内細菌との相互作用や炎症性腸疾患の再現などに加え、再生医療分野への応用も期待されます。さらに、マウス、ラットなどの実験動物を用いた試験の代替法となるため、動物実験の「4Rの原則」を強力に推進できると期待します。
特記事項
本研究成果は、2024年2月29日(木)に科学誌「Stem Cell Research & Therapy」(オンライン)に掲載されました。
タイトル:“Functional intestinal monolayers from organoids derived from human iPS cells for drug discovery research”
著者名:Tatsuya Inui, Yusei Uraya, Jumpei Yokota, Tomoki Yamashita, Kanae Kawai, Kentaro Okada, Yukiko Ueyama-Toba, Hiroyuki Mizuguchi
https://link.springer.com/content/pdf/10.1186/s13287-024-03685-5.pdf
なお、本研究は、独立行政法人日本学術振興会 科学研究費助成事業(学術研究助成基金助成金)挑戦的研究(開拓)(課題番号21K18247, 20K20381, 19J21382)、国立研究開発法人日本医療研究開発機構 創薬等先端技術支援基盤プラットフォーム事業(BINDS)(課題番号JP23ama121054, JP23ama121052)、同機構 医薬品等規制調和・評価研究事業(課題番号23mk0121258h0001)、同機構 次世代治療・診断実現のための創薬基盤技術開発事業(課題番号23ae0121042h0003)、厚生労働省科学研究費補助金(課題番号22KA3005)、公益財団法人 内藤記念科学振興財団研究助成金の一環として行われました。
参考URL
用語説明
- ヒトiPS細胞由来腸管オルガノイド
ヒトiPS細胞を腸管上皮細胞に分化誘導しゲル中に包埋・浮遊させ、各種液性因子(サイトカインや増殖因子、低分子化合物など)を加えた培地で培養することにより樹立される3次元培養体。出発材料としてヒト腸管組織を用いるものも知られているが、本報告ではヒトiPS細胞由来の腸管オルガノイドを特に扱っている。
- 薬物動態
投与された薬物がどのように吸収され、分布し、代謝され、排泄されるのかについて、濃度と速度過程等により解析する学問領域。
- in vitro
試験管や培養器の中で培養細胞等を用いて行う実験系。
- Caco-2細胞
ヒト結腸癌由来の細胞株。Caco-2細胞における薬物透過の度合いは、ヒト生体における腸管吸収と相関するとされており、薬物の消化管膜透過性の評価に広く使用されてきた。その一方で、主要な薬物代謝酵素であるCYP3A4の発現がほとんど見られない等の課題が指摘されている。
- 4Rの原則
動物福祉・愛護の観点から適正な動物実験の実施を推進するための原則。Replacement:代替法の利用、Refinement:苦痛の軽減、Reduction:動物数の削減、Responsibility:実験者の責任、から成る。
