iPS細胞から分化誘導した肝細胞を世界で初めて実用化
信頼性の高い「毒性評価系」の構築をみすえて
薬学研究科・教授・水口裕之
今、世界から注目されているiPS細胞は、再生医療だけでなく、「創薬分野」での応用にも期待が高まっている。分子生物学を専門とする水口裕之教授は、創薬プロセスにおける毒性試験で使用される肝臓細胞(以下肝細胞)を、ヒトiPS細胞から分化誘導し、実用化に成功。その業績により第10回産学官連携功労者表彰・厚生労働大臣賞と、第4回ドイツ・イノベーション・アワード「ゴットフリード・ワグネル賞2012」奨励賞を受賞した。

新しい医薬品の開発には、ヒト肝細胞での毒性評価が必須
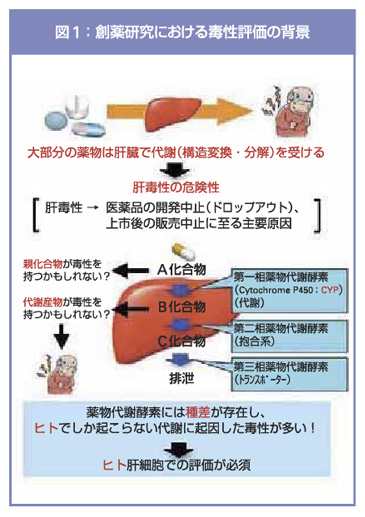
水口裕之教授は、低コストでの医薬品の毒性診断をみすえた「評価系の構築」に取り組んでいる。医薬品の開発には長期にわたる研究と莫大な費用が必要で、製薬メーカーは常に大きなリスクを抱えている。「創薬プロセスの途中で開発が中止になったり、新しい医薬品として市場に出たものの撤退するケースなども多く、その原因として最も多いのは『肝毒性』です。そのため肝臓における毒性をきちんとテストできる、評価系の構築が非常に重要になってきています」と水口教授。
経口であれ注射であれ、ほとんどの薬物は、肝臓に存在する薬物代謝酵素によって代謝(異なる化合物に変換あるいは分解)される(図1)。「その代謝された化合物が毒性を持つ可能性があるのです。また、薬物代謝酵素には種差(ヒトと動物の特性の差)が大きく、ヒトでしか起こらない代謝に起因した毒性を見るためには、ヒト肝細胞での評価が必要となります」
iPS細胞由来のヒト肝細胞で、より正確な毒性評価が可能に
現状では多くの製薬メーカーが、ヒト初代培養肝細胞(生体から直接採取した肝細胞。凍結細胞として輸入することが多い)を使用して毒性検査をしているが、日本では倫理上の問題があり、100%輸入に頼っている。「ヒト初代培養肝細胞は非常に高価で、メーカーによっては年間1億円ほどの購入費を使っていると聞いたことがあります」。またヒトの肝臓の薬物代謝酵素には、その機能に数十倍から千倍以上もの個体差があり、「そのためロット間の品質にばらつきが大きく、再現性のある評価が困難です。また、培養中に薬物代謝酵素の活性が低下するという問題もあります」。
それらを解決できるのが、水口教授が分化誘導し実用化に成功した「ヒトiPS細胞由来の肝細胞」。無限に増殖が可能で大量に安定的に供給できるため、低コストでの活用が期待される。また、規格化により均一な品質を持つロットが調製できれば、毒性評価の再現性も確保できる。「創薬プロセスの早期に、正確な毒性評価ができますから、新薬の開発期間や費用が大幅に縮小できます。また生体内の肝臓に近い状態での毒性評価が可能となり、より安全な医薬品を開発できるようになります」
遺伝子導入技術を利用し肝細胞への高効率分化誘導に成功

これまでヒトiPS細胞から肝細胞への分化誘導法は、「未分化細胞から 内胚葉へ、内胚葉から肝幹前駆細胞へ、 肝幹前駆細胞から成熟肝細胞へ」という分化の3段階で、サイトカインなどの液性因子を付加する方法が一般的だった(図2)。「しかしその方法では分化の効率も、毒性評価のための機能も十分ではありませんでした。そこで私たち(大阪大学、独立行政法人医薬基盤研究所)は液性因子に加え、細胞分化の適切な段階で適切な遺伝子(SOX17、HEX、HNF4α)を、独自開発した改良型アデノウイルスベクター(Adベクター)を利用して導入する分化誘導法を開発しました」。この新技術により、肝細胞への分化効率が飛躍的に向上。またその機能を評価した結果、「ヒト初代培養肝細胞と同等レベルの薬物代謝酵素の遺伝子発現レベルを示し、肝毒性を示す薬剤に対して細胞毒性を示した」という。
そして水口教授の研究グループは、この分化誘導法にさらなる改良を加えるため、肝臓の分化を促進する遺伝子(FOXA2、HNF1α)を探索して導入。この独自技術により分化誘導されたヒト肝細胞が、バイオベンチャー企業との共同開発によって製品化され、今年5月から世界初のヒトiPS由来肝細胞として活用されている。
将来は難病の病態解析や治療薬開発につながる可能性も
このようなiPS細胞の研究を薬学研究科で行っている事例は少なく、「特に肝細胞分野における、創薬への応用を目的としたiPS細胞研究では、私たちが日本で最も進んでいると思います」と水口教授。今後は、「生体内の肝臓の機能にさらに近づけた細胞を作っていきたい。また、より正確な毒性評価を行うには、平均的な人が有する薬物代謝能を示す肝細胞に加えて、個人差の上限と下限の薬物代謝能を示す肝細胞が必要となるので、そのような肝細胞を作りたい。最終的には様々な薬物代謝能を有した肝細胞評価パネルを作り、ヒトで起こる毒性を、より正確にテストできる毒性評価系を構築することが大きな目標です」
また次の段階としてiPS細胞由来の肝細胞を、糖尿病やC型・B型肝炎の病態解明(病気の原因究明)や治療薬開発のためのモデル細胞として使用するなど、新しい切り口での研究もめざしているという。「さらにその先には、医学系研究科とタイアップした再生医療という方向性も考えられますね」
「アデノウイルスベクター 」 の技術が iPS細胞由来肝細胞の実用化を支えた

アデノウイルスベクターは目的遺伝子が染色体に組み込まれず、目的遺伝子を適切なタイミングで、一過性で発現させることができ、遺伝子治療において機動的な運び屋の役割をする。
水口教授は、本来がアデノウイルスベクターの研究者。大阪大学で博士号取得後、ワシントン大学に留学して研究を開始。そして遺伝子導入発現用アデノウイルスベクターを簡単に作成できる技術を世界で初めて開発。その作成キットは世界中で販売され、現在でも様々な分野で活用されている。
その後もウイルス表面タンパク質(ファイバー)の改変などの改良を重ね、高効率の遺伝子導入に成功。この最新の改良型アデノウイルスベクターは、日本と米国で特許を取得している。
(本記事の内容は、2012年12月大阪大学NewsLetterに掲載されたものです)
