ミクロオートファジーによる新たなリソソーム修復機構を発見
リソソームの恒常性を維持し、老化を防ぐ可能性を示唆
研究成果のポイント
- 傷ついたリソソームがミクロオートファジーによって修復されることを発見
- ミクロオートファジー制御因子の欠損により細胞や個体レベルでの老化が亢進(こうしん)、ミクロオートファジーによるリソソーム恒常性維持が老化を防ぐ可能性を示唆
- 健康寿命延長、加齢性疾患の治療への応用に期待
概要
大阪大学大学院生命機能研究科 大学院生の小倉もな美さん(博士後期課程)、医学系研究科/生命機能研究科の吉森保教授、奈良県立医科大学医学部医学科生化学講座の中村修平教授らの研究グループは、傷ついたリソソームの修復を制御する新たな分子メカニズムを明らかにしました(図1)。
生体分子の分解を担う細胞小器官であるリソソームは、さまざまな疾患の病原因子や老化に伴い損傷を受けることが知られ、病態の悪化や老化進行につながると考えられています。傷ついたリソソームは“リソソーム損傷応答”と総称される複数の経路によって修復されることが知られていますが、その詳細な分子機構は明らかにされていませんでした。
今回、研究グループは、リソソーム損傷応答の新たな制御因子の探索を行い、STK38というキナーゼと、GABARAPファミリータンパク質 (GABARAPs) の2つを同定しました。また、リソソームがオートファジーの一形態であるミクロオートファジーによって修復され、STK38とGABARAPsはこの経路の進行に必要であることを見出しました。さらに、これらの因子の欠損はリソソームの損傷増加を伴い、細胞の老化亢進や個体の寿命低下を引き起こしたことから、老化に対して防御的に働くことが示唆されました。これらの成果は、リソソームの恒常性維持に着目した健康寿命延伸や加齢性疾患の新規治療法への応用に役立つことが期待されます。
本研究成果は、国際科学誌「EMBO reports」に、11月21日(火)20時(日本時間)に公開されました。
図1. 研究成果の概略
研究の背景
リソソームは我々の体を構成するすべての細胞の中に存在し、細胞内外から運び込まれたさまざまな生体分子の分解を行う、いわば「細胞内のゴミ処理施設」として働く細胞小器官です。この役割を果たすため、リソソームの中は常に酸性に保たれ、多数の加水分解酵素が含まれています。このため、取り込んだ物質によってリソソームの膜が傷つけられると、酸性の内容物が外へと漏れ出し、炎症や細胞死など細胞にとって非常に有害な影響をもたらします。実際、リソソームの損傷がパーキンソン病のα-シヌクレインをはじめとした加齢性疾患の病原因子や老化に伴って誘導されることが報告されており、病態悪化や老化進行に繋がることが示唆されています。
最近の研究から、細胞はリソソーム損傷応答と総称される複数の経路を駆使し、リソソームの損傷に対処していることがわかってきました。本研究グループでもこれまで、損傷リソソームの除去機構やリソソーム生合成の活性化機構を明らかとし、これらがリソソーム損傷を伴う疾患に対して防御的に働くことを報告してきました (Maejima et al., EMBO J, 2013; Nakamura et al., Nat Cell Biol, 2020)。これらに加え、ESCRT複合体によるリソソーム膜の修復やミクロオートファジーによる膜タンパク質の選択的分解など、リソソームの恒常性維持に関わる多様な応答が報告されています。しかし依然として、リソソーム損傷応答の各経路の実態やそれらがどのように制御されているのか、さらにその生理学的意義についてはほとんどわかっていませんでした。
研究の内容
研究グループはまず、リソソーム損傷応答の新規制御因子を探索すべく、Hippo経路に着目しました。Hippo経路は細胞増殖などを制御する経路であり、オートファジー制御にも関わることが報告されていましたが、リソソーム損傷応答での働きは知られていませんでした。そこで、Hippo経路を構成する因子について、リソソーム損傷の蓄積を指標としたスクリーニングを行い、STK38というキナーゼをリソソーム損傷応答の新規制御因子として同定しました。この因子をノックダウンした細胞ではリソソームの修復を担うESCRT複合体の構成因子VPS4のリソソーム局在が低下しており、STK38がVPS4の局在化を制御していることがわかりました(図2)。さらに、STK38によるVPS4の局在化制御にはキナーゼ活性が重要であり、その下流でDOK1というタンパク質が働いていることも明らかとしました。
実は、ESCRT複合体がどのようにリソソームを修復しているかは、明確にはわかっていませんでしたが、研究グループはこれがミクロオートファジーを介して行われていることを見出し、両者が同一経路であることを新たに示しました。即ち、STK38がVPS4の局在化制御を介してミクロオートファジーによるリソソーム修復を制御していることが明らかとなりました。
ESCRT複合体は複数の構成因子が順次膜上に集積しながら膜を変形させ、最後にVPS4がESCRT複合体の膜からの解離と膜の切り離しを行うことが知られています。研究グループは損傷リソソーム上でのESCRT複合体の局在制御に関するさらなる解析を行い、ESCRT複合体のリソソーム上での集積開始にオートファジー関連因子としてよく知られるATG8が必要であることを見出しました。興味深いことに、ATG8の2つのサブファミリーのうちGABARAPファミリーが主にこの機能を担っており、リソソームの膜に結合したGABARAPsがESCRT複合体と相互作用し、リソソーム上での集積を誘導していることが示唆されました。
そして、STK38やGABARAPsをノックダウンした細胞では細胞老化の亢進とリソソーム損傷の増加を認めました。また老化研究のモデル生物である線虫でも、これら因子の欠損によって老齢期のリソソーム損傷の増加と寿命の短縮が認められました(図3)。
以上から、STK38とGABARAPsが制御するミクロオートファジーによるリソソーム修復がリソソームの恒常性維持によって、老化抑制や寿命延長に寄与している可能性が示唆されました。
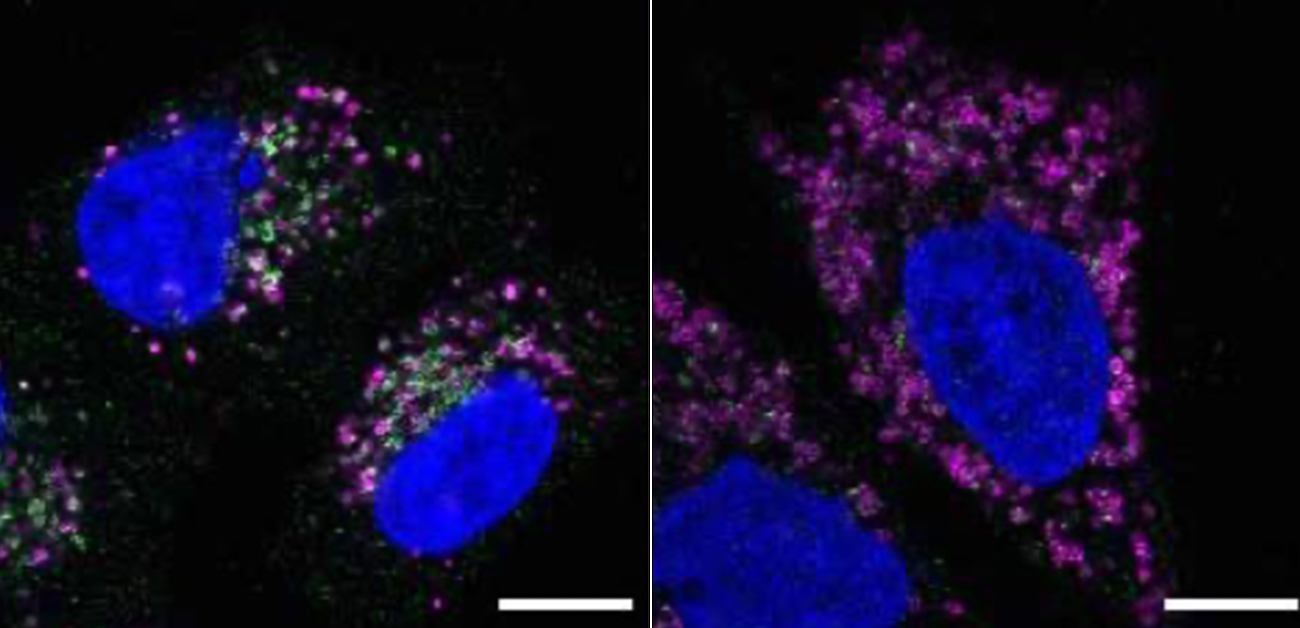
図2. STK38はVPS4のリソソーム局在に必要である
コントロールの細胞ではリソソームが損傷するとVPS4のドット(緑)がリソソーム(赤)上に形成される(左下)。一方、STK38のノックダウン細胞ではVPS4のリソソーム上でのドット形成が低下する(右下)。
図3. STK38の欠損により老化が亢進する
(左)STK38欠損線虫では老齢個体における損傷リソソーム(緑)の蓄積が増加する
(右)STK38欠損線虫(赤)は野生型(黒)よりも寿命が短縮する
本研究成果が社会に与える影響(本研究成果の意義)
本研究では、リソソームの恒常性維持機構を明らかとし、これが老化の進行を防いでいる可能性を示唆することができました。超高齢化社会を迎えた我が国において、「いかに長く健康に生き続けられるか」、すなわち健康寿命の延伸は喫緊の課題とされています。従って本研究で得られた知見が、健康寿命の延伸や加齢性疾患の新たな治療戦略に繋がることが期待されます。
特記事項
本研究成果は、国際科学誌「EMBO reports」に、11月21日(火)20時(日本時間)に公開されました。
タイトル:“Microautophagy regulated by STK38 and GABARAPs is essential to repair lysosomes and prevent aging”
著者名:Monami Ogura1, Tatsuya Kaminishi2, Takayuki Shima2,†, Miku Torigata2, Nao Bekku2, Keisuke Tabata1,2, Satoshi Minami2, Kohei Nishino5, Akiko Nezu2, Maho Hamasaki1,2, Hidetaka Kosako5, Tamotsu Yoshimori1,2,3,* and Shuhei Nakamura1,2,4,*, †(*責任著者)
所属:
1. 大阪大学 大学院生命機能研究科 細胞内膜動態研究室
2. 大阪大学 大学院医学系研究科 遺伝学
3. 大阪大学 先導的学際研究機構(OTRI) 生命医科学融合フロンティア研究部門
4. 大阪大学 高等共創研究院
5. 徳島大学 先端酵素学研究所
† 奈良県立医科大学 医学部医学科 生化学講座(現所属)
DOI:https://doi.org/10.15252/embr.202357300
本研究は、科学技術振興機構(JST)戦略的創造研究推進事業 CREST研究領域「細胞外微粒子に起因する生命現象の解明とその制御に向けた基盤技術の創出」における研究課題「オートファジーによる細胞外微粒子応答と形成」(研究代表者:吉森保)「JPMJCR17H6」、日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)研究開発領域「プロテオスタシスの理解と革新的医療の創出」における研究課題「細胞内膜動態によるプロテオスタシス制御の理解:健康長寿の実現に向けて」(研究代表者:吉森保)「JP22gm1410014」、日本学術振興会基盤研究S「疾患と老化に対抗するオートファジーの分子機構と制御因子の作動原理の解明」(研究代表者:吉森保)「22H04982」文部科学省 学術変革領域研究 B 「TFEB 依存的・非依存的ポストリソソームシグナルによる個体および生殖寿命制御機構」 (研究代表者:中村修平)「21H05145」、日本学術振興会 科研費 挑戦的研究(萌芽)、「「ミクロ」オートファジーによるリソソーム膜修復を介した老化抑制機構の解明」(研究代表者: 中村修平)「23K18140」、日本学術振興会特別研究員奨励費「損傷リソソーム応答の連携を担うTRIM21の作用機構とその生理学的意義の解明」(研究代表者:小倉もな美)「21J21647」の一環として行われました。
参考URL
大阪大学 大学院医学系研究科 遺伝学/生命機能研究科 細胞内膜動態学
http://www.fbs.osaka-u.ac.jp/labs/yoshimori/jp/
奈良県立医科大学 生化学講座
https://bioch.naramed-u.ac.jp/
中村修平教授 research map
https://researchmap.jp/shuhei/?lang=japanese
用語説明
- ミクロオートファジー
細胞内の分解システムであるオートファジーの形態の一つ。リソソームの膜が変形・陥入して分解対象を直接取り込み、分解する。なお、これに対し、オートファゴソームと呼ばれる膜構造体が分解対象を囲い込み、リソソームへ運んで分解する経路はマクロオートファジーと呼ばれる。
- ESCRT複合体
Endosomal sorting complex required for transportの略。いくつかの機能的複合体から構成され、細胞の膜を変形、切り離す役割を持つ。細胞分裂や損傷した膜の修復など、多岐に渡る経路において重要な役割を果たしている。
- キナーゼ
ATPなどに含まれるリン酸基を特定の化合物に転移させる酵素。リン酸化酵素とも呼ばれる。リン酸化はタンパク質の活性制御に大きく関わり、キナーゼは細胞内の多様なシグナル伝達において重要な役割を果たしている。
- ノックダウン
特定の遺伝子の発現量を減少させること。
- 細胞老化
細胞が増殖を停止した状態のこと。細胞は増殖できる回数が限られており、その限界にまで達し、これ以上増殖しなくなった細胞を老化細胞と呼ぶ。異常な細胞増殖を防ぐことでがんを予防する役割があるとされる一方、炎症を起こす物質(サイトカイン)などを分泌し、組織や臓器の機能低下を起こすことが知られ、老化の要因の一つであるとされている。
