細菌間栄養ネットワークを介した歯周病発症メカニズムを解明
代謝物を標的とした新たな歯周病予防法の開発に期待
研究成果のポイント
- 口腔常在菌フソバクテリウムは他の常在菌とのアミノ酸を介した相互作用によりポリアミンを産生することを発見しました。
- ポリアミンは歯周病菌Porphyromonas gingivalisのバイオフィルムの病原性を高めることを示しました。
- 細菌間栄養ネットワークを制御することで新たな歯周病予防法の開発が期待できます。
概要
大阪大学大学院歯学研究科の坂中哲人助教、久保庭雅恵准教授、天野敦雄教授(予防歯科学)、同工学研究科の新間秀一准教授、福﨑英一郎教授(生物資源工学)らは、ルイビル大学(米・ケンタッキー州)との国際共同研究によって、口腔バイオフィルムにおけるフソバクテリウム(Fusobacterium nucleatum)を中心とする細菌間栄養ネットワークを介した歯周病発症メカニズムを明らかにしました(図1)。
歯周病は歯周ポケット内の細菌叢(そう)においてPorphyromonas gingivalisなど数種類の歯周病菌が増加することが引き金となり発症すると考えられていますが、その過程で他の口腔細菌がどのようにP. gingivalisを栄養的にサポートするかについては十分に解明されていませんでした。
今回、本研究グループは、実験的な手法とヒト被験者の歯垢(口腔バイオフィルムの一種)を用いた解析を組み合わせ、F. nucleatumがStreptococcus gordoniiなどの初期定着菌から供与されたアミノ酸を利用してポリアミンを産生し、それがP. gingivalisのバイオフィルムの生活環を加速させることで、歯周病発症に関与することを解明しました。これにより口腔バイオフィルム内でのcross-feedingを介した細菌間栄養ネットワークを制御することで、新たな歯周病予防法の開発が期待できます。
本研究成果は2022年7月19日(現地時刻)に米国科学誌「mSystems」にオンライン掲載されました。
図1. 本研究が明らかにした細菌間栄養ネットワークの概略図
A. 口腔常在菌F. nucleatumは、S. gordoniiによるアルギニン代謝の副産物であるオルニチンを利用してプトレシンを産生し、歯周病菌P. gingivalisのバイオフィルム化を促します。
B. 赤い矢印が本研究により示された知見です。
C. 口腔バイオフィルム内でF. nucleatumが細菌間代謝ネットワークを統合することで、バイオフィルムの歯周病原性が高まると考えられます。
研究の背景
歯周病はP. gingivalisなどの病原菌の増加により引き起こされると考えられていますが、近年の研究で善玉菌を含めた様々な細菌間の相互作用による細菌叢全体のバランスの変化が、病原菌増加の根底にあることが分かってきました。なかでもF. nucleatumは強力な接着因子を有し、様々な口腔細菌に結合することで細菌集団を物理的にまとめる役目を担っていますが、細菌間での栄養素の授受を介した相互扶助については不明な点が多く、とりわけ歯周病発症の過程で栄養学的にP. gingivalisをどのようにサポートするかについては解明されていませんでした。
研究の内容
本研究グループでは過去に、初期定着菌S. gordoniiがアルギニン・オルニチンアンチポーター(ArcD)を利用してオルニチンを排出し、それがcross-feedingによりF. nucleatumのバイオフィルムとしての成長をサポートすることを示しました。今回まず、S. gordoniiとの共培養時のF. nucleatumのメタボローム解析および遺伝子発現解析を行ったところ、F. nucleatumはオルニチンデカルボキシラーゼ(FN0501)という酵素の発現を高め、S. gordoniiから供与されたオルニチンをプトレシンへと代謝することがわかりました。実際に、S. gordoniiのArcD欠損株との共培養時にはF. nucleatumのプトレシン産生能は著しく低下することから、この反応はS. gordoniiのアルギニン代謝とF. nucleatumのオルニチン代謝が掛け合わさることで生じるシナジー代謝であることを示しました(図2)。
図2. F. nucleatumとS. gordoniiのシナジー代謝によるプトレシン産生
アルギニンを含む最小培地を用いて所定の時間培養し、菌体を除去した後の培養上清中の代謝物濃度を測定しました。S. gordoniiのArcDを介したオルニチンのcross-feedingに依存してF. nucleatumはプトレシンを産生することが分かります。
プトレシンを含むポリアミンは、多くの細菌に対して様々な生理反応を引き起こすことが知られています。そこで本研究グループでは、代表的な歯周病菌であるP. gingivalisに対するポリアミンの効果を評価しました。その結果、プトレシンはP. gingivalisのバイオフィルム化を促進するだけでなく、そこからの離脱も促進することで、バイオフィルムとしての生活環を加速させることが示唆されました。実際に3菌種を用いた混合バイオフィルム実験の結果、S. gordoniiとF. nucleatumのシナジー代謝が生じない条件(ArcD欠損株)では、P. gingivalisのバイオフィルム化とそこからの離脱は有意に抑制されることがわかりました(図3)。さらに102名の歯垢サンプルを用いた解析の結果、歯周病重篤度の高い被験者においてS. gordonとF. nucleatumのプトレシン産生遺伝子モジュールとP. gingivalis遺伝子は高い共起関係にあることが確認されました(図4)。このことからF. nucleatumを中心とした栄養ネットワークが歯周病発症に関与する可能性が示されました。
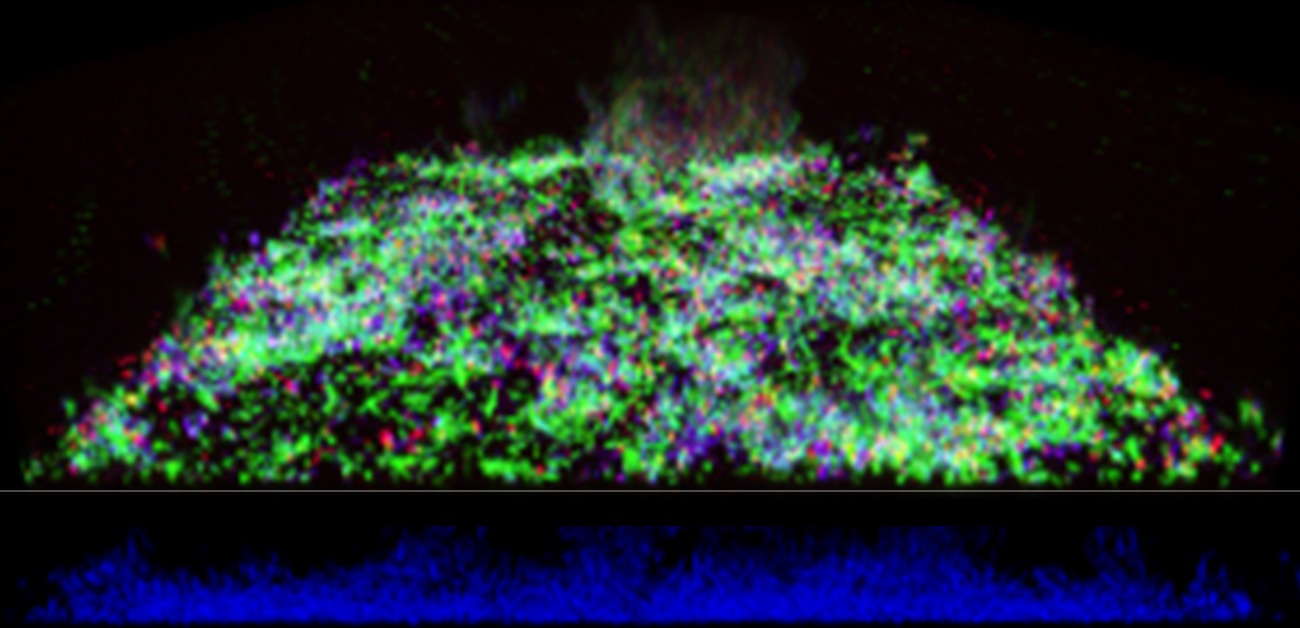
図3. F. nulceatum (緑)-P. gingivalis (青)-S. gordonii (赤)混合バイオフィルム実験
F. nucleatumとS. gordoniiによるシナジー代謝が生じない条件(S. gordoniiのArcD欠損株使用時)では、P. gingivalisのバイオフィルム化とそこからの離脱は有意に抑制されることが分かります。
図4. S. gordoniiとF. nucleatumによるプトレシン産生遺伝子モジュールとP. gingivalis遺伝子の共起関係
A. 歯周病重症度が高い群ほどP. gingivalis陽性者が多く、既報とも一致する妥当な結果です。
B, C. P. gingivalis陽性群ではS. gordoniiとF. nucleatumによるプトレシン産生遺伝子モジュールの存在量に違いがあり、これを指標にするとP. gingivalis陽性群を判別可能であることが分かります。
本研究成果が社会に与える影響(本研究成果の意義)
口腔の常在菌であるF. nucleatumは近年、大腸がん等との関連が指摘され、その多面性に注目が集まっています。今回の研究でF. nucleatumは、善玉菌にとっての排泄物であるアミノ酸を使ってエネルギーを得るとともに、それを使ってポリアミンを産生し歯周病菌を栄養することで、口腔バイオフィルムの成熟と高病原化を促進することを明らかにしました。このことから歯磨きを怠ると、F. nucleatumが栄養的な橋渡し役となり口腔バイオフィルム内の細菌が自発的に代謝物のやりとりを始め、最終的に悪玉菌の増加を招くと考えられます。今後さらに研究が進み、口腔バイオフィルム内での細菌間栄養ネットワークを制御できれば、新たな歯周病予防法の開発が期待できます。
特記事項
本研究成果は2022年7月19日に米国科学誌「mSystems」にオンライン掲載されました。
タイトル:“Fusobacterium nucleatum metabolically integrates commensals and pathogens in oral biofilms”
著者名: Akito Sakanaka1, Masae Kuboniwa1, Shuichi Shimma2, Samar A. Alghamdi1, Shota Mayumi1, Richard J. Lamont3, Eiichiro Fukusaki2, Atsuo Amano1
1. 大阪大学大学院歯学研究科 予防歯科学
2. 大阪大学大学院工学研究科 生物資源工学
3. ルイビル大学歯学部 口腔免疫感染症学
DOI:https://doi.org/10.1128/msystems.00170-22
また、本研究成果は2022年8月1日(現地時刻)に英国科学誌「Nature Reviews Microbiology」のNews & Commentに短報として取り上げられました。
DOI:https://doi.org/10.1038/s41579-022-00787-w
Research Highlightsフリーアクセス記事:https://rdcu.be/cSXXr
本研究は日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)、日本学術振興会科学研究費補助金、NIH/NIDCRの支援を受け、大阪大学大学院歯学研究科、同工学研究科、アメリカ・ルイビル大学の共同研究チームによって実施されました。
また、 American Society for Microbiology (ASM)の2024年highly cited collectionに選出されました。
用語説明
- バイオフィルム
固相表面に形成される雑多な微生物の集合体。広く自然界に存在し、マトリックスと呼ばれる粘着性の物質に覆われることで外部の環境変動に耐えることができる。人体において歯垢は最もよく知られた例の一つであり、う蝕や歯周病の原因となる。
- バイオフィルムの生活環
バイオフィルムを一つの有機体としてみたときのライフサイクルのこと。個々の微生物の固相への付着とクラスターの形成、マトリックス産生と浮遊微生物の合流によるバイオフィルムの形成と成熟、バイオフィルムからの離脱と新たなバイオフィルムの形成というサイクルがある。
- cross-feeding
異なる微生物間での代謝物を介した相互作用のこと。代謝物の流れが一方向か双方向か、あるいは相互作用が互恵的かなどによって分類されるが、一般的に代謝物の受け手の利益となることが多い。多くの微生物間で広くみられる現象であり、微生物叢の栄養共生ネットワークを形成し、疾患傾向にも関与するとされる。
- メタボローム解析
質量分析装置を用いてある生物系における低分子化合物を網羅的に測定する分析技術。
- シナジー代謝
異なる代謝特性を有する複数種の微生物が存在することではじめて発揮される代謝活性のこと。
- 遺伝子モジュール
機能的にまとまった遺伝子のセットのこと。
