
「甘草」なのに「甘くない」のはなぜ?
カンゾウ属植物が作る有効成分グリチルリチンの生産性を決める分子メカニズム
研究成果のポイント
- カンゾウ属植物には、砂糖の150倍以上の甘味を呈するグリチルリチンが含まれており、漢方で最も使用される生薬「甘草」として知られている。ところが、カンゾウ属植物には、種によってグリチルリチンを作らない(すなわち甘くない)ものがあるが、その仕組みは未解明だった。
- 今回の研究で、グリチルリチンを作る/作らないことの理由が、グリチルリチン生成に関わる酵素のわずかな違いによることが明らかになった。
- 生成機構が未解明な、植物有用物質生産への応用が期待される。
概要
大阪大学大学院工学研究科のMuch Zaenal Fanani(ムチャ ザエナル ファナニ) 招へい研究員(研究当時 大学院生(博士後期課程))、澤井学特任研究員、村中俊哉教授(理化学研究所客員主管研究員兼任)と理化学研究所環境資源科学研究センターの斉藤和季センター長(千葉大学植物分子科学研究センター長兼任)らの研究グループは、株式会社常磐植物化学研究所、Universidad Regional Amazónica IKIAMなどと共同で、生薬「甘草」(図1)の基原植物を含むマメ科カンゾウ属植物が作る有用成分グリチルリチンの生産性を左右する分子メカニズムの一端を解明することに成功しました。
今回、研究グループは、グリチルリチン生産性の異なるカンゾウ属植物を材料にグリチルリチン生成に関わる酵素の働きを調べました。その結果、この酵素の働きのわずかな違いが、グリチルリチン生産性を左右することが明らかになりました。また、グリチルリチンの顕著な生産が見られないカンゾウ属植物由来の酵素の活性は生成機構が未解明な天然の有用物質生成に応用できる可能性があり、合成生物学による代替生産法の開発が期待できます。
本研究成果は日本植物生理学会誌「Plant & Cell Physiology」2021年2月号に掲載(2021年5月発行)されました。本論文は同号Editor-in-Chief’s ChoiceならびにResearch Highlightsに選ばれました。

図1. 甘草(Much Z. Fanani博士撮影)
研究の背景
マメ科カンゾウ(Glycyrrhiza)属のカンゾウはその地下部に砂糖の150倍以上とも言われる天然甘味成分グリチルリチンを蓄積することで知られています。また、グリチルリチンには抗炎症作用など薬理活性を有することから、それを蓄積するカンゾウの地下部を乾燥したものは生薬「甘草」として漢方など、洋の東西を問わず古くから薬として用いられています(図1)。カンゾウ属の中でもG. uralensis(ウラルカンゾウ)、G. glabra、G. inflataはグリチルリチンを比較的多く蓄積していることが知られています。一方、カンゾウ属にはG. pallidiflora(イヌカンゾウ)をはじめ甘味成分であるグリチルリチンの顕著な蓄積が見られない種も多く存在します。これまで、同じカンゾウ属でも種によってグリチルリチンの生産性が大きく異なる理由は未解明でした。
本研究グループは2008年にグリチルリチンの生成にはウラルカンゾウが持つシトクロムP450の1種、CYP88D6がグリチルリチンの生成に必須な2度の酸化反応を触媒することを報告しています参考文献。今回、グリチルリチンの顕著な蓄積が見られないイヌカンゾウが持つCYP88D6に相当する酵素(CYP88D15)の働きを調べた結果、2度目の酸化反応を触媒する働きが弱く、グリチルリチン生成に不向きであることがわかりました(図2)。つまり、カンゾウ属植物のCYP88D6、またはそれに相当する酵素のわずかな働きの強さの違いが、グリチルリチン生産性を左右する分子メカニズムの一端であることを解明できました。
【参考文献】
Hikaru Seki, Kiyoshi Ohyama, Satoru Sawai, Masaharu Mizutani, Toshiyuki Ohnishi, Hiroshi Sudo, Tomoyoshi Akashi, Toshio Aoki, Kazuki Saito, and Toshiya Muranaka (2008) Licorice b-amyrin 11-oxidase, a cytochrome P450 with a key role in the biosynthesis of the triterpene sweetener glycyrrhizin. Proc Natl Acad Sci USA 105: 14204-14209.
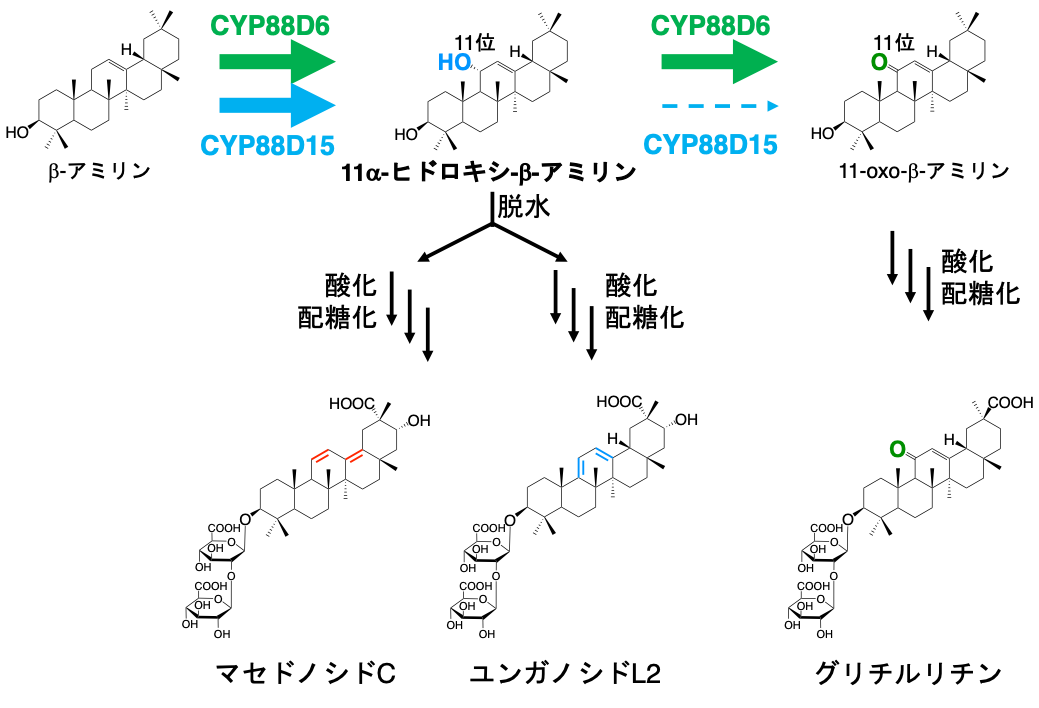
図2. CYP88D6とCYP88D15が触媒する酸化反応
グリチルリチンは生薬「甘草」の有効成分で食品添加物(甘味料)としても使用されている。イヌカンゾウなどグリチルリチンの顕著な蓄積が見られないカンゾウ属植物はしばしばマセドノシドC、ユンガノシドL2などジエン構造を持つサポニンを高蓄積している。マセドノシドCはheteroannular型ジエン構造(赤)、ユンガノシドL2はhomoannular型ジエン構造(青)を有する。
グリチルリチンを比較的高蓄積するカンゾウ属植物由来のCYP88D6はグリチルリチン生成に必須な11位の2段階酸化反応を触媒する(緑矢印)。グリチルリチンの顕著な蓄積が見られないカンゾウ属植物由来のCYP88D15は2段階目の酸化反応活性が弱く(点線青矢印)グリチルリチン生成に不向きであり、中間体である11a-ヒドロキシ-b-アミリンはマセドノシドC、ユンガノシドL2などグリチルリチンを蓄積しないカンゾウ属植物がしばしば高蓄積するサポニンへと代謝されると考えられる。
本研究成果が社会に与える影響(本研究成果の意義)
イヌカンゾウなどグリチルリチンの顕著な蓄積が見られないカンゾウ属植物はしばしばグリチルリチンに代わってマセドノシドC、ユンガノシドL2などheteroannular型ジエン構造またはhomoannular型ジエン構造を持つサポニンを高蓄積することが知られています。今回調べたイヌカンゾウのCYP88D15触媒機能から、CYP88D15はマセドノシドC、ユンガノシドL2などに見られるheteroannular型ジエン構造またはhomoannular型ジエン構造の形成に関与していると考えられます。天然には有用な生物活性を示すジエン構造を持つトリテルペノイドがいくつも存在します。それらのジエン構造の生成機構は未解明です。本研究で明らかとなったCYP88D15触媒活性を用いることで、それら生成機構未解明な有用トリテルペノイドの合成生物学的手法による生産等が期待されます。
特記事項
本研究成果は日本植物生理学会誌「Plant & Cell Physiology」2021年2月号掲載(2021年5月発行)に先立ち、オンライン版(2021年1月13日付け)で公開されました。また、同号Editor-in-Chief’s ChoiceならびにResearch Highlightsに選ばれました。
タイトル:“Allylic Hydroxylation Activity is a Source of Saponin Chemodiversity in the Genus Glycyrrhiza”
著者名:Much Z. Fanani†, Satoru Sawai†, Hikaru Seki, Masato Ishimori, Kiyoshi Ohyama, Ery O. Fukushima, Hiroshi Sudo, Kazuki Saito*, Toshiya Muranaka*
†These authors contributed equally to this work.
*Corresponding authors.
掲載誌情報:Plant & Cell Physiology 62(2):262–271 (2021), doi.org/10.1093/pcp/pcaa173
Research Highlights:https://academic.oup.com/pcp/pages/research_highlights_2021_2
なお、本研究の一部は、農林水産省農林水産業・食品産業科学技術研究推進事業「作物における有用サポニン産生制御技術の開発」(独立行政法人生物系特定産業技術研究支援センターイノベーション創出基礎的研究推進事業「作物における有用サポニン産生制御技術の開発」より移管)、日本学術振興会科学研究費助成事業基盤研究(B)、文部科学省国費外国人留学生制度などの支援を受け、日本大学 青木俊夫教授、明石智義教授、理化学研究所 清水英明研究員、横山茂之領域長、橋之口裕美氏、北海道医療大学 高上馬希重准教授、大阪医科薬科大学 芝野真喜雄教授、東京工業大学 藤本善徳名誉教授、桐田理生氏、テネシー大学David R. Nelson教授、大阪大学 井上匡子助教の協力を得て行われました。
参考URL
村中俊哉教授 研究者総覧URL
https://rd.iai.osaka-u.ac.jp/ja/18096dd925d4ba31.html
SDGs目標

用語説明
- シトクロムP450
ヘムを含むタンパク質の1群。ヒトを含む動物から、植物、微生物に至るまで、幅広い生物が持つタンパク質群。ヘムに一酸化炭素が結合すると450 nm付近に極大吸収を示すことにその名が由来する。主に酸素分子を用いたモノオキシゲナーゼとして機能することが知られている。
- heteroannular型ジエン構造またはhomoannular型ジエン構造
環状化合物において2つの二重結合が1つの環にある構造をhomoannular型ジエンと呼び、2つの二重結合それぞれが異なる環に存在する構造をheteroannular型ジエンと呼ぶ。
- サポニン
トリテルペンを非糖部の基本構造とする配糖体。グリチルリチンもサポニンの1種。
- トリテルペノイド
炭素数5のイソプレン単位6つからなる炭素数30の化合物であるトリテルペンを基本構造とする化合物群。
