心臓の鼓動を制御する分子メカニズムをついに可視化
筋収縮のカルシウム制御機構の全貌が明らかに
研究成果のポイント
・心筋の収縮と弛緩のカルシウム制御のメカニズムを解明するため、ヒト心筋の細いフィラメント の立体構造をクライオ電子顕微鏡法 によって解析し、オン・オフの2状態間の構造変化を解明。
・細いフィラメントを構成する5種類のタンパク質の各立体構造はX線や電子顕微鏡によって明らかにされてきたが、細いフィラメント全体の構造解析は非常に困難であった。今回、クライオ電子顕微鏡画像解析の工夫により全体構造の全貌が明らかになり、さらに、カルシウム存在下(オン;収縮)と非存在下(オフ;弛緩)の2状態間構造変化の可視化に成功。
・肥大型・拡張型心筋症などの突発性心筋症は細いフィラメント構成蛋白質の遺伝子変異が原因であることが知られており、これらの病態の原因解明や創薬への応用に期待。
概要
大阪大学大学院生命機能研究科の山田有里佳特任研究員、難波啓一特任教授、藤井高志特任准教授(常勤)の研究グループは、ヒト心筋の細いフィラメントにおける収縮弛緩の制御メカニズムを分子レベルで明らかにしました。1960年代に江橋節郎博士が、筋肉の収縮装置にカルシウムイオンで駆動する制御スイッチが存在すること、そのスイッチの鍵となるのがアクチンで構成される細いフィラメント上に存在するトロポニンであることを発見しました。それ以来、筋収縮のカルシウム調節機構の詳細なメカニズムを明らかにするために、様々な生化学、生理学研究や構造研究が行われてきました。細いフィラメントの構造研究では、アクチン、トロポミオシン、トロポニンのそれぞれ単体についてX線や電子顕微鏡により構造解析が行われていましたが、細いフィラメント全体の構造はほとんど見えていませんでした。
今回、研究グループは、クライオ電子顕微鏡を用いてカルシウム存在下および非存在下の2状態における細いフィラメントの立体構造変化を明らかにすることにより、筋収縮制御メカニズムの構造基盤を世界に先駆けて明らかにしました。これにより、肥大型・拡張型心筋症の原因解明や創薬などに役立てることが期待されます。
本研究成果は、2020年1月9日(木)19時(日本時間)に米国科学誌「Nature Communications」(オンライン)に掲載されました。
図1 筋肉の構造の模式図(左)と細いフィラメント全体構造(右)
研究の背景
筋肉は多数の筋原繊維の束でできており、筋原繊維はサルコメアと呼ばれる単位構造が直列に連結したものです。サルコメアでは、アクチンからなる”細いフィラメント”とミオシンからなる”太いフィラメント”が重なり合うようにして規則正しく整列しています (図1) 。細いフィラメントは、アクチン繊維とトロポミオシン、トロポニンから構成され、トロポミオシンとトロポニンはアクチン14分子に対して2分子ずつペアで結合しています。筋収縮のエネルギー源はATP であり、ミオシン頭部におけるATP加水分解反応に伴ってアクチンとミオシンの結合と解離が繰り返されることで、両フィラメント間の滑り運動が起こり、サルコメアが短縮して筋収縮が起こります。これを制御しているのが細胞内カルシウムイオン(Ca 2+ )の濃度です。弛緩状態では、筋細胞内のCa 2+ 濃度が低いためアクチン繊維上のトロポニンからCa 2+ が解離していて、トロポミオシンがアクチン分子表面のミオシン結合部位を覆っているため、ミオシン頭部はアクチンと相互作用できませんが、神経から電気信号が届くと筋小胞体からCa 2+ が放出され、筋細胞内のCa 2+ 濃度が高まり、アクチン繊維上のトロポニンにCa 2+ が結合し、トロポミオシンを移動させてアクチン分子表面のミオシン結合部位を露出させます。こうしてミオシン-アクチン相互作用が可能になり、両フィラメント間の滑り運動によるサルコメアの短縮が開始すると考えられてきました。しかし、トロポニンへのCa 2+ 結合がどのようにトロポミオシンを移動させるのか、細いフィラメントの全体構造が明らかでないため長らく謎のままでした。筋収縮と弛緩のCa 2+ スイッチ機構を解明するためには、Ca 2+ 存在下と非存在下の2状態の細いフィラメントの構造を高分解能で解析することが必要でした。この構造を可視化できる唯一の方法は最近急速に進歩したクライオ電子顕微鏡の単粒子像解析法ですが、トロポミオシンはきわめて細長く、トロポニンも小さな分子で、しかもアクチン繊維・トロポミオシン・トロポニン複合体の構造が不安定であるため、細いフィラメントの構造解析は大変困難な課題でした。
このたび研究グループは、クライオ電子顕微鏡と画像解析法の工夫を重ねることにより、ヒト心筋の細いフィラメントの立体構造解析に成功しました。トロポニンC, I, Tの3分子からなるトロポニンが予想外にトロポミオシンと同程度に細長い分子であることや、トロポミオシンと共にアクチン繊維に結合している様子を明らかにしました。さらに、Ca 2+ 存在下と非存在下の2状態における細いフィラメントの構造を解明し、収縮弛緩の制御に関わるトロポニンとトロポミオシンの構造変化を可視化することに成功しました。
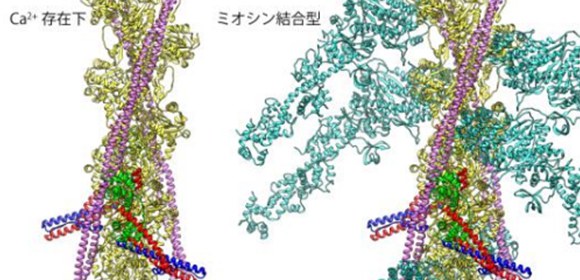
図2 Ca 2+ 非存在下(左)と存在下(右)の細いフィラメントの構造と比較
図3 筋収縮・弛緩の制御メカニズムに関わる細いフィラメントのCa 2+ 結合による構造変化の模式図(左)とミオシン頭部の結合状態(最右)まで含めた分子構造モデル(右)
本研究成果が社会に与える影響(本研究成果の意義)
肥大型・拡張型心筋症などの突発性心筋症は原因がわかっていないものが多く、遺伝的な要因が関与していることが知られています。そして、これらはトロポニンの変異によって筋収縮のCa 2+ 制御機能の異常を引き起こしていると考えられています。本研究成果を基盤として今後の研究が発展すれば、アクチンやトロポミオシン、トロポニンの変異によって引き起こされる心筋症の原因解明や治療法の開発への応用が期待されます。
特記事項
本研究成果は、2020年1月9日(木)19時(日本時間)に米国科学誌「Nature Communications」(オンライン)に掲載されました。
タイトル:“Cardiac muscle thin filament structures reveal calcium regulatory mechanism”
著者名:Yurika Yamada, Keiichi Namba and Takashi Fujii
なお、本研究は、JSTさきがけ(JPMJPR12L6)、JSPS科研費(25000013、18K06155)、AMED/BINDS(JP19am0101117)、AMED/CiCLE(JP17pc0101020)、および日本電子YOKOGUSHI協働研究所の支援の一環として行われました。
研究者のコメント
1960年代の江橋節郎博士によるトロポニンと筋収縮Ca 2+ 制御機構の発見以来、半世紀以上にわたって長らく謎であったその分子構造基盤を、クライオ電子顕微鏡による画像解析法の工夫を重ねてようやく明らかにすることができました。ヒトの心臓が約1秒ごとに収縮弛緩して鼓動する際に、心筋細胞内のタンパク質繊維で起こっている変化が分子レベルで見えたのは大変嬉しいことで、一般の方達にも大変興味深いことではないかと思います。
参考URL
大阪大学大学院生命機能研究科HP
http://www.fbs.osaka-u.ac.jp/index.php
用語説明
- 細いフィラメント
アクチン繊維、トロポミオシン、トロポニン(トロポニンC, I, Tの複合体)の5つの構成因子タンパク質からなる繊維状複合体で、トロポミオシン・トロポニンはアクチン繊維に沿ってアクチン14分子に2分子ずつ結合している。
- クライオ電子顕微鏡
液体窒素や液体ヘリウムで冷却した試料ステージを装備した透過型電子顕微鏡。生体分子や細胞などの生体試料の水溶液を重金属で染色することなく、孔あきカーボン薄膜上に水溶液薄膜を作り液体エタンで急速凍結させて非晶質氷薄膜とし、その中に試料を閉じ込めて低温で観察するので、本来の構造や機能を保持したまま立体構造を観察できる。様々な方向で氷薄膜中に包埋された生体分子の透過像を数多く撮影して画像解析することにより、生体分子の立体構造を解析するのが単粒子像解析法。
- ATP
アデノシン三リン酸。代謝や合成などに使われる生体内の主要なエネルギー源で、筋収縮のエネルギー源でもある。
