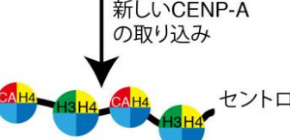
染色体の分配装置が形成される仕組みを解明
染色体異常を伴う疾患の原因解明に期待
研究成果のポイント
・次世代の細胞へ染色体が伝達される際、重要な働きを担う分子装置(セントロメア)の形成メカニズムを発見。
・これまでセントロメアが形成される元となる分子(CENP-A)が知られていたが、本研究では CENP-A が他の因子(KNL2/M18BP1)と協調しながら、どのようにセントロメアへ取り込まれるのか、についてその仕組みを明らかにした。
・染色体の分配異常で起こる各種疾病の原因解明につながる成果として期待。
概要
大阪大学大学院生命機能研究科の深川竜郎教授らの研究グループは、染色体が次世代の細胞へ伝わる際に重要なセントロメア が形成される仕組みを明らかにしました。染色体の伝達には、セントロメアと呼ばれる分子装置が重要であり、その元としてCENP-A と呼ばれる分子が関与することはわかっていました。しかしながら、セントロメアが形成・維持されるためにCENP-Aがどのようにセントロメアへ取り込まれるのか、その仕組みについては不明でした。
今回、研究グループは、KNL2というタンパク質に注目して研究を行い、ニワトリの細胞を使った細胞内条件(in vivo)と試験管内の実験(in vitro)において、KNL2がCENP-Aと染色体上で結合することを明らかにしました。また、細胞が増殖する過程において、染色体に取り込まれていない CENP-A (新しい CENP-A)が KNL2 を含む複合体を認識して、元々CENP-A が存在する領域(古い CENP-A 領域)に新しく取り込まれる仕組みを見出しました (図1) 。
染色体の伝達異常に起因する染色体異常は、がんやダウン症などの各種疾病の原因になることが知られており、染色体の厳密な伝達メカニズムの詳細に迫る今回の研究成果は、各種疾病に見られる染色体異常の原因解明につながる成果と期待されます。
本研究成果は、米国科学誌「Developmental Cell」に、7月25日(火)0時半(日本時間)に公開されました。
図1 新しいCENP-Aがセントロメアに取り込まれる仕組みについての模式図
セントロメアにまだ取り込まれていない新しいCENP-A(図中CA)は、セントロメア上のCENP-A(古いCENPA)にあるKNL2を含む複合体を認識して、新たにセントロメアへ取り込まれる。
研究の背景
生物のすべての遺伝情報(ゲノム)は、染色体と呼ばれる構造体に包まれ、次世代の細胞に伝達されて行きます。染色体の正確な伝達は、生命を維持する上で必須です。染色体の伝達に異常がおきると、染色体構造に異常が生じ本研究成果は論文掲載先である「て、その染色体異常は、がんやダウン症を始め、多くの病気の原因になることが知られています。したがって、染色体が正確に次世代の細胞へ伝達されるメカニズムを解明することは、生命を維持するための基本原理の理解に繋がり、染色体異常が原因で起こる病気の発症機構を解明する上でも重要な研究と言えます。
染色体の伝達は、細胞の両極から伸びた紡錘糸が染色体のセントロメアと呼ばれる特殊領域を捉え、娘細胞と呼ばれる次世代の細胞へ染色体を分けることによって行われます (図2) 。したがって、染色体が正確に娘細胞へ伝達される仕組みを知るためには、セントロメアが形成される仕組みを詳細に理解しなければなりません。
これまでの研究から、セントロメアが形成される元となる分子としてCENP-A分子が知られていました。CENP-Aが取り込まれると、その領域がセントロメアとなりますので、CENP-Aはセントロメアの形成に非常に重要な分子です。しかしながら、CENP-Aがどのようにセントロメアに取り込まれ、セントロメアがどのように維持されるのかについては、わかっていませんでした。
図2 遺伝子が次世代の細胞へ伝わる仕組み
全ゲノム情報は染色体という構造体に含まれる。細胞分裂期に、紡錘糸が染色体上の分裂装置とくっついて、次世代の細胞へゲノム情報を伝達する。紡錘糸の付着する染色体上の分裂装置をセントロメアとよぶ。
本研究の成果
今回、研究グループは、KNL2(M18BP1)というタンパク質に注目しました。これまでの研究からKNL2は複合体を形成してCENP-Aの取り込みに関与することが想定されていましたが、実際にニワトリ細胞内でKNL2を働かないようにすると、新たにCENP-Aがセントロメアに取り込まれなくなることが明らかになりました。次にKNL2の重要であると予測された領域(KNL2がコードする全長、1088アミノ酸残基の内、中央部の19アミノ酸領域)に注目し、その部分を取り除くと、KNL2が機能しなくなることを突き止めました。またKNL2タンパク質とCENP-Aを精製し試験管内で混ぜる実験から、KNL2タンパク質は、上記機能でも重要と確認された特有の19アミノ酸領域を介してCENP-Aと特異的に結合することが証明されました。さらに、KNL2タンパク質を非セントロメア領域に存在させると、染色体上に集まる前の新たなCENP-Aがその領域に集合してくることが明らかになりました。
以上の実験結果より、KNL2を含む複合体は、セントロメアにすでに存在しているCENP-A(古いCENP-A)と結合しており、染色体に取り込まれていないフリーの新しいCENP-Aは、KNL2を含む複合体を認識して新たにセントロメアに取り込まれる仕組みがあることが判明しました (図3) 。すなわち、細胞増殖を経ながら、どうやってCENP-Aが、セントロメア領域に取り込まれていくのかという仕組みを明らかにしました。
図3 新しいCENP-Aがセントロメアに取り込まれる仕組みについての模式図
セントロメアにまだ取り込まれていない新しいCENPA(図中CA)は、ヒストンH4、HJURPとともに、CENPA複合体を作る。今回の論文で注目したKNL2は複合体を形成してセントロメア上のCENP-Aとすでに結合してセントロメアに存在している(古いCENP-A)。新しいCENP-A複合体は、KNL2を含む複合体を認識して、新たにセントロメアへ取り込まれる。このようにして、CENP-Aは次々とセントロメアへ取り込まれ、セントロメアは維持されている。
本研究成果が社会に与える影響(本研究成果の意義)
がんやダウン症を始め、染色体の伝達異常が原因となる疾患は多く知られています。その原因の解明には、染色体の正確な伝達メカニズムを理解することが不可欠です。本研究成果により、染色体の分配異常で起こる各種疾病の原因解明につながる成果と期待されます。将来的には、セントロメア形成に関わる分子を標的とした薬剤開発にもつながると期待されます。
特記事項
本研究成果は、2017年7月24日(月)15時半(UTC)〔7月25日(火)0時半(日本時間)〕に米国科学誌「Developmental Cell」(オンライン)に掲載されました。
タイトル:“Association of M18BP1/KNL2 with CENP-A nucleosome is essential for centromere formation in non-mammalian vertebrates”
著者名:Tetsuya Hori 1 , Wei-Hao Shang 1 , Masatoshi Hara 1 , Mariko Ariyoshi 1 , Yasuhiro Arimura 2 , Risa Fujita 2 , Hitoshi Kurumizaka 1 , and Tatsuo Fukagawa 1* ,
1.大阪大学大学院生命機能研究科
2.早稲田大学先進理工学研究科
(*責任著者)
なお、本研究は、日本学術振興会科学研究費補助金基盤研究(S)及び文科省科学研究費補助金新学術領域研究「染色体OS」の一環として行われた、早稲田大学との共同研究です。
参考URL
大阪大学大学院生命機能研究科 深川研究室
http://www.fbs.osaka-u.ac.jp/labs/fukagawa/index_j.html
用語説明
- セントロメア
細胞分裂の際、紡錘糸が結合する染色体の分子装置を指す。動原体とも呼ばれる。セントロメアが形成されるためには、ある特定の領域に複数のタンパク質が集合しなければならない。どのような分子機構でセントロメアが形成・維持されるのかについては不明な点が多い。セントロメアの機能不全によって、染色体分配が正常に起きなくなり、染色体異常が生じる。染色体異常は、がんやダウン症などの病気の原因となることが知られている。
- CENP-A
セントロメアに存在するタンパク質の一種であり、セントロメア形成の元となる分子であることが知られている。
