室温でスピンの向きを揃えられる分子の種類を 増やす共結晶化技術の開発に成功
量子技術を用いた超高感度MRIによる 精密がん診断や治療効果判定に向けて大きく前進
研究成果のポイント
概要
核スピン(原子核が持つ磁石のような性質)の振る舞いを見るNMR(核磁気共鳴)やMRI(磁気共鳴イメージング)の検出感度は、核スピンの向きの揃い具合(偏極率)に比例します。一般的な偏極率は極めて低く、より高度なNMRやMRI測定、例えば微小な腫瘍のMRI検出などは困難です。極低温で核スピンの向きを揃える動的核偏極(DNP)と呼ばれる方法が盛んに研究されていますが、高価な装置や液体ヘリウムなどの寒剤がネックとなり、広く社会に普及していません。
徳島大学大学院社会産業理工学研究部物理科学分野の犬飼宗弘准教授、大阪大学量子情報・量子生命研究センターの宮西孝一郎講師、根来誠准教授、大阪大学ヒューマン・メタバース疾患研究拠点 香川晃徳特任准教授(常勤)、筑波大学計算科学研究センターの堀優太助教、重田育昭教授、金沢大学理工研究域の栗原拓也助教らからなる研究チームは、光とマイクロ波を照射することで引き起こされる量子力学的過程によって、室温でスピンの向きを揃えられる光励起三重項の電子スピンを用いたDNP(トリプレットDNP)に注目しました。トリプレットDNPは古くから研究されている手法ですが、この技術を応用するためには課題が残されており、適用できる分子の種類が限られていました。
本研究では、トリプレットDNPが適用できる分子の種類を劇的に増やす方法として、共結晶化技術を開発しました。トリプレットDNPにより感度を向上させたいターゲット分子、補助分子、そして感度向上の元となる偏極源から組み上がる共結晶を開発し、MRI分子プローブである尿素を含む複数分子のトリプレットDNPを室温で実現しました。
将来、本研究が提案する共結晶化技術とMRIを組み合わせることで、従来法では困難であった精密ながんの診断や治療判定を可能とする超高感度MRIが期待されます。
本成果は令和6年5月17日10時(日本時間)に米国化学会のJournal of the American Chemical Societyオンライン版に公開されました。
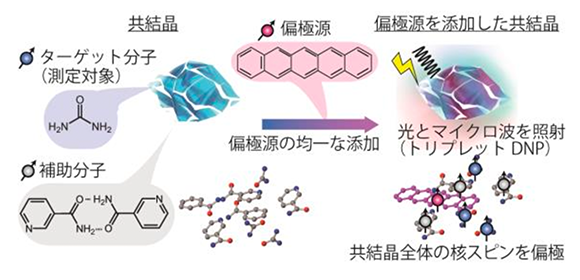
図1. ターゲット分子、補助分子、偏極源を含む共結晶の開発に成功しました。トリプレットDNPにより共結晶全体の核スピンのNMR信号を室温で増大することができます。
研究の背景と経緯
核スピン(原子核が持つ磁石のような性質)の振る舞いを見るNMR(核磁気共鳴)法は、分子や材料の構造や運動状態を調べる解析方法として広く利用されています。また、人体の内部に含まれる水分子が持つ水素原子核の核スピンを画像化したものがMRI(磁気共鳴イメージング)であり、医療分野において重要な検査法の一つです。それらの検出感度は、核スピンの向きの揃い具合(偏極率)に比例します。一般的な偏極率は極めて低く、より高度なNMRやMRI測定、例えば微小な腫瘍のMRI検出などは困難です。近年、比較的向きの揃いやすい電子スピンを利用して、核スピンの向きを揃えるDNP(動的核偏極)と呼ばれる方法が盛んに研究されています。しかしながら、一般的なDNPは、装置の一部であるミリ波発振源と極めて低い温度環境を作る液体ヘリウムに多額の費用が掛かるため、広く社会に普及していません。
一方、分子の光励起三重項が持つ電子スピンの偏りを高感度化に利用するトリプレットDNPは、極低温環境の代わりにレーザーを用いることで核スピンの高偏極化が可能です。レーザーとマイクロ波を照射することで引き起こされる量子力学的過程を利用しており、量子技術の一つとして注目されています。利点として、上記に挙げたミリ波発振源や液体ヘリウムなどの寒剤を使用せずに高い偏極率を得ることができます。しかしながら、試料中の核スピンが長いスピン緩和時間を持つ必要があり、かつ偏極源となる分子を均一に添加できることも必要です。それらを両立できる試料はほぼなく、適用できる分子や材料は限られています。
図2. NMR・MRIの感度を向上させる動的核偏極。本研究では、極低温の代わりにレーザーを使用することで核スピンを偏極します。
研究の内容と成果
研究グループは、トリプレットDNPが適用できる分子の種類を劇的に増やす方法として、ターゲット分子、補助分子、そして偏極源から組み上がる共結晶化技術を開発しました。一般的に共結晶を含む有機結晶の結晶構造は最も安定な構造です。密に分子が充填された結晶内部の運動は非常に小さく「硬い」状態です。その硬さによりスピン緩和は長くなるため、多くの共結晶がトリプレットDNPに適していることを発見しました。また共結晶の結晶構造内部に、偏極源となるペンタセンを、結晶構造を保ったまま均一に添加できることも見いだしました。共結晶は組み合わせ次第で、多彩な結晶構造や物性を示し、高い多様性を持っています。ターゲット分子として、MRI分子プローブの一つである尿素を選びました。ピルビン酸と尿素の二種類のMRI分子プローブを組み合わせたMRI計測の高感度化は、精密ながん診断や治療効果判定への応用が期待されています。本研究では、共結晶化技術を用いて尿素を含む多数の有機分子のトリプレットDNPに室温で成功しました。
図3. MRI分子プローブなどのターゲット分子、補助分子、そして偏極源から組み上がる共結晶。
図4. a) 共結晶のトリプレットDNPとb) MRI分子プローブの一つである尿素のトリプレットDNP
今後の展開
共結晶は、創薬の分野で広く研究されており、膨大な数の結晶構造が既に報告されて、データベースに格納されています。それらを参考にしながら、分子の組み合わせを最適化することで、偏極できる分子の種類を増やすことができ、より高い偏極率を得ることが期待できます。
トリプレットDNPは、比較的安価、かつコンパクトな装置で寒剤を一切使用せずに、偏極することが可能です。既設のMRIの側にトリプレットDNPの装置を設置することで、超高感度MRIによる精密がん診断が期待されています。本研究が提案する共結晶を用いたスピン偏極材料により、MRI分子プローブの室温トリプレットDNPを可能としました。超高感度MRIの実現に向けて大きく前進したと考えています。
特記事項
【発表者】
犬飼 宗弘(徳島大学 大学院社会産業理工学研究部理工学域 准教授)
佐藤 晴紀(徳島大学 大学院創成科学研究科 博士後期課程2年)
宮西 孝一郎(大阪大学量子情報・量子生命研究センター 講師)
根来 誠(大阪大学量子情報・量子生命研究センター 准教授、同大学ヒューマン・メタバース疾患研究拠点
准教授、量子科学技術研究開発機構量子生命科学研究所 チームリーダー兼任)
香川 晃徳(大阪大学ヒューマン・メタバース疾患研究拠点 特任准教授(常勤))
堀 優太(筑波大学計算科学研究センター 助教)
重田 育照(筑波大学計算科学研究センター 教授)
栗原 拓也(金沢大学理工研究域 助教)
中村 浩一(徳島大学 大学院社会産業理工学研究部理工学域 教授)
【論文情報】
掲載誌:Journal of the American Chemical Society
論文名:Cocrystalline Matrices for Hyperpolarization at Room Temperature Using Photoexcited Electrons
著者名:Munehiro Inukai, Haruki Sato, Koichiro Miyanishi, Makoto Negoro, Akinori Kagawa, Yuta Hori, Yasuteru Shigeta, Takuya Kurihara, Koichi Nakamura
DOI番号: 10.1021/jacs.4c01050
本研究は、文部科学省 光・量子飛躍フラッグシッププログラム(Q-LEAP)(グラント番号:JPMXS0120330644)、日本学術振興会科学研究費(グラント番号:21H01965)、JST次世代研究者挑戦的研究プログラム(グラント番号:JPMJFS2130)、JSPS WPI「ヒューマンメタバース疾患研究拠点(PRIMe)」、および徳島大学産業院ものづくり未来共創機構の支援を受けて実施されました。
用語説明
- DNP(動的核偏極、DNPDynamic Nuclear Polarization)
通常の分子中では、スピンの向きが反対の二つの電子が対になり、電子スピンによる電磁波の吸収、放出は打ち消されます。しかし、ラジカルと呼ばれる分子では不対電子が安定して存在しています。このようなラジカルを少量添加した試料に電子スピンが共鳴するマイクロ波を照射すると、電子スピンの首ふり運動の角度が変化します。この角度の変化する速度に、核スピンが共鳴する周波数が含まれるとき、電子スピンと核スピンの偏極率が交換されます。これによって核スピンの向きを揃えることを動的核偏極と呼びます。熱平衡状態の電子スピンを使ったDNPでは原理的には水素核スピンに対して最大660倍の信号強度増大が可能となります。温度が低いほど熱平衡状態の電子スピンの偏極率は大きくなるので、従来のDNPではより高感度化を求めて極低温下で行われています。
- NMR(核磁気共鳴、NMRNuclear Magnetic Resonance)
核スピンに静磁場をかけると、その磁場のまわりをコマのように歳差運動(首ふり運動)を行います。その歳差運動の周波数の電磁波(例えば、0.4テスラの磁場中の水素核スピンなら17 MHzの電磁波)を与えると、それに共鳴して首ふり運動の角度が変化し、放出された電磁波からその様子を観察できます。このような現象を核磁気共鳴(NMR)現象と呼びます。原子核の種類や分子構造の違いによって周波数が異なるので、この電磁波を解析することによって分子構造情報を調べることができます。これはNMR分光法と呼ばれ、化学分析に必要不可欠な方法となっています。
- MRI(核磁気共鳴画像、 MRIMagnetic Resonance Imaging)
スピンの歳差運動の周波数、共鳴する電磁波の周波数は静磁場の強さに比例します。そのため、試料に勾配のある磁場を与えておくと、同じ分子でも場所によって共鳴する電磁波の周波数が変わることになります。MRIは、勾配磁場を用いて人体内部に含まれる水分子などの量の分布を、共鳴する電磁波を解析することで画像化する方法で、けがや病気の診断や脳機能の研究などに欠かせない分析法となっています。
- トリプレットDNP(Triplet-DNPTriplet Dynamic Nuclear Polarization)
DNPの一種です。分子の光励起三重項が持つ電子スピンの偏りを核スピンに転写することで、NMRの検出感度を高感度化することができます。電子スピンの偏りは、温度や磁場の強度に依存しないため、温和な環境(例えば、寒剤を使用しない室温、そして電子スピンが共鳴する周波数がマイクロ波領域となる0.1~0.6 Tの低磁場環境)でDNPをすることができます。
- 共結晶
複数種の分子が水素結合やπ-π結合で組み上がる結晶です。本成果は色々な種類の共結晶に注目し、トリプレットDNPができることを示しました。
- MRI分子プローブ
分子センサーの一種で、生体内の環境や反応に応じて、NMRもしくはMRI信号が変化する分子です。
- 偏極率
静磁場中の水素核スピンや電子スピンのエネルギー準位は、スピンが磁場に対して平行な状態のエネルギーと反平行な状態のエネルギーに分裂します。それぞれのエネルギーを持つスピンの占有数の差を総スピン数で割ったものが偏極率と定義されています。一般的な環境下での熱平衡状態では、偏極率はスピンの磁気回転比と静磁場強度に比例し、温度に反比例します。電子スピンの磁気回転比は水素核スピンに比べ660倍大きいので、同環境下では電子スピンの方が偏極率は660倍大きくなります。
- スピン緩和
核スピンが集団で首ふり運動をしている時にその運動が揃っている状態からバラバラな状態へと引き戻そうとする緩和現象のことです。
