細胞組織培養に革新 硬化領域を「おへそ」に組織形成が進む?!
高分子で生体内の局所環境を模倣する新技術
研究成果のポイント
- 生体の硬さの多様性(脳は軟らかく、骨は硬い)と臓器形成との関わりは未解明な点が多く、特に、臓器発生の時に見られる硬い領域の意義は大きな謎。
- 均一で柔軟な培養材料の中央に“わざと”硬い領域を混ぜ込むと、組織形成のおへそ(中心)になることを発見(図1)。
- 様々な臓器組織の培養材料として再生医療の研究に貢献できる可能性がある。
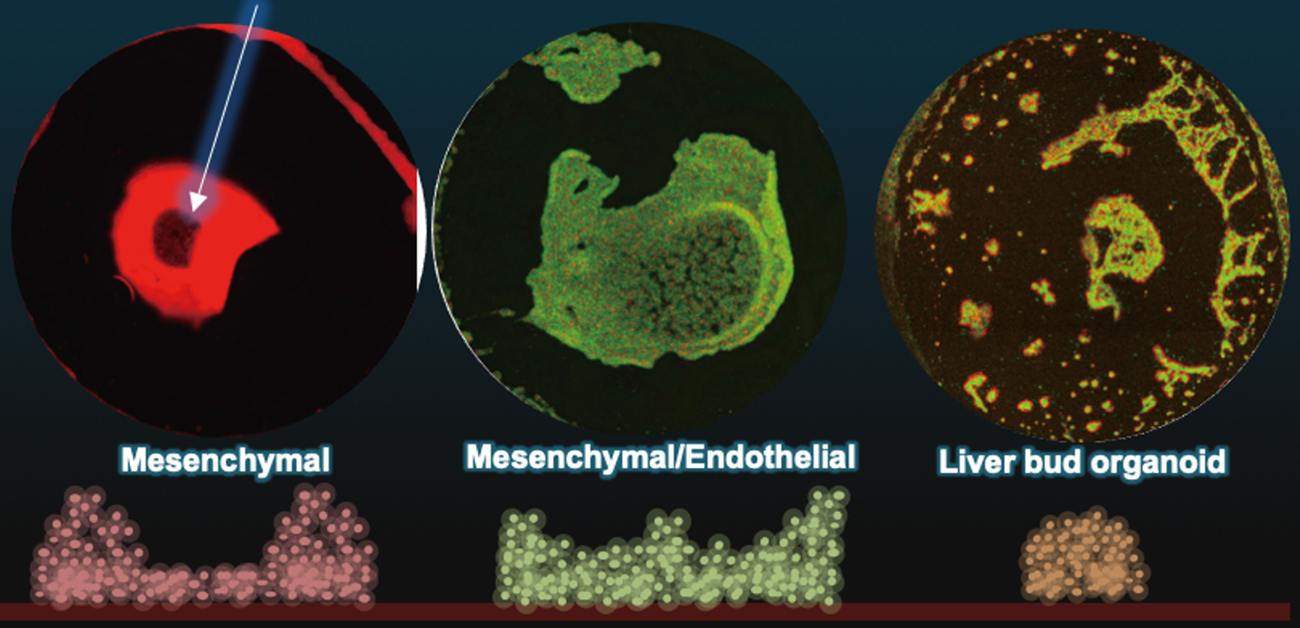
図1. 局所硬化の基板(柔らかい材料の中心に硬い領域が存在)の上で誘導される肝臓原基オルガノイド(肝臓の種、一番右)とその構成要素の細胞群。Mesenchymal cell: 間葉系細胞、Endothelial cell: 血管内皮細胞
概要
松﨑賢寿助教(大阪大学大学院工学研究科附属フューチャーイノベーションセンター若手卓越教員)、武部貴則教授(東京医科歯科大学大学院医歯学総合研究科先端医療開発学講座)、吉川洋史教授(大阪大学大学院工学研究科物理学系専攻応用物理学コース)らの研究チームは、柔軟な培養材料の中心に極端に硬い領域を持たせることで、組織の形を制御する新たな方法を確立しました。
生体は、硬い骨から柔らかい脳まで多様な硬さの臓器で形成されています。近年の研究で、臓器の硬さは、適切な臓器機能を発現するための重要因子であることがわかってきました。一方、硬さが臓器形成にどのように関与しているかについてはまだ未解明な点が多くあります。本研究では、筋肉組織や肝臓原基オルガノイド(ミニ臓器)が、培養基板の硬さの空間パターンに応答して組織形成することを見出しました(組織形成のおへそ)。本技術により様様な形態の組織を作製することが可能になることが期待され、今後組織の機能を評価することで、再生医療などへの応用検証を進めていく予定です。
研究の背景
生体は、脳のような軟らかい領域から、骨のような硬い領域まで、幅広い硬さ(ここではその物性値としてヤング率 [kPa]を定義)を示します。近年では、細胞やその組織は、このような生体内の多様な硬さ環境を認識し、分化などの機能を発現することが明らかとなり、生体内での“硬さ”と生命機能との関係を調べる研究(バイオメカニクス・メカノバイオロジー)が世界中で盛んになっています。これまで本研究チームでは、硬さ環境と臓器形成との相関に着目し、2015年には培養基板の硬さがミニ臓器の形成に重要であることを見出しました。一方、これまでの研究では均一な硬さの培養基板を用いてきましたが、生体内はマクロ・ミクロのレベルで空間的に不均一な硬さを示します。生体内の臓器形成過程においても、発生初期には硬さの特異な空間パターンが生じることが知られていますが、その役割については不明な点が多く残されていました。
研究の内容
本研究チームは、高分子で作製した培養基板の中心にわざと硬い領域を混ぜ込むと、その中心に向かって細胞運動が促され、組織形成の“おへそ”になることを発見しました。本高分子は光照射により固まる性質を有するため、おへその形を円、二等辺三角形、星へと様々な形の空間パターンを作製することができます。本研究グループでは、組織の形が、硬さの空間パターンに応答して多様に変化することがわかりました(図2)。
図2. 硬さの空間パターンに応答して形を変える細胞組織
本研究成果が社会に与える影響(本研究成果の意義)
今日では、世界中で様々なオルガノイドが培養皿の上で作られ、それを用いた臓器形成メカニズムの解明や、移植応用する再生医療研究が盛んに行われています。本研究で開発した硬さパターンを有した培養材料が、様々な臓器の再生医療を支える培養皿となることが期待されます。
特記事項
本研究成果は、2022年9月28日(水)午前0時(日本時間)に米国科学誌「iScience」(オンライン)に掲載され、同誌の特集号”Biomaterial control of cell and tissue dynamics”に選出されました。
タイトル:“Mechanical guidance of self-condensation patterns of differentiating progeny”
DOI:https://doi.org/10.1016/j.isci.2022.105109
著者名:Takahisa Matsuzaki*, Yuko Shimokawa, Hiroyuki Koike, Masaki Kimura, Yuma Kawano, Nao Okuma, Ryuzo Kawamura, Yosuke Yoneyama, Yasuro Furuichi, Fumihiko Hakuno, Shin-Ichiro Takahashi, Seiichiro Nakabayashi, Satoshi Okamoto, Hiromitsu Nakauchi, Hideki Taniguchi, Takanori Takebe*, and Hiroshi Y. Yoshikawa*
*Triple corresponding authors(図3).
なお、本研究は、日本学術振興会科学研究費助成事業(JP22H00302、JP22H05423、JP21H03790、JP21KK0195、JP20K21117、JP19K22416)、日本医療研究開発機構 再生医療実現拠点ネットワークプログラム(幹細胞・再生医学イノベーション創出プログラム)「内胚葉オルガノイドの線維化誘導とメカノスクリーン体系の創生」(20bm0704025h0003)、科学技術振興機構(創発的研究支援事業JPMJFR205N:松﨑賢寿、JPMJFR205K:古市泰郎 のTEAM-KINNIKU連携)、内藤記念科学振興財団、武田科学振興財団などの支援を受けて行われました。
図3. 3人の責任著者
参考URL
松﨑賢寿助教 Researchmap
https://researchmap.jp/7000026401
吉川洋史教授 研究室
https://mp-ap.eng.osaka-u.ac.jp
武部貴則教授 研究室
https://takebelab.com
SDGsの目標
用語説明
- オルガノイド
生体の器官に類似した組織構造体のこと。近年盛んに研究が進んでいる学問領域であり、これまで武部教授らは様々な臓器のオルガノイド(ミニ臓器)が作製可能であることを Nature 誌(Nature 499, 481-484, (2013)、Nature 574, 112–116 (2019)など)、Cell Reports誌(Cell Reports 21, 2661–2670 (2017))、Cell Metabolism 誌(Cell Metabolism 30, 374-384 (2019))にそれぞれ報告している。
- 培養基板の硬さ
本研究チームの武部教授、吉川教授、松﨑助教らは、培養基板の硬さが様々なオルガノイド形成制御に重要であることを見出し、2015年に論文発表した(Cell Stem Cell, 16(5):556-65, 2015)。
- TEAM-KINNIKU
創発的研究支援事業では、研究代表者の松﨑賢寿助教と古市泰郎助教(東京都立大学)らが重要な臓器の一つである骨格筋の再生機序を解明する医理工連携(TEAM-KINNIKU)を進めています。本成果はTEAM-KINNIKU初の成果となります。


