急性骨髄性白血病(AML)の新しい治療法を開発
臍帯血由来の免疫細胞療法による白血病治療の新展開
研究成果のポイント
- 同種造血幹細胞移植後に再発した急性骨髄性白血病(AML)患者に対し、新しく「CAR T細胞療法」、および「臍帯血由来CAR NK細胞療法」を開発
- AMLは、同種造血幹細胞移植後の再発により死亡するケースが多く、また、他の血液がんで効果を発揮する「CAR T細胞療法」のターゲットとなりうる抗原が見つかっていなかった
- KG2032抗体由来のCAR T細胞、および臍帯血由来CAR NK細胞を作製したところ、いずれも高い抗腫瘍効果を示した
概要
大阪大学免疫学フロンティア研究センターの池田峻弥 特任研究員(常勤)(免疫細胞治療学)、大学院医学系研究科保仙直毅 教授(血液・腫瘍内科学/免疫学フロンティア研究センター免疫細胞治療学)らの研究グループは、同種造血幹細胞移植後に再発した急性骨髄性白血病(AML)患者に対し、HLA-DRB1タンパクの遺伝子多型を標的とした新規CAR T細胞、および臍帯血由来CAR NK細胞療法を開発しました。
AML患者の多くは化学療法のみでは治らず、同種造血幹細胞移植を行いますが、再発により死亡する症例は少なくありません。CAR T細胞療法は患者自身のT細胞に遺伝子改変を施してがん細胞を攻撃する治療法で、白血病や悪性リンパ腫などの治療に用いられます。AMLに対してもその開発が期待されていますが、今のところ良い標的抗原が見つかっていないのが現状です。
今回、研究グループは、自作した14,000個の抗AML細胞抗体の中から、多様なHLA-DRB1(白血球の血液型のようなもので人によって型が異なる)のうち約半分の型を認識するKG2032抗体を見出しました。一部の患者では、KG2032抗体を元にCAR T/ NK細胞を作製すれば、同種移植後に再発したAML患者の正常血液細胞は攻撃せずに、白血病細胞だけを攻撃することができます(図1)。そこで、KG2032由来CAR T細胞、および臍帯血由来CAR NK細胞を作製したところいずれも著明な抗腫瘍効果を示しました。
本研究成果により、今まで同種造血細胞移植をもってしても救えなかったAML患者の一部を救うことができる可能性があります。さらに、臍帯血を用いたCAR NK細胞が実用化されれば、すぐに使える、より安価な遺伝子細胞治療を実現する可能性があります。
本研究成果は、「Nature Cancer」に3月24日(月) に公開されました。
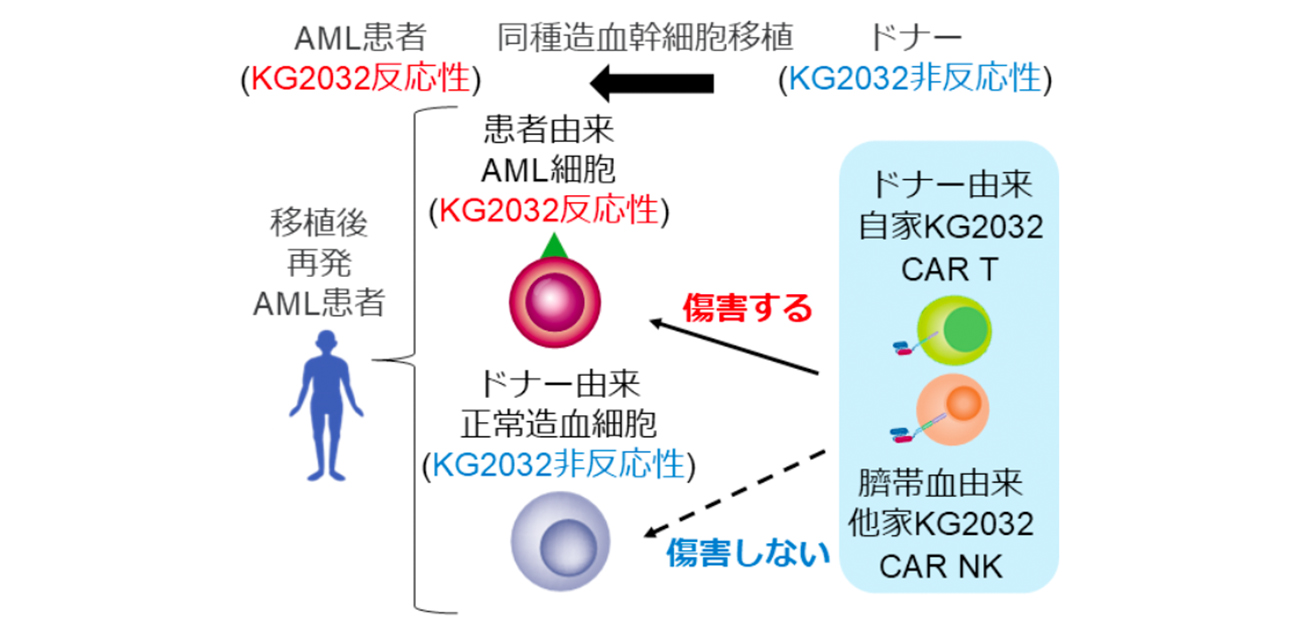
図1. 同種造血幹細胞移植後再発急性骨髄性白血病に対する新規CAR T/臍帯血由来CAR NK細胞療法
KG2032反応性AML患者がKG2032非反応性ドナーから同種造血幹細胞移植を受けた場合、KG2032由来の CAR を導入したドナーT細胞あるいは臍帯血由来NK細胞を投与すれば、患者由来AML細胞は傷害されるが、ドナー由来正常造血細胞は傷害されない。
研究の背景
AML患者さんの多くは化学療法のみでは治らないため、同種造血幹細胞移植を行います。しかしながら、再発による死亡が多く、同種移植後のAML患者さんに対する新たな治療法が必要とされています。他の血液がんではCAR T細胞が驚異的な効果を示しており、AMLに対してもCAR T細胞の開発が期待されていますが、AML細胞と正常造血細胞を見分けることの可能な良い標的抗原が存在しないのが現状です。また、CAR T細胞は患者さんごとに製造する必要がありますが、製造に時間がかかる上、コストが高く、他家由来の細胞治療の開発が望まれています。
研究の内容
研究グループはAML細胞に結合するモノクローナル抗体を多種類作製し、新たな抗原を探すところから研究をスタートしました。研究グループはAML細胞に結合するモノクローナル抗体約14,000クローンの中からB細胞以外の健常人末梢血に結合せず、AML患者さんの骨髄由来AML細胞に強く結合するKG2032という抗体を同定しました。また、KG2032が結合するタンパク質がHLA-DRB1であることを明らかにしました。HLA-DRB1とは白血球の血液型のようなもので個人により型が異なりますが、KG2032は約半分の型に結合することが分かりました。
同種造血細胞移植は多くのAML患者において行われますが、患者さんとドナーでHLA-DRB1の型が異なることはよくあります。患者さんのAML細胞が持つHLA-DRB1にKG2032が結合し、ドナーのそれには結合しない場合、KG2032はAML細胞だけを特異的に認識します。そこでKG2032抗体を元にCAR T細胞を作製したところ、著明な抗腫瘍効果を示しました(図2上)。
さらに、研究グループではKG2032由来CARを用いて、臍帯血由来CAR NK細胞の開発を行い、AML細胞に対して著明な抗腫瘍効果を持つことを示しました(図2下)。
図2. KG2032 CAR T/CAR NK細胞の著明な抗腫瘍効果
光の強さが腫瘍量を反映している。コントロール細胞投与群では、経時的な腫瘍量増加が見られるが、KG2032 CAR T/NK細胞投与群では腫瘍量の増加が見られず、著明な抗腫瘍効果が認められた。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、今まで同種造血細胞移植をもってしても救えなかったAML患者さんの一部を救うことができる可能性があります。また、同種造血幹細胞移植後という状況において、血液細胞に発現する多型分子がCAR T/CAR NK細胞の治療標的として使えることを初めて示しました。さらに、臍帯血を用いたCAR NK細胞が実用化されれば、すぐに使える、より安価な遺伝子細胞治療を実現する可能性があります。
特記事項
本研究成果は、2025年3月 24日(月) 19時(日本時間)に「Nature Cancer」(オンライン)に掲載されました。
【タイトル】“CAR T or NK cells targeting mismatched HLA-DR molecules in acute myeloid leukemia after allogeneic hematopoietic stem cell transplant”
【著者名】 Shunya Ikeda1,21, Kana Hasegawa1,21, Yosuke Kogue2, 3,21, Takao Arimori4, Ryuhei Kawamoto5, Tansri Wibowo6, Moto Yaga6, Yuri Inada5, Hirofumi Uehara5, Miwa Matsubara5, Mana Tachikawa5, Makiko Suga3, Shuhei Kida3, Kumi Shibata3, Kazuhito Tsutsumi3, Kentaro Fukushima3, Jiro Fujita3, Tomoaki Ueda3, Shinsuke Kusakabe3, Akihisa Hino3, Michiko Ichii3, Asao Hirose7, Hirohisa Nakamae7, Masayuki Hino7, Takafumi Nakao8 Megumu Inoue9, Kyoko Yoshihara10, Satoshi Yoshihara10, Shuji Ueda11, Tetsuro Tachi12, Hideki Kuroda12, Koki Murakami12, Noriyuki Kijima12, Haruhiko Kishima12, Eri Igashira13, Mari Murakami13, Tsuyoshi Takiuchi14, Tadashi Kimura14, Takashi Hiroshima15, Toru Kimura15, Yasushi Shintani15, Chihaya Imai16, Kosuke Yusa17, Ryota Mori18, Takayuki Ogino18, Hidetoshi Eguchi18, Kiyoshi Takeda1, 13, 19, 20, Yusuke Oji5, Atsushi Kumanogoh1, 6, 19, 20, Junichi Takagi4, Naoki Hosen1, 3, 19, 20* (*責任著者)
【所属】
1. 大阪大学 免疫学フロンティア研究センター(iFReC)
2. 大塚製薬株式会社 大阪創薬研究センター
3. 大阪大学 大学院医学系研究科 血液・腫瘍内科学
4. 大阪大学 蛋白質研究所
5. 大阪大学 大学院医学系研究科保健学専攻生体病態情報科学講座
6. 大阪大学 大学院医学系研究科 呼吸器・免疫内科学
7. 大阪公立大学 大学院医学系研究科 血液腫瘍制御学
8. 大阪市立総合医療センター 血液内科
9. 市立伊丹病院 血液内科
10. 兵庫医科大学病院 血液内科
11. 兵庫県立西宮病院 血液内科
12. 大阪大学 大学院医学系研究科 脳神経外科学
13. 大阪大学 大学院医学系研究科 免疫制御学
14. 大阪大学 大学院医学系研究科 産科学婦人科学
15. 大阪大学 大学院医学系研究科 呼吸器外科学
16. 富山大学 学術研究部医学系 小児科学講座
17. 京都大学 医生物学研究所 幹細胞遺伝学分野
18. 大阪大学 大学院医学系研究科 消化器外科学
19. 大阪大学 先導的学際研究機構(OTRI) 生命医科学融合フロンティア研究部門
20. 大阪大学 感染症総合教育研究拠点(CiDER)
21. 同等貢献
DOI:https://doi.org/10.1038/s43018-025-00934-1
本研究は、日本医療研究開発機構(AMED)(次世代がん医療創生研究事業(2019-2020急性骨髄性白血病に対する新規CAR-T細胞療法の開発、2021-2022急性骨髄性白血病に対する新規CAR-T細胞療法の開発)、再生・細胞医療・遺伝子治療実現加速化プログラム(2021-2023多発性骨髄腫に対する臍帯血由来CAR-NK細胞療法の開発)、革新的がん医療実用化研究事業(2023-2025, 同種造血幹細胞移植後再発急性骨髄性白血病患者に対する新規CAR-T細胞の開発),再生医療等実用化研究事業(2024-2026, 同種造血幹細胞移植後急性骨髄性白血病患者に対する臍帯血由来新規CAR-NK細胞の開発)、生命科学‣創薬研究支援基盤事業(2022-2026、創薬ターゲットおよびバイオ医薬候補品の高品質生産の支援))、日本学術振興会(JSPS)科研費(JP19K16799、 JP21K15487、JP26461404、JP20H03710)、化学及血清療法研究所、武田科学振興財団の支援を受けて行われました。
参考URL
大阪大学大学院医学系研究科血液・腫瘍内科学
https://www.med.osaka-u.ac.jp/pub/bldon/
用語説明
- 同種造血幹細胞移植
ドナーから採取した造血幹細胞を患者に移植する治療法が造血幹細胞移植である。自己の造血幹細胞を移植する自家移植と他人から移植する同種移植があり、同種移植ではドナーのリンパ球ががん細胞を攻撃する効果がある。
- CAR T細胞療法
リンパ性白血病やリンパ腫に対して効果を示してきた強力ながん免疫療法の一つである。がん細胞に結合する抗体の抗原認識部位とT細胞を活性化させる4-1BBおよびCD3を融合したキメラ抗原受容体(CAR)を患者のT細胞に発現させることにより作製されたCAR T細胞は、標的抗原と反応して活性化し、強い細胞傷害活性を発揮し、増殖することによって抗腫瘍効果を示す。
- CAR NK細胞療法
NK細胞はリンパ球の1種であり、がん細胞やウイルス感染細胞を排除する。NK細胞に上述のCARを発現させたCAR NK細胞はCAR T細胞と比べて製造コストが低く抑えられ、またCAR T細胞療法の副作用として起こり得るサイトカイン放出症候群を起こさないことが知られている。
- HLA-DRB1
エイチエルエーディーアールビーワン。白血球の血液型として発見されたヒト白血球抗原(HLA)のクラスII抗原DRの遺伝子型。B細胞やマクロファージ、樹状細胞などの抗原提示細胞に主に発現しているタンパク質である。
- 遺伝子多型
個体間で異なるDNAの塩基配列を持つこと。
