母体の口腔環境と子どもの腸内健康が関連していることを発見
口腔ケアに基づく消化器疾患の予防法・治療法開発に期待
研究成果のポイント
概要
大阪大学免疫学フロンティア研究センター免疫微生物学の北本宗子特任准教授(常勤)と鎌田信彦特任教授(常勤)(大阪大学感染症総合教育研究拠点、米国ミシガン大学との兼任)、ミシガン大学医学部消化器内科学の原口雅史研究員(研究当時)らの研究グループは、母親由来の口腔細菌が子の腸炎発症に関与していることを明らかとしました。
乳児は母親の様々な部位(皮膚、口腔、腸、膣など)から微生物を受け取り、それらは乳児の腸内に早期に定着することが示されています。そのため、健康な母体の微生物叢の乱れ、特に腸内微生物叢の乱れ(腸内ディスバイオシス)は、子の腸内微生物叢の構成に影響を及ぼし、健康状態にも影響を与える可能性があります。しかし、腸以外の母体微生物が乳児の健康や疾患に与える影響については、ほとんど研究されていませんでした。
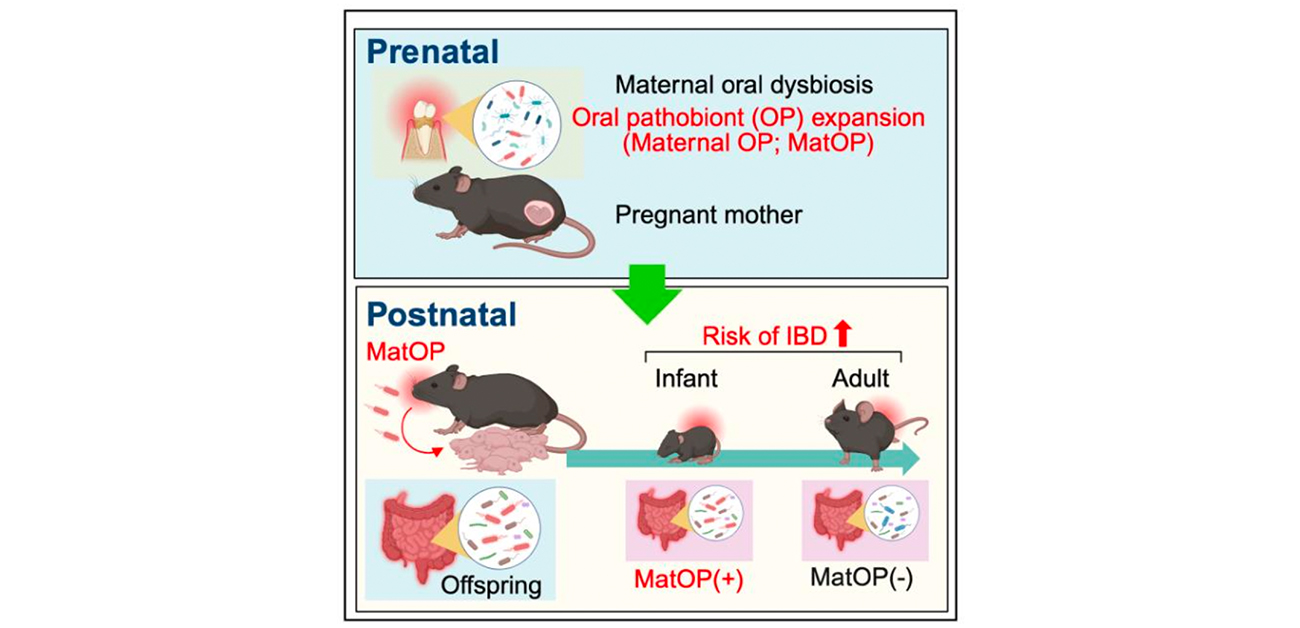
今回、研究グループは、母体の口腔内ディスバイオシスが子どもに持続的な健康影響を及ぼす可能性があることを示しました。本研究では、歯周炎マウスモデルを用いて、母体において歯周炎が誘発されると、口腔内病原性細菌の増殖を促進し、これが乳児の腸内に垂直伝播して腸管免疫システムを変化させた結果、腸炎への感受性が高まる(炎症性腸疾患の様態を模す)ことを見出しました。また、母体由来の口腔病原性細菌は子の腸内細菌叢が成熟するとともに排除されるものの、子の腸炎感受性は成人期まで持続することを明らかとしました。このことから、母体の口腔内ディスバイオシスは乳児の早期腸内微生物叢を変化させるだけでなく、子の長期的な健康にも影響を及ぼす可能性があると考えられます(図1)。
今回の研究成果は、周産期における母親の口腔健康の重要性を示唆しており、母親の口腔微生物叢を適切に管理することが、子どもの将来の腸疾患や免疫関連疾患(炎症性腸疾患など)のリスク軽減につながる可能性に期待できます。
本研究成果は、米科学誌「Cell Reports」に7月16日(水)に公開されました。
図1. 本研究の概要
歯周炎により口腔ディスバイオシスを誘導した母マウス (MatOP) から産まれた子は、腸管の炎症感受性(炎症性腸疾患のリスク)が高い。
研究の背景
ヒトを含む哺乳動物は、母親の胎内にいる間は無菌状態であり、出生後に外部から細菌を獲得することで腸内細菌叢が形成されます(=早期定着腸内細菌)。新生児や乳児は食事など様々な環境由来の細菌に加え、出生時および出生後に母親との密接な接触を通じて、母親の様々な体表や粘膜組織(口腔、皮膚、膣、腸管)から共生細菌を獲得することが知られています。この母子間の垂直感染によって形成される早期定着腸内細菌叢は、粘膜免疫の寛容性を促進し、乳幼児の免疫システムの構築や長期的な健康維持において重要な役割を果たすことが明らかとなってきました。
一方で、新生児・乳児期における早期定着腸内細菌の乱れ(例:抗生剤投与)は、将来的に炎症性腸疾患や精神疾患、アレルギー疾患などの発症リスクを高める可能性があることも報告されています。しかしながら、母親から移行してきた細菌が具体的にどこに由来し、また子の健康や疾患にどのように関与しているかについては、多くの点が未解明のままです。
研究グループは以前、口腔内ディスバイオシスが炎症性腸疾患の発症に寄与していることを、動物モデルおよびヒト検体を用いた研究によって明らかにしました(S. Kitamoto et al., Cell 2020. J. Imai et al., JCI insight 2021.)。よって本研究では、母親の口腔内ディスバイオシスが乳児の腸内細菌叢に与える影響や、炎症性腸疾患の病態形成に関与し得るのかを検証しました。
研究の内容
今回、研究グループでは、母親の口腔内ディスバイオシスが子の腸内細菌叢に与える影響について、歯周炎マウスモデルを用いて検証を行いました。まず、妊娠前の雌マウスにリガチャーを挿入して口腔内ディスバイオシスを誘発し、さらに口腔病原細菌であるKlebsiella aerogenes(K. aerogenes)を経口投与した後、雄マウスと交配させ、母から子への細菌伝達を解析しました。まず、口腔内ディスバイオシスを持つ母マウスから産まれた仔マウス(生後2週齢)と口腔内ディスバイオシスを持たない母マウス(リガチャーを長期挿入しておらず歯周炎が発症していないマウス:以下、コントロール群)から産まれた仔マウスの腸内細菌叢を解析したところ、母体の口腔内ディスバイオシスが仔マウスの腸内微生物叢の初期コロニー形成に影響を与えることが確認されました。さらに、口腔内ディスバイオシスを持つ母マウスから生まれた仔マウスの腸管内はK. aerogenesが顕著に増加しており、母体由来の口腔内病原性細菌が仔の腸へ移行していることを確認しました。一方で、コントロール群から産まれた仔マウスの腸管内では、K. aerogenesは検出されませんでした。これらの結果を踏まえ、母体の口腔内ディスバイオシスが、乳幼児の腸管免疫システムに与える影響を検証した結果、口腔内ディスバイオシスを持つ母マウスから産まれた仔マウスの腸管内では、炎症性腸疾患の腸炎憎悪に関与すると考えられているRORγt陽性Th17細胞や組織常在性記憶 T 細胞 (tissue-resident memory T cell: TRM) の増加および炎症関連遺伝子の亢進がみられました (コントロール群から産まれた仔と比較して)。
さらに研究グループは、これらのモデルから産まれた仔マウス(生後2週齢)に対して、抗CD3抗体を投与し腸炎を誘導したところ、口腔内ディスバイオシスの母から産まれた仔マウスの腸炎は、コンロール群の仔マウスよりも重度であることが明らかとなり、母体の口腔内ディスバイオシスが子の腸炎感受性を高めることが示唆されました(図2)。さらに、交叉保育実験から、母体由来口腔病原細菌が子へ暴露される時期が、妊娠期よりも出生後の方が後の子の腸炎感受性に大きな影響を与えることを見出しました。
また、生後7週齢(成人期)の時点でも口腔内ディスバイオシスを持つ母から産まれた仔マウスでは、腸管免疫プロファイルおよび腸内細菌構成の変化、またそれに伴う腸炎感受性の高さが確認されました。この結果は、母体の口腔内ディスバイオシスが子の健康に長期的な影響を及ぼす可能性を示しています。
図2. IBDリスク因子を保有する母から産まれ仔は腸炎感受性が高い
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果は、母体の口腔状態が子どもの将来の健康に深く関わることを示しました。母体の口腔内微生物叢を改善するための予防的介入(例:歯周病治療やプロバイオティクスの利用)が、子どもの将来の腸疾患や免疫関連疾患のリスク軽減につながる可能性があると考えられ、この知見を基づき、新たな医療政策や介入方法の開発が期待されます。
特記事項
【掲載紙】米国科学雑誌 Cell Reports(オンライン)2025年7月16日
【タイトル】Transmission of maternal oral pathobionts to the infant gut predisposes offspring to exacerbated enteritis
【著者名】Masafumi Haraguchi,1,2,11 Yeji Kim,1,11 Natsuru Watanabe,1,11 Kyoko Yamazaki,1 Kira L. Newman,1 Merritt G. Gillilland III,1 Yijie Guo,1,3 Daisuke Watanabe,1,4 Ingrid L. Bergin,5 Takehiro Suzuki,6 Daisuke Motooka,7 Kohei Sugihara,6 Sho Kitamoto,6 Hiroko Nagao-Kitamoto,6,*, and Nobuhiko Kamada.1,6,8,9,10,12,* *
11:These authors contributed equally
*:Co-Corresponding author
* *:Corresponding author
【所属】
1. Division of Gastroenterology and Hepatology, Department of Internal Medicine, University of Michigan
2. Department of Gastroenterology and Hepatology, Nagasaki University Graduate School of Biomedical Sciences
3. Department of Psychiatry and Center for Brain Science, The First Affiliated Hospital of Xi’an Jiaotong University
4. Division of Gastroenterology, Department of Internal Medicine, Kobe University Graduate School of Medicine
5. The Unit for Laboratory Animal Medicine, University of Michigan
6. WPI Immunology Frontier Research Center, The University of Osaka
7. NGS Core Facility, Bioinformatics Center, Research Institute for Microbial Diseases, The University of Osaka
8. Department of Pathology, University of Michigan
9. Center for Infectious Disease Education and Research, The University of Osaka
【DOI】https://doi.org/10.1016/j.celrep.2025.115974
本研究は、アメリカ国立衛生研究所(NIH)日本学術振興会科研費(JSPS)、武田科学振興財団、日本医療研究開発機構(AMED)革新的先端研究開発支援事業ステップタイプ(FORCE)JP25gm4010030「炎症性腸疾患における母子移行共生細菌と疾患リスク」(研究代表者:鎌田信彦)、AMED 革新的先端研究開発支援(PRIME)JP21gm6310023「新生児期腸内細菌叢に存在する免疫寛容誘導細菌の同定」(研究代表者:鎌田信彦)、AMED 難治性疾患実用化研究事業 JP24ek0109775「母体垂直伝播から捉える超早期発症炎症性腸疾患の病態形成機序」(研究代表者:北本宗子)の支援により行われました。
用語説明
- ディスバイオシス
生体内の細菌叢のバランスが乱れた状態。腸内においては、腸内細菌叢の恒常性が損なわれた状態を指す。この状態では、通常腸内に共存している有益な細菌が減少したり、有害な細菌が異常増殖したり、腸内細菌叢のバランスが乱れている。
- 腸内細菌叢
腸内に存在する多種多様な微生物(主に細菌)が集団で無数に生息する様子を「草むら(叢)」に例えて、腸内細菌叢と呼ぶ。
- 微生物
肉眼でみることができない非常に小さな生物の総称。主に、細菌、ウイルス、真菌、原虫などが含まれる。微生物の集まりやコミュニティを微生物叢と呼ぶ。
- 歯周炎マウスモデル
C57BL/6マウスの上顎の大臼歯間にリガチャー(Ligature)と呼ばれる手術用の絹糸を挿入し歯周炎を誘導。リガチャー挿入後、1~2週間程度で歯周炎が発症し、口腔内ディスバイオシスが起こることを確認(S. Kitamoto et al., Cell 2020)。
- 炎症性腸疾患
Inflammatory Bowel Disease(IBD)。腸を中心とする消化管粘膜に慢性の炎症や潰瘍をひきおこす原因不明の腸疾患の総称。
- 交叉保育
動物実験において、異なる母親から生まれた新生児を交換し、別の母親に育てさせる飼育方法。本研究では、口腔内ディスバイオシスをもつ母マウスから産まれた仔マウスをコントロール母マウスに養育させ、コントロール母マウスから産まれた仔マウスを口腔内ディスバイオシスをもつ母マウスに養育させた。
