「放射化イメージング」でマウス体内の金ナノ粒子を可視化
がん治療薬の長期的な動態イメージングに向けて
研究成果のポイント
- がん治療薬を腫瘍へ運ぶ金ナノ粒子のイメージング技術をマウス実験で実証
- これまで困難だった核医学治療薬(アルファ線放出核種)の長期動態追跡を実現
- 様々な治療薬の長期的な体内動態をイメージングする手法としての応用に期待
概要
早稲田大学大学院先進理工学研究科博士後期課程1年の越川 七星(こしかわ ななせ)と、同大学理工学術院の片岡 淳(かたおか じゅん)教授らの研究チームは、大阪大学放射線科学基盤機構の豊嶋 厚史(とよしま あつし)教授、角永 悠一郎(かどなが ゆういちろう)特任助教(常勤)、加藤 弘樹(かとう ひろき)特任教授(常勤)、京都大学複合原子力科学研究所の高宮 幸一(たかみや こういち)教授らと共同で、薬剤キャリアである金ナノ粒子を直接可視化する「放射化イメージング」を提案し、実際に金ナノ粒子をマウスに投与して体内分布を可視化しました。
また、腫瘍をピンポイントで攻撃するアルファ線治療薬アスタチンAt-211を、放射化金ナノ粒子に標識することにも成功しました。これにより、これまで困難であったAt-211の長期的な動態追跡を実現しました。今後は様々な治療薬で、動態可視化への応用が期待されます。本成果をまとめた論文は、論文誌『Applied Physics Letters』の”Featured article”に選ばれたほか、AIP(米国物理学協会)発行の論文全体から顕著な成果を特集するScilight (Science highlight) で紹介されます。
本研究成果は、2025年3月12日(水)午前10時(米国東部標準時)に『Applied Physics Letters』のオンライン版で公開されました。
図. 金ナノ粒子のイメージング
研究の内容
(1)これまでの研究でわかっていたこと
がんは、長きにわたって日本人の死因第一位であり、効果的で負担の少ない治療法が求められています。がんの治療法には様々なものがありますが、放射性の治療薬を投与して腫瘍へダメージを与える核医学治療は、手術が要らず副作用の少ない方法として注目されています。
近年、核医学の分野では、アルファ線を放出する治療薬が盛んに研究されています。アルファ線は狭い範囲に大きなエネルギーを与える放射線で、腫瘍だけを効果的に攻撃することが期待されます。中でも質量数211のアスタチン(At-211)は、国内のサイクロトロンで比較的簡単に製造できることから有望視されています。また、At-211はアルファ線だけでなく、エネルギー79 keV(キロ電子ボルト)のX線を放出します。マウスの体を透過してきたX線を検出することで、At-211を体の外からイメージングできます。
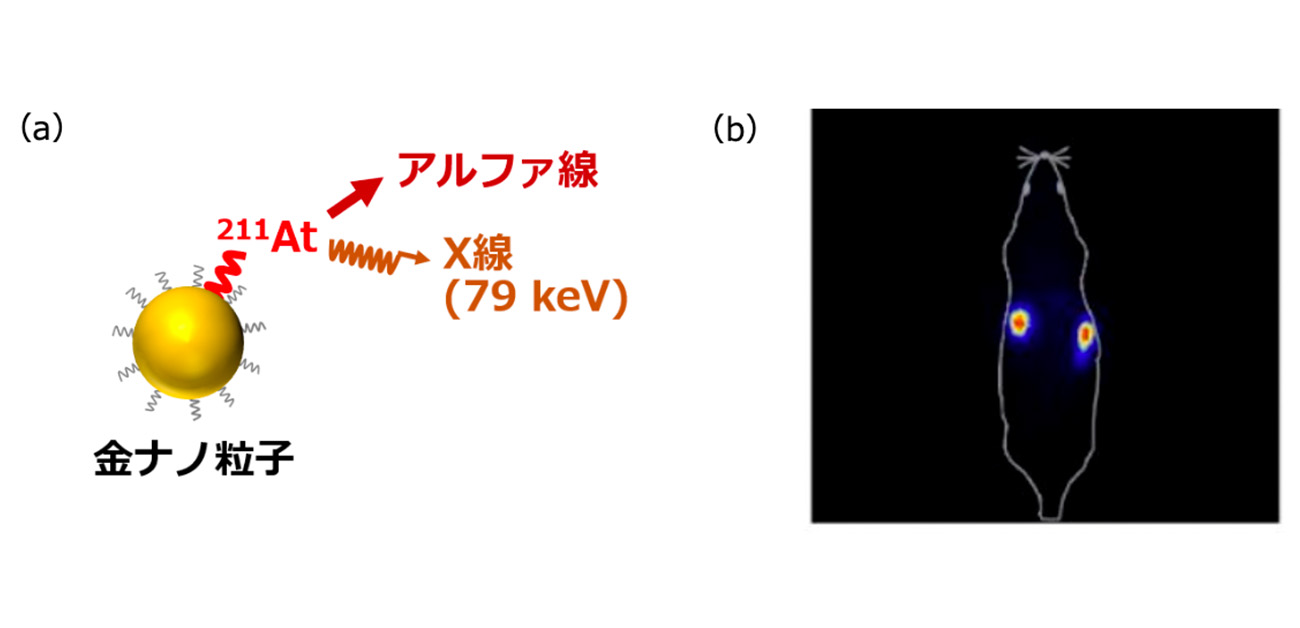
効果的かつ副作用の少ない治療を実現するには、At-211をはじめとする治療薬を腫瘍へ届け、集積させる必要があります。治療薬を腫瘍へ運ぶ「薬剤キャリア」として特に注目を集めているのが、ナノサイズ(直径が10-9 m程度)の金の粒子(金ナノ粒子)です。実際に、図1 (a)のように金ナノ粒子にAt-211を標識して腫瘍に投与すると、図1 (b)のように金ナノ粒子が腫瘍に留まり、高い治療効果が得られることがわかっています[1]。次のステップとして、マウス実験により集積から排出まで、数日間にわたる長期の動態を調べることが不可欠です。これまで、At-211からのX線を使ってAt-211標識金ナノ粒子のイメージングが行われてきました。しかし、At-211の半減期は7.2時間と短く、投与から2日後にはX線の強度は約1/100になってしまうため、数日間にわたる動態を追うことはできませんでした。また、この方法では体内でAt-211と金ナノ粒子が分離してしまっているかどうか調べられないことも問題でした。
図1. (a) At-211標識金ナノ粒子。At-211はアルファ線とX線を放出する。(b) At-211標識金ナノ粒子を投与したラットのイメージング結果(投与4時間後。Kato et al. (2021)[1]より転載)。
(2)今回の研究で新たに実現しようとしたこと
本研究では、金ナノ粒子の「放射化イメージング」により、At-211と金ナノ粒子の個別イメージング、そしてAt-211標識金ナノ粒子の長期的な動態追跡を目指しました。放射化とは、安定な原子を放射性同位体に変えることです。自然界に存在する金は質量数が197の安定な元素です。これに熱中性子(エネルギーの低い中性子)をぶつけると、金の原子核の一部が中性子を取り込んで質量数が198の金(Au-198)に変わります。Au-198は半減期が2.7日の放射性同位体で、エネルギー412 keVのガンマ線を放出します。金ナノ粒子に含まれる金の一部を放射性のAu-198に変え、ガンマ線を体外から検出することで、金ナノ粒子の体内分布を体外から可視化できます。
金ナノ粒子をイメージングする技術には、他にもトレーサー(放射性物質や造影剤)による標識やCTイメージング(コンピュータ断層撮影)があります。しかし、トレーサーが金ナノ粒子から外れてしまう可能性があること、CTでは金ナノ粒子が高濃度(mg/mL程度)でないとイメージングできないことが課題となっていました。放射化イメージングは金ナノ粒子を直接イメージングする手法であり、3桁も低い濃度(μg/mL程度)であってもイメージングができるという点で、これまでの制限を打破する方法となり得ます。At-211標識した放射化金ナノ粒子を図2 (a)に示します。79 keVのX線、412 keVのガンマ線を使ってAt-211と金ナノ粒子の分布を個別にイメージングし、At-211が金ナノ粒子から外れていないかを確認できると考えました。さらに、At-211は半減期7.2時間で急激に減衰しますが、半減期2.7日のAu-198は数日間ガンマ線を出し続けるので、At-211標識金ナノ粒子の集積と代謝を数日間にわたり追うことができます。
At-211と金ナノ粒子を独立にイメージングするには、数十 keVからMeV(メガ電子ボルト)付近まで、幅広いX線・ガンマ線を1台かつ同時に識別できる「広帯域のカメラ」が必要です。しかし、従来のSPECT(単一光子放射断層撮影)では約300 keV以下、PET(陽電子放出断層撮影)では511 keVのみと、イメージングできるX線・ガンマ線のエネルギーが限られていました。そこで、独自に開発した「ハイブリッド・コンプトンカメラ」をイメージング装置として用いました。ハイブリッド・コンプトンカメラは、低エネルギー(200 keV以下)用のピンホールモードと高エネルギー(200 keV以上)用のコンプトンモードの2種類の方法でイメージングができます。図2 (b)に示すように、装置は2枚の検出器(散乱体と吸収体)で構成され、散乱体には3×3 mm2の孔が空いています。低エネルギーのX線・ガンマ線は散乱体に当たると吸収され、孔を通ったものだけが吸収体に届くので、ピンホールカメラの原理でイメージングができます(図中①)。高エネルギーのガンマ線は散乱体でコンプトン散乱され、吸収体で吸収されます。散乱体・吸収体での検出エネルギーから散乱角を計算することでイメージングが可能です(図中②)。
図2. (a) At-211標識した放射化金ナノ粒子。(b) ハイブリッド・コンプトンカメラ。
低エネルギーのX線・ガンマ線は①のように、高エネルギーのガンマ線は②のように検出される。
(3)新しく開発した手法と、それによる実証結果
本研究では、まずマウスに投与できる、極小サイズの金ナノ粒子を合成する手法を模索しました。試行を重ね、四塩化金酸(HAuCl4)を材料として粒径5 nm(ナノメートル)ほどの金ナノ粒子を安定的に合成することに成功しました。次に、京都大学研究用原子炉(KUR)[4]を用いて四塩化金酸を放射化し、同じ手順に沿って放射化金ナノ粒子を合成しました。続いて、At-211の標識で不可欠となる、メトキシポリエチレングリコール(mPEG)で放射化金ナノ粒子を表面修飾し、マウスの腫瘍に投与しました。ハイブリッド・コンプトンカメラで得られたガンマ線のエネルギースペクトルを図3 (a)に示します。412 keVにピークが見られ、放射化によるAu-198の生成が確認できました。投与9分後、4日後に、コンプトンモードでイメージングした結果を図3 (b)に示します。4日後も金ナノ粒子が腫瘍付近に留まっている様子をイメージングでき、これまで不可能であった長時間の動態追跡に有効な方法であることが示されました。
次に、放射化金ナノ粒子にAt-211を標識し、マウスの尾静脈から投与しました。投与9分後、2日後のガンマ線エネルギースペクトルとイメージング結果を図4に示します。投与9分後のエネルギースペクトルには、79 keV(At-211)と412 keV(Au-198)にピークが見られます。また、At-211と金ナノ粒子(Au-198)それぞれのイメージングに成功しました。79 keVのX線はピンホールモード、412 keVのガンマ線はコンプトンモードで解析することで、1回の測定でAt-211と金ナノ粒子の分布を個別に知ることができます。At-211と金ナノ粒子が概ね同じ位置に集積していることを確認できました。投与2日後のエネルギースペクトルでは、At-211の減衰によって79 keVのピークは非常に弱くなっている一方、Au-198由来の412 keVはピークの高さがあまり変わりません。イメージング結果では、At-211は減衰により分布を見ることができないのに対し、金ナノ粒子ははっきりとイメージングできています。このように、金ナノ粒子を放射化することで、At-211標識金ナノ粒子の長期的な動態追跡に成功しました。
図3. (a) 放射化金ナノ粒子のX線・ガンマ線エネルギースペクトル。(b) マウスに投与した放射化金ナノ粒子のイメージング結果(投与9分後、4日後)。
図4. (上)At-211標識した放射化金ナノ粒子のX線・ガンマ線エネルギースペクトルと、(下)At-211、放射化金ナノ粒子それぞれのイメージング結果(投与9分後、2日後)。投与2日後には減衰のためAt-211自体はイメージングできないが、キャリアである放射化金ナノ粒子がイメージングできる。
(4)研究の波及効果や社会的影響
本研究では、At-211を放射化金ナノ粒子に標識することで、これまで困難であったAt-211と金ナノ粒子の同時イメージング、そしてAt-211標識金ナノ粒子の長期的な動態追跡に成功しました。同じように、抗がん剤など、これまで体外からイメージングできなかった様々な治療薬を放射化金ナノ粒子に標識することで、体内動態を調べられるようになる可能性があります。
また、金ナノ粒子のイメージングは、治療に最適な金ナノ粒子のサイズや形状を調べるためにも重要です。金ナノ粒子は、血管透過性・滞留性亢進効果(EPR効果)によって腫瘍へ集積するといわれています。EPR効果は2つの側面から成ります。1つ目は、正常な血管と異なり腫瘍付近の血管には隙間が空いているために、血中の金ナノ粒子が腫瘍付近でのみ漏れ出すことです。これによって金ナノ粒子が腫瘍へ運ばれると期待できます。2つ目は、腫瘍付近では異物を排出するリンパ系が未発達であり、金ナノ粒子が滞留しやすいことです。今回、腫瘍に直接投与した金ナノ粒子が4日後も腫瘍に留まっていたのは2つ目の要因によるものと考えています。しかし、これらの効果は金ナノ粒子のサイズ・形状など様々な条件に依存することがわかっています。さらに、金ナノ粒子が肝臓や脾臓(ひぞう)といった臓器に異物とみなされ、捕獲されることが問題視されており、この影響も金ナノ粒子のサイズや形状に依存します。そこで近年、多種多様な金ナノマテリアルが開発され、より腫瘍への集積量が大きく、健康な臓器への集積量が小さい条件を探す研究が活発に行われています。放射化イメージングは金を放射性同位体に変えるというシンプルな手法で、様々なサイズ・形状の金ナノ粒子を同様の方法でイメージングできると考えており、今後幅広い応用が期待できます。
(5)今後の課題
本研究ではAt-211と放射化金ナノ粒子を広帯域X線・ガンマ線撮影装置であるハイブリッド・コンプトンカメラでイメージングしました。ハイブリッド・コンプトンカメラは広帯域であることや、X線やガンマ線の強度が弱くてもイメージングできることが強みですが、分解能には課題があります。マウスとの距離5 cmにおけるハイブリッド・コンプトンカメラの分解能は8 mm程度です。現状でも腫瘍や臓器への集積を大まかに見ることはできるものの、詳細なイメージングには2~3 mmの分解能が必要です。現在、より高分解能の装置を開発中で、より精度のよい放射化金ナノ粒子のイメージングに向けて研究を進めています。
(6)研究者のコメント
本研究では、原子を中性子放射化して可視化する「放射化イメージング」によって、これまで困難だったAt-211(治療薬)と金ナノ粒子(薬剤キャリア)の独立なイメージング、そしてAt-211標識金ナノ粒子の長期動態イメージングに成功しました。これまでイメージングできなかった様々な治療薬が同様の方法でイメージングできると考えており、汎用的な薬物動態のイメージング手法となり得ます。また、金ナノ粒子の放射化イメージングは薬物送達に適したサイズ・形状の金ナノマテリアルを開発するうえでも重要な役割を果たすと考えています。効果的ながん治療の実現に向け、放射化イメージングが幅広い技術の発展に寄与することを期待しています。
[1] Kato et al. 2021, “Intratumoral administration of astatine-211-labeled gold nanoparticle for alpha therapy”, Journal of Nanobiotechnology, 19, 223, DOI: 10.1186/s12951-021-00963-9
[2] 放射化イメージングについては以下を参照
・ Koshikawa et al. 2022, “Proof of concept of activation imaging with hybrid Compton camera”, Applied Physics Letters, 121, 193701, DOI: 10.1063/5.0116570
・ Koshikawa et al. 2023, “Activation imaging: New concept of visualizing drug distribution with wide-band X-ray and gamma-ray imager”, Nuclear Instruments and Methods in Physics Research – section A, 1045, 167599, DOI: 10.1016/j.nima.2022.167599
・ 「様々な元素の分布を可視化する「放射化イメージング」に成功」https://www.waseda.jp/top/news/85249
[3] ハイブリッド・コンプトンカメラについては以下を参照
・ Omata et al. 2020, “Performance demonstration of a hybrid Compton camera with an active pinhole for wide-band X-ray and gamma-ray imaging”, Scientific Reports, 10, 14064
DOI: 10.1038/s41598-020-71019-5
・ 「X線ガンマ線の同時可視化を可能に」https://www.waseda.jp/top/news/69935
[4] 京都大学複合原子力科学研究所の研究用原子炉KUR については以下を参照
https://www.rri.kyoto-u.ac.jp/facilities/kur
特記事項
【論文情報】
雑誌名:Applied Physics Letters
論文名:Activation imaging of gold nanoparticles for versatile drug visualization: an in vivo demonstration
執筆者名:Nanase Koshikawa1、Yuka Kikuchi1、Kazuo S. Tanaka1、Katsuyuki Tokoi2、Akina Mitsukai2, Hiroki Aoto2, Yuichiro Kadonaga3, Atsushi Toyoshima3, Hiroki Kato3, Kazuhiro Ooe3, Koichi Takamiya4, Jun Kataoka1
1.早稲田大学理工学術院 先進理工学研究科 物理学及応用物理学専攻
越川 七星(論文筆頭著者)、菊池 優花、田中 香津生、片岡 淳
2.大阪大学大学院 理学研究科 化学専攻
床井 健運、水飼 秋菜、青戸 宏樹
3.大阪大学 放射線科学基盤機構
角永 悠一郎、豊嶋 厚史、加藤 弘樹、大江 一弘
4.京都大学 複合原子力科学研究所
高宮 幸一
掲載日時(米国東部標準時):2025年3月12日(水)午前10時
掲載日時(日本時間):2025年3月13日(木)午前0時
DOI:10.1063/5.0251048
掲載URL:https://doi.org/10.1063/5.0251048
本研究は、科学技術振興機構(JST)戦略的創造研究推進事業 ERATO「片岡ラインX線ガンマ線イメージングプロジェクト」(2021~2026年度;グラント番号 JPMJER2102)の支援を得て実施したものです。ここに深く感謝申し上げます。
用語説明
- 放射化イメージング
一般に、原子には安定な同位体と、不安定な同位体があります。これらは原子核内部の陽子数(=原子番号)は同じで中性子数が異なるだけのため、化学的性質は変わりません。不安定な原子核は特定の半減期で崩壊し、安定な核種となります。その際に、余ったエネルギーをX線やガンマ線(以下※2を参照)として原子核の外に放出します。このガンマ線を可視化するのが、本研究の「放射化イメージング」です。
- アルファ線、X線、ガンマ線
放射線には様々な種類があります。アルファ線はヘリウムの原子核で、プラスの電荷を2つ持ちます。質量がとても重く、体内で飛ぶ距離が数十マイクロメートルと短い(細胞のサイズと同程度)ことが特長です。そのため、うまく腫瘍に集積させると、腫瘍細胞のみを選択的に殺傷することができます。一方で、X線やガンマ線は電磁波の一種で、電荷を持ちません。どちらも不安定な同位体から出ますが、原子核から出るエネルギーの高い電磁波をガンマ線、また電子軌道から出る比較的エネルギーの低い電磁波をX線として区別します。
- 標識
化合物中で、特定の原子に放射性核種を結合することをいいます。今回の研究では、金ナノ粒子が治療薬を運ぶキャリアであり、ここに治療薬本体であるアスタチン(At-211)を標識しています。
- SPECT(単一光子放射断層撮影)
核医学診断法の1つで、放射性医薬品を体内に投与して、その分布を断層画像として描出します。たとえばTc-99m(テクノチウム)を骨の代謝や反応が盛んなところに集まる性質を持つ物質と化合させ、がんが骨のどの部位にどの程度転移しているかを診断することができます。Tc-99mの可視化には 140 keVのガンマ線が用いられます。他の薬剤でも、SPECT で可視化できるガンマ線はおおむね 300 keV 以下に限られます。
- PET (陽電子放出断層撮影)
こちらも広く行われている核医学診断法で、陽電子を放出する放射性核種で標識された医薬品を体内に投与し、その放射線を検出することで、腫瘍の位置や活性度を画像化する核医学検査です。対消滅するガンマ線を対向する検出器で捉えるため、原理上 511 keV のガンマ線のみを対象としたイメージング法です。
- ハイブリッド・コンプトンカメラ
ハイブリッド・コンプトンカメラは、異なるイメージング技術である「コンプトンカメラ」と「ピンホールカメラ」を1台で実現する新しい技術です。ハイブリッド・コンプトンカメラは散乱体と吸収体の2枚の検出器からなり、それぞれの検出器はシンチレータ(放射線が当たると蛍光を示す物質)と蛍光を読み出すセンサーで構成されます。低いエネルギーのX線は、散乱体を透過することができず、ピンホールを通ってきたものだけが吸収体に届きます。すなわち「散乱体がヒットせず、吸収体のみヒットする」「吸収体のエネルギーが (たとえば)200keV以下」の条件を課せば、ピンホールカメラとして可視化できます。一方で、高いエネルギーのガンマ線は、散乱体を透過して吸収体に届くもの、散乱体でコンプトン散乱して吸収体に届くもの、様々な成分が混ざります。しかしながら、「散乱体と吸収体が同時にヒットする」条件を課せば、通常のコンプトンカメラと同様に可視化することができます。
