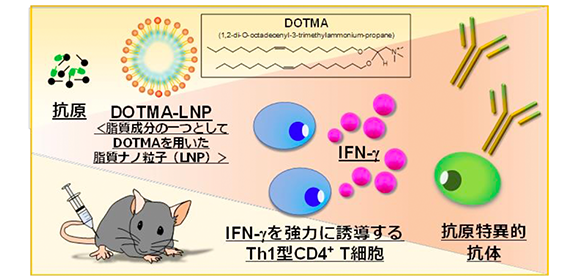
脂質ナノ粒子のワクチンアジュバント としての有用性を実証
感染症に対する新たなワクチン開発に有用な知見
研究成果のポイント
- 脂質ナノ粒子のサブユニットワクチン用アジュバントとしての有用性を評価。様々な組成の脂質ナノ粒子を作製し、組成・物性の違いにより誘導可能な免疫応答が異なることを解明。
- 脂質ナノ粒子の組成を至適化することで、抗原特異的抗体のみならず、Th1型免疫を強力に誘導可能な脂質ナノ粒子を設計可能であることを見出した。また本脂質ナノ粒子が、感染症ワクチン用のアジュバントとして有用であることを明らかにした。
- 本脂質ナノ粒子を活用することで、新たなmRNAワクチンの開発にも繋がることが期待される。
概要
大阪大学大学院薬学研究科の河合惇志さん(博士後期課程大学院生(研究当時))、野田雅寛さん(学部生(研究当時))、吉岡靖雄 特任教授(常勤)(大阪大学先導的学際研究機構/微生物病研究所/薬学研究科/国際医工情報センター/感染症総合教育研究拠点/先端モダリティー・ドラッグデリバリーシステム研究センター、一般財団法人阪大微生物病研究会)らの研究グループは、帝京大学薬学部、大阪大学大学院薬学研究科、大阪大学蛋白質研究所などとの共同研究により、mRNAワクチンにも使用される脂質ナノ粒子のワクチンアジュバントとしての有用性を評価しました。その結果、1)脂質ナノ粒子の組成・物性の違いにより、誘導可能な免疫応答が異なること、2)組成を至適化することで、抗原特異的抗体のみならず、Th1型免疫をも強力に誘導可能なLNPを設計可能であること、3)本LNPは感染症ワクチン用のアジュバントとして有用であることを明らかとしました(図1)。
本研究成果は、感染症に対する安全で有効なワクチンの開発に大きく貢献するだけでなく、新たなmRNAワクチンの開発にも有用な情報を提供すると期待されます。
本研究成果は、米国科学誌「ACS Nano」に2024年6月17日(月)に公開されました。
図1. 脂質成分の一つとしてDOTMAを有する脂質ナノ粒子(LNP)は、抗原蛋白質と混合するだけで、抗原特異的な抗体産生のみならずTh1型免疫を強力に誘導し得ること、さらに、副反応が低いなど、アジュバントとして有用であることを明らかにした。
研究の背景
ワクチンには様々な種類が存在しており、例えば、mRNAワクチン、弱毒生ワクチン、不活化ワクチンや、組換え蛋白質を抗原に用いたサブユニットワクチンなどが存在します。サブユニットワクチンは、迅速に作製可能であること、病原体そのものを使用しないことなどから、古くから使用されてきたワクチンの一つです。サブユニットワクチンにおいては、ワクチン効果を増強するために、免疫賦活化剤(アジュバント)の併用が必須となっています。一方で、抗原特異的T細胞応答を強力に誘導するアジュバントは少ない現状にあり、従来のアジュバントよりも起炎性が低く、強力に抗体産生を誘導しつつ、Th1型免疫などのT細胞応答をも誘導可能なアジュバントの開発が急務となっています。
研究の内容
脂質成分で構成される、粒子径100nm程度の脂質ナノ粒子(LNP)は、簡便に大量生産可能であり、内包した核酸医薬の分解を抑制しつつ目的細胞に送達可能なことから、核酸医薬の送達担体として期待されてきました。さらに昨今、抗原蛋白質のメッセンジャーRNA(mRNA)を内包したLNPによるワクチン(mRNA-LNPワクチン)が、新型コロナウイルスに対するワクチンとして世界中で使用されるなど、LNPの新たな可能性が見出されています。
一方で、LNPが免疫賦活化作用(アジュバント活性)を有することが明らかとなりつつあるものの、LNPのアジュバントへの応用は殆どなされていませんでした。本観点で我々はこれまでに、世界的にも汎用される1,2-dioleoyl-3-trimethylammonium-propane(DOTAP)を正電荷脂質に用いたLNPと蛋白質抗原を混合しワクチンした場合、強力に抗体産生を誘導することを見出してきました(Vaccines (Basel). 2020 Aug 3;8(3):433. )。一方でDOTAP-LNPでは、T細胞応答を効率良く誘導するには至っていませんでした。本研究では、脂質の種類・組成の異なるLNPを用い、抗原特異的抗体産生のみならず、IFN-gを産生するCD4陽性T細胞(Th1型免疫)をも強力に誘導可能なLNPを探索しました。
まず、異なる脂質成分を用いてLNPを作製することで、LNPの表面電荷を変化させましたそれらLNPとインフルエンザ由来抗原を混合し、マウスにワクチンすることで、LNPのアジュバント活性を評価しました。その結果、本抗原を用いた場合においては、DOTAPを用いたLNPなど、正電荷を帯びたLNPは抗原特異的抗体産生に優れるものの、負電荷を帯びたLNPは抗体をほとんど産生しませんでした(図2)。また、いずれのLNPもTh1型免疫の誘導能は低いものでした(図2)。
図2. DOTAP、DPPC、NG-DOPEを用い、表面電荷の異なるLNPを作製した。抗体産生は正電荷LNPでのみ観察された。Th1型免疫は負電荷LNPで観察されたが、誘導能は低いものだった。
そこで、正電荷LNPが抗体産生に優れる点に着目し、異なる正電荷脂質を用いたLNPのアジュバント活性を評価しました。その結果、1,2-di-O-octadecenyl-3-trimethylammonium-propane(DOTMA)を用いたDOTMA-LNPにおいて、抗原特異的抗体のみならず、Th1型免疫が強力に誘導されていました(図3)。なお抗体産生は、一般的に汎用されるアジュバントであるアルミニウム塩と同等に誘導されていました(図4)。さらに、Th1型免疫を誘導することが知られているアジュバントであるCpG核酸と比較しても、DOTMA-LNPはIFN-gを強く産生誘導するなど、非常に強力にTh1型免疫を誘導することが明らかとなりました(図4)。
図3. DOTMA-LNPが抗体産生のみならずTh1型免疫を強力に誘導することが見出された。なお、左から2番目のSVは抗原単独でワクチンしたもの、左から3番目のDOTAP50は“抗体産生に優れると以前に報告した”LNPである。
図4. DOTMA-LNPは既存のアジュバントであるアルミニウム塩やCpG核酸と比較しても、抗体産生は同等であり、Th1型免疫は圧倒的に強力に誘導する。
次に、ワクチン後にインフルエンザウイルスを感染させ、感染防御効果を検証しました。ワクチンに使用した抗原と同じ種類のインフルエンザウイルスを感染させたところ、DOTMA-LNPを含め、他のアジュバントを用いたワクチン群でも、完全に感染を防御することが分かりました(図5左)。一方で、ワクチンに使用した抗原と異なる種類のインフルエンザウイルスを感染させたところ、Th1型免疫を誘導したDOTMA-LNPとCpG核酸のみで感染防御が確認されました(図5右)。さらに、DOTMA-LNPの強力な感染防御には、Th1型免疫のIFN-gが必要であることも明らかとし、Th1型免疫を強力に誘導可能なDOTMA-LNPのアジュバントとしての有用性が見出されました。
図5. ワクチン抗原はH1N1カリフォルニア株由来の抗原を用いた。左はH1N1カリフォルニア株を感染、右はH1N1プエルトリコ株を感染させた後の体重推移を示す。赤のDOTMA-LNPでは、左右どちらも全く体重減少が観察されず、強力に感染防御することがわかる。
そこで、優れた感染防御効果を示したDOTMA-LNPとCpG核酸の副反応を、脾腫や炎症性サイトカイン産生を指標として評価したところ、DOTMA-LNPはCpG核酸と比較して、起炎性に起因する副反応が低いことが示され、DOTMA-LNPは優れたアジュバントになり得るものと考えられました。
次に、DOTMA-LNPのアジュバントとしての汎用性を評価しました。新型コロナウイルス由来スパイク蛋白質、肺炎球菌由来PspA蛋白質の組換え蛋白質を抗原として用いたところ、いずれの抗原においても、DOTMA-LNP群で抗体産生のみならずTh1型免疫を強力に誘導することが判明しました(図6)。そのため、DOTMA-LNPは汎用性に優れ、様々な抗原において適用できる可能性が示されました。
図6. PspAの結果を示した。DOTMA-LNPはアルミニウム塩やCpG核酸と比較しても、抗体産生は同等であり、Th1型免疫は強力に誘導するなど、汎用性が示された。
これまでに、正電荷を帯びた脂質がTLR4やNLRP3を活性化するという報告がなされていました。そこで、DOTMA-LNPのアジュバント活性のメカニズムを評価するため、TLR4およびNLRP3のノックアウトマウスを用いてワクチン効果を検証しました。その結果、いずれのノックアウトマウスにおいても、野生型マウスと比較して、抗体産生およびTh1型免疫に変化は観察されませんでした。そのためDOTMA-LNPが、なぜこれほどまでに強力なTh1型免疫を誘導するかは、今後の検討課題として残されています。
以上、本研究では、DOTMAを正電荷脂質に用い、適切な組成で作製したDOTMA-LNPにおいて、既存のアジュバントと比較して起炎性が低く、抗原特異的抗体産生のみならずTh1型免疫をも強力に誘導し得ることを先駆けて見出しました。
本研究成果が社会に与える影響(本研究成果の意義)
本研究では、LNPのアジュバントとしての有用性を実証すると共に、従来までのアジュバントと比較した優位性も見出しました。即ち本研究成果は、感染症に対する安全で有効なサブユニットワクチンの開発に大きく貢献すると期待されます。また、本研究で見出したLNPは、mRNAワクチンへそのまま活用することはできませんが、mRNAワクチン用に改良することで、新たなmRNAワクチンの開発にも有用な情報を提供すると期待されます。
特記事項
本研究成果は、2024年6月17日(月)に米国科学誌「ACS Nano」(オンライン)に掲載されました。
タイトル:“Lipid Nanoparticle with 1,2-Di-O-octadecenyl-3-trimethylammonium-propane as a Component Lipid Confers Potent Responses of Th1 Cells and Antibody against Vaccine Antigen”
著者名:Atsushi Kawai, Masahiro Noda, Haruki Hirata, Lisa Munakata, Teppei Matsuda, Daiki Omata, Naoki Takemura, Sakura Onoe, Mika Hirose, Takayuki Kato, Tatsuya Saitoh, Toshiro Hirai, Ryo Suzuki, Yasuo Yoshioka
DOI:10.1021/acsnano.4c00278
(https://pubs.acs.org/doi/10.1021/acsnano.4c00278)
なお本研究は、日本学術振興会(JSPS)科学研究費補助金、日本医療研究開発機構(AMED)、大阪大学感染症総合教育研究拠点 (CiDER)、CAMaD「ワクチン開発のための世界トップレベル研究開発拠点の形成事業」などの研究支援を受け、帝京大学薬学部、大阪大学薬学研究科、大阪大学蛋白質研究所、一般財団法人阪大微生物病研究会の協力を得て行われました。
参考URL
用語説明
- 脂質ナノ粒子
脂質成分で構成される粒子径100nm程度のナノ粒子であり、英語名Lipid NanoParticleからLNPとも呼ばれる。核酸医薬の送達担体や、mRNAワクチンに使用されている。
- アジュバント
樹状細胞などの免疫細胞を活性化する物質。抗原蛋白質と共にワクチンすることで、免疫応答を増強可能となる。水酸化アルミニウムなどのアルミニウム塩が汎用されており、海外ではToll様受容体9のアゴニストであるCpG核酸も使用されている。
- Th1型免疫
抗原に反応して、IFN-を産生するCD4陽性T細胞を主とした免疫応答。IFN-が多くの免疫細胞を刺激することで、感染防御にも寄与する。
- サブユニットワクチン
病原体全体ではなく、その一部分(サブユニット)を使用して作られるワクチン。通常、病原体の特定のタンパク質や糖類など、免疫系が識別しやすい部分で構成される。
