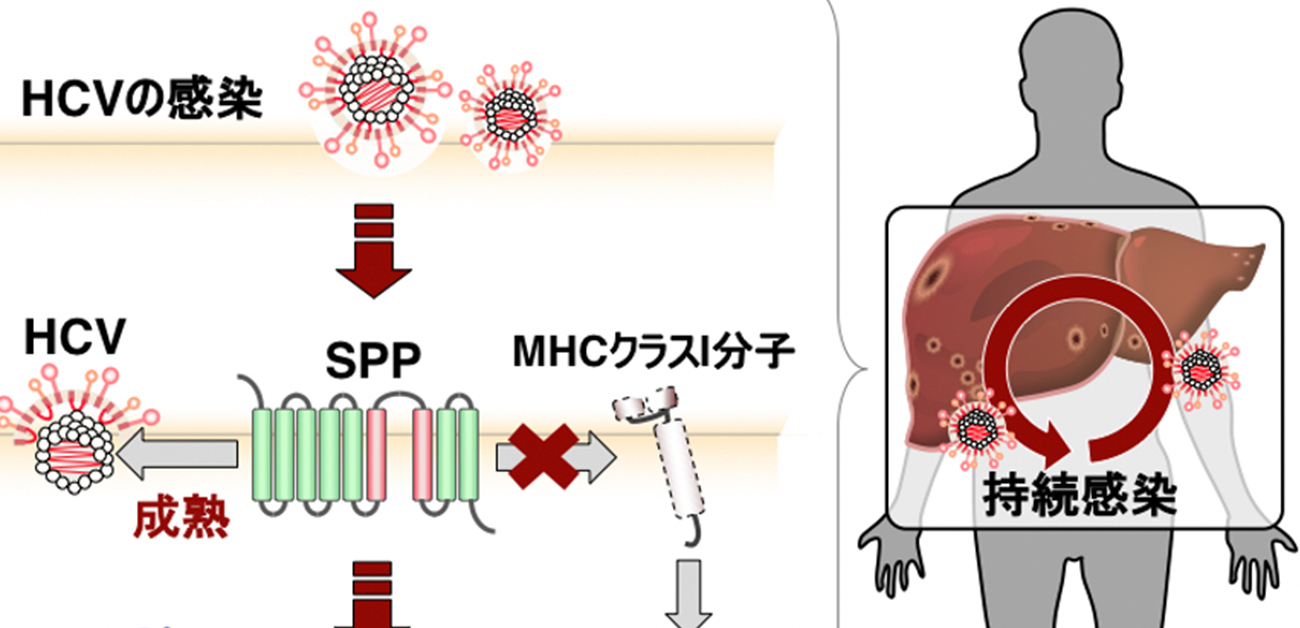
持続感染するウイルスが免疫を回避する新たなメカニズムを解明!
研究成果のポイント
- C型肝炎ウイルス(HCV)がウイルス増殖に利用する因子のシグナルペプチドペプチダーゼ(SPP)に、免疫関連タンパク質のMHCクラスI分子を成熟させる機能があることを発見しました。
- HCVが増殖する際にSPPを利用することで、MHCクラスI分子の成熟が阻害されることが分かりました。このメカニズムが、HCVが持続感染する際に免疫を回避するのに役立っていると考えられます。
- HCVだけでなく、同じく持続感染を起こすヒトサイトメガロウイルス(HCMV)もSPPを免疫回避に役立てていることが本研究により明らかになりました。このため、様々なウイルスの持続感染にSPPが関与している可能性があります。
概要
大阪大学大学院医学系研究科の大学院生の平野順紀さん(研究当時博士課程、現国立感染症研究所研究員)、感染症総合教育研究拠点(微生物病研究所兼任)松浦善治特任教授(常勤)、高等共創研究院(微生物病研究所兼任)岡本徹教授らの研究グループは、C型肝炎ウイルス(HCV)が、シグナルペプチドペプチダーゼ(SPP)と呼ばれる因子を利用してウイルス増殖を行うことが、ウイルスによる免疫回避や持続感染に役立っていることを明らかにしました。
MHCクラスI分子は、ウイルス由来の異物を細胞表面で免疫細胞に提示する役割を持っていることが知られています。岡本教授らの研究グループは、MHCクラスI分子が成熟し、機能するには、SPPが必要であることを発見しました。また、HCVの感染時には、ウイルスの増殖にSPPが利用されるため、MHCクラスI分子の成熟が十分に行えなくなること、その結果生じた未成熟なMHCクラスI分子が分解されてしまうため、MHCクラスI分子の発現が抑制されることも分かりました。MHCクラスI分子の発現が低下した細胞を免疫細胞と共に培養した場合には、免疫細胞によるMHCクラスI分子の認識が起こりにくくなるため、免疫細胞の活性化が抑制されました。このため、HCVが免疫細胞の監視を逃れて肝細胞で持続感染する際にSPPが役立っていることが示唆されました(図1)。本研究グループはさらに、HCVと同じく持続感染するヒトサイトメガロウイルス(HCMV)においても、ウイルスによるMHCクラスI分子の発現抑制にSPPが役立っていることを明らかにしました。この成果により、HCVやHCMVといった進化的に関連性の無いウイルスが共通して持続感染にSPPを介した経路を利用していることから、SPPが様々なウイルスの持続感染に共通して関与している可能性が示唆されました。
本研究成果は、米国科学誌「米国科学アカデミー紀要(PNAS)」に、5月25日(火)午前4時(日本時間)に公開されました。
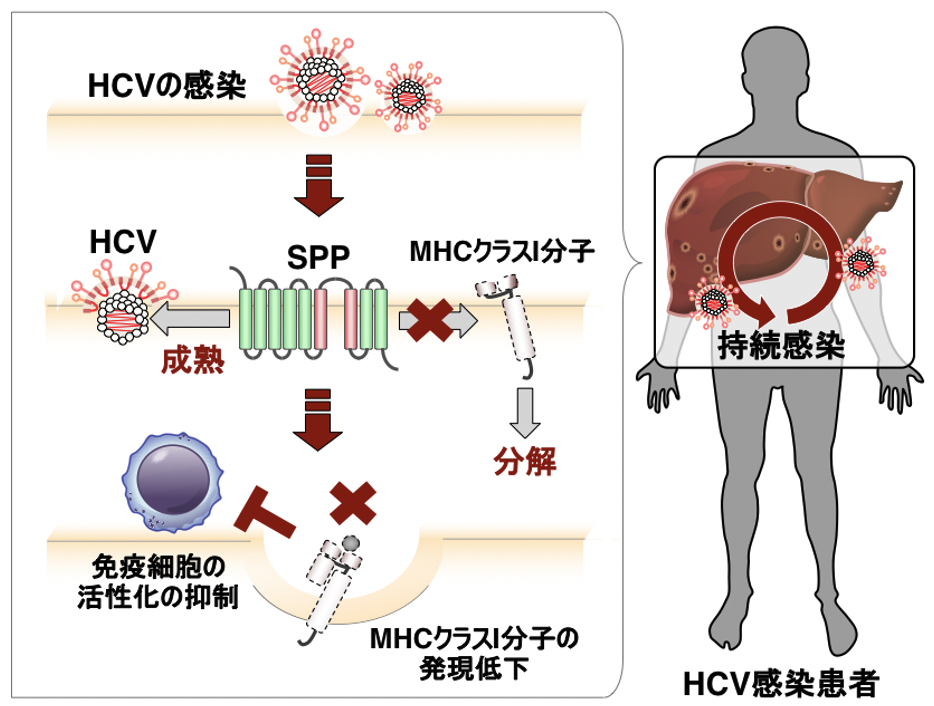
図1. HCVは肝細胞に侵入後、自己の増殖を行います。この過程で、HCVはSPPを利用し、MHCクラスI分子の分解を誘導します。このため、MHCクラスI分子の発現が抑制され、免疫細胞の活性化が抑制されます。このメカニズムが、HCVの持続的な感染に役立っていることが示唆されました。
研究の背景と成果
C型肝炎ウイルス(HCV)は肝臓に持続感染し、脂肪肝、慢性肝炎、肝線維化、肝硬変、肝癌といった慢性肝疾患の主要な原因となるウイルスです。これまでに岡本徹教授の研究グループは、松浦善治特任教授(常勤)らの研究グループとともに、HCV粒子を構成するウイルスタンパク質のコアタンパク質(HCV Core)が、細胞内の小胞体に局在する宿主のプロテアーゼであるシグナルペプチドペプチダーゼ(SPP)により切断されることが、HCVの粒子形成や病原性に重要であることを明らかにしてきました。
今回、本研究グループは、SPPが本来細胞内で担っている役割に着目し、SPPが免疫関連因子のMHCクラスIの成熟にも重要な働きを有していることを発見しました。MHCクラスI分子は成熟過程でSPPによって切断を受けること、SPPの切断活性を抑制した場合には、MHCクラスI分子が未成熟なまま分解されることが分かりました。また、HCV感染時にはHCV CoreがSPPと優先的に結合して切断を受けることにより、MHCクラスI分子のSPPによる切断および成熟が妨げられること、その結果、未成熟なMHCクラスI分子がHRD1と呼ばれる細胞内の因子を介して分解され、発現が低下することが分かりました (図2)。さらに、HCV Coreを肝臓で発現するコア発現マウスや、HCV感染患者の肝臓では、MHCクラスI分子の発現が低下していることも明らかになりました。MHCクラスI分子の発現が低下している、HCV Coreを発現した細胞やモデルマウスの肝細胞を、ウイルス排除に重要な役割を持っている免疫細胞のCD8+T細胞と共培養した場合には、CD8+T細胞の活性化が起こりにくいことも分かりました(図3)。これは、CD8+T細胞によるMHCクラスI分子の認識が起こりにくくなったためと考えられます。HCVは高率に持続感染することが知られていましたが、その分子機序はこれまで分かっていませんでした。本研究により、HCV Coreが持続感染に必要な機能を担っていることが初めて明らかになりました。
HCV以外で持続感染するウイルスの1つに、ヒトサイトメガロウイルス(HCMV)が挙げられます。本研究では、HCMVのウイルスタンパク質のUS2タンパク質 (HCMV US2)もSPPと相互作用し、MHCクラスI分子の分解を促進する機能を持つという、HCMV US2の作用機序が明らかになりました。HCV CoreとHCMV US2では、SPPと相互作用することが予想される領域の構造の一部が類似していることも分かりました(図4)。
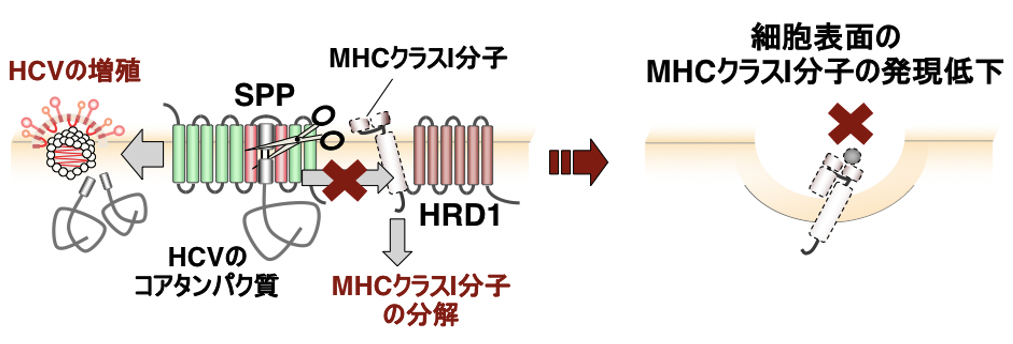
図2. HCVのコアタンパク質により、MHCクラスI分子のHRD1を介した分解が誘導されます。この結果、MHCクラスI分子の発現低下が起こります。
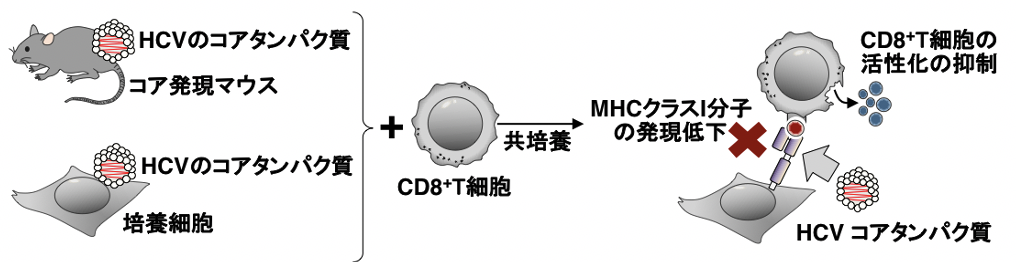
図3. HCVのコアタンパク質を発現するマウスの細胞や培養細胞を、免疫細胞のCD8+T細胞と共培養した場合、コアタンパク質によるMHCクラスI分子の発現低下に伴い、CD8+T細胞の活性化は起こりにくくなります。
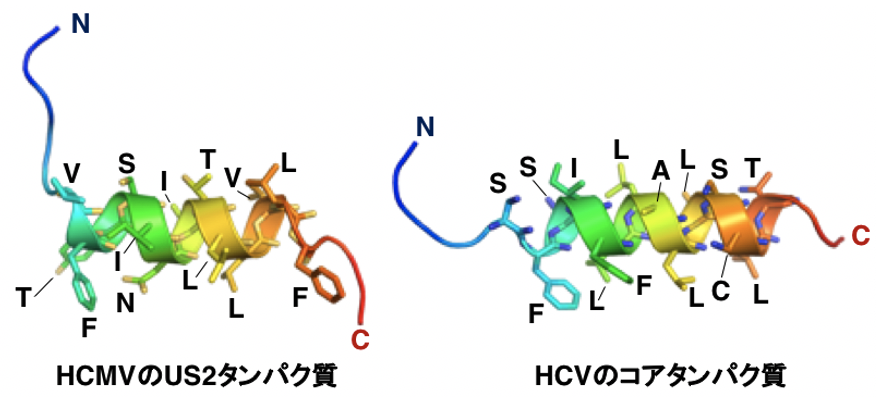
図4. HCMVのUS2タンパク質とHCVのコアタンパク質では、SPPと相互作用すると考えられる領域の構造が一部類似していることが予想されました。
本研究成果が社会に与える影響(本研究成果の意義)
HCVとHCMVの間には進化的な関連性がないため、これらのウイルスはそれぞれ独自に、SPPを免疫回避に役立てていることが示唆されました。持続感染するウイルスの免疫回避に役立っている共通の因子や免疫回避の分子機序の詳細を明らかにすることが出来ました (図5)。
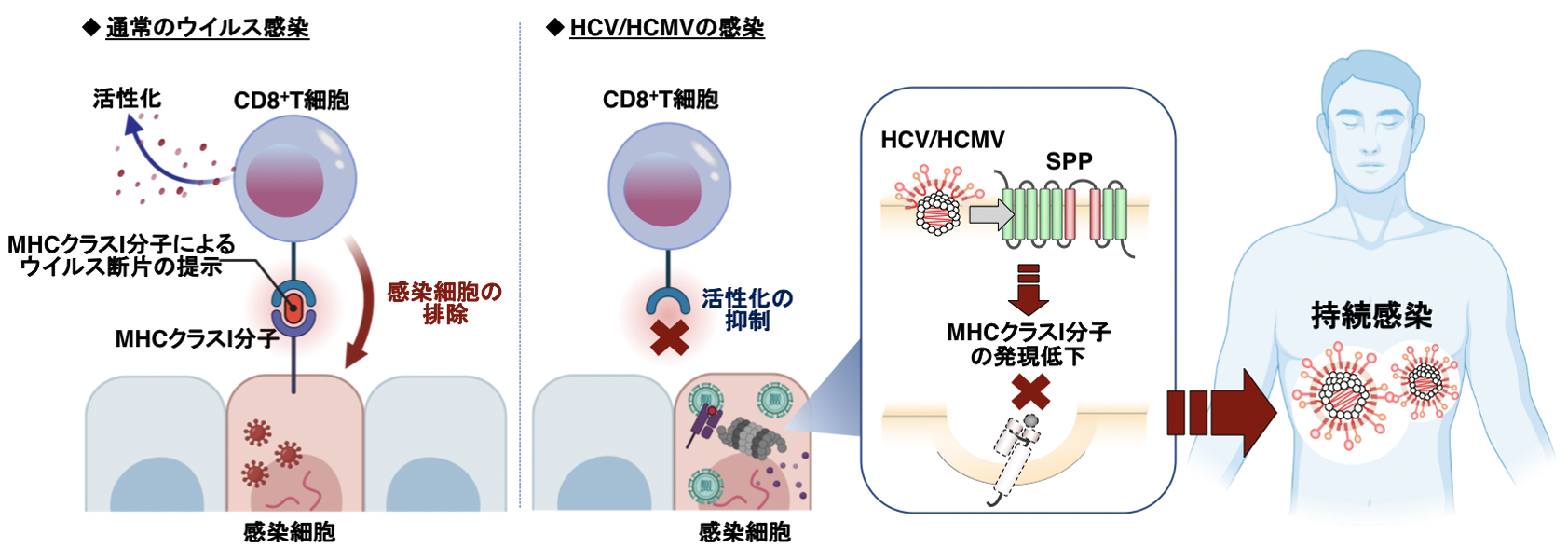
図5. 本研究成果の概略図。ウイルス感染時には通常、CD8+T細胞がMHCクラスI分子にロードされたウイルス由来の異物を認識することで、ウイルス感染細胞の除去が行われます。しかし、HCVやHCMVの感染下では、ウイルスがSPPを利用することでMHCクラスI分子の発現が低下し、ウイルス感染細胞はCD8+T細胞の監視を回避することが出来ます。このメカニズムが、HCVやHCMVの持続感染に役立っていることを明らかにしました。
特記事項
本研究成果は、2021年5月25日(火)午前4時(日本時間)に米国科学誌「米国科学アカデミー紀要(PNAS)」(オンライン)に掲載されました。
タイトル:“Hepatitis C virus modulates signal peptide peptidase to alter host protein processing”
著者名:Junki Hirano, Sachiyo Yoshio, Yusuke Sakai, Li Songling, Tatsuya Suzuki, Yumi Itoh, He Zhang, David Virya Chen, Saori Haga, Hiroko Oomori, Takahiro Kodama, Yusuke Maeda, Yoshihiro Ono, Yu Takahashi, Daron M. Standley, Masahiro Yamamoto, Kohji Moriishi, Kyoji Moriya, Tatsuya Kanto, Tetsuo Takehara, Kazuhiko Koike, Yoshiharu Matsuura and Toru Okamoto
なお、本研究は、科学研究費補助金、日本医療研究開発機構 肝炎等克服緊急対策研究事業、新興・再興感染症研究基盤創生事業、新学術領域研究「ネオウイルス学」(研究総括 河岡義裕)の研究支援を受けて実施されました。
参考URL
大阪大学微生物病研究所高等共創研究院岡本研究室
http://www.biken.osaka-u.ac.jp/laboratories/detail/51
用語説明
- C型肝炎ウイルス(HCV)
HCVは世界に2億人、日本に170万人の感染者がいるとされており、血液や血液製剤を介して感染します。HCVは感染後、高率に慢性化し、脂肪肝、慢性肝炎、肝線維化、肝硬変や肝癌を引き起こすことが知られています。近年開発された治療薬によって日本国内での感染者は減少傾向にありますが、ウイルスが長期間持続感染した肝臓では、ウイルスの排除後も病態が進行することが問題になっています。
- シグナルペプチドペプチダーゼ(SPP)
細胞内小器官の小胞体に局在するタンパク質で、基質となる様々なタンパク質を切断する機能を持っていることが知られています。HCVのコアタンパク質を含むウイルスタンパク質が基質として報告されている一方、宿主のタンパク質の切断にも関与することが知られていますが、SPPによる宿主タンパク質の切断の生物学的な意義はよく分かっていません。
- MHCクラスI分子
ウイルスタンパク質由来の断片などの異物をロードし、細胞表面でこれらの異物をCD8陽性T細胞などの免疫細胞に提示する役割を持っています。CD8陽性T細胞は異物の乗ったMHCクラスI分子を認識して感染細胞を排除します。
- ヒトサイトメガロウイルス(HCMV)
HCMVは通常、幼小児期に不顕性感染することが知られており、免疫抑制状態で再活性化してCMV感染症と呼ばれる種々の病態を引き起こします。また、免疫が正常な場合にも、HCMVにより肝炎や伝染性単核球症などの疾患を発症する場合があります。
