タンパク質合成反応を解析する大規模全成分計算機シミュレーターを開発
241分子種をスピード処理。有用タンパク質生産に応用も
本研究成果のポイント
・その複雑性ゆえ困難であったタンパク質合成反応 の大規模全成分計算機シミュレーター を世界で初めて 開発。241分子種が示す濃度変化の観測に成功し、実験結果と整合性のあるシミュレーション結果を生成した。
・研究グループは、大規模データの中から、擬定常状態 (quasi-stationary state:QSS)に着目する解析手法 を開発。QSS成分が構成するネットワークが時間経過に伴い離合集散を繰り返す、タンパク質合成反応の新しい特徴を解明した。
・開発したシミュレーターとデータ解析手法は、細胞内反応の大規模時系列データの解析や再構成型無細胞翻 訳系 を用いた有用タンパク質生産量の向上など、応用面でもその活用が期待される。
リリース概要
大阪大学大学院工学研究科の松浦友亮准教授と理化学研究所生命システム研究センターの清水義宏ユニットリーダーらの研究グループは、その複雑性ゆえ困難であった最少成分からなるタンパク質合成反応の大規模全成分計 算機シミュレーターを世界で初めて開発し、実験結果と整合性のあるシミュレーション結果の生成に成功しました (図1) 。同研究グループは、シミュレーションで得られた大規模データの擬定常状態(quasi-stationary state:QSS)に着目した新しい解析手法を開発。QSS成分で構成されるネットワークが時間経過に伴って離合集散を繰り返す、タンパク質合成反応の新しい特徴が明らかになりました。ネットワークが離合集散する性質は、細胞内の多くの反応でも起こっていると推測されます。今回新たに開発したシミュレーターおよびデータ解析手法は、細胞内反応の大規模時系列データの解析や再構成型無細胞翻訳系を用いた有用タンパク質生産量の向上など、応用面でもその活用が期待されます。
本研究成果は、米国科学誌『米国科学アカデミー紀要(Proceedings of the National Academy of Sciences)』 (オンライン)に、2月7日(火)午前5時(日本時間)に公開されました。
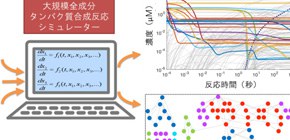
図1 タンパク質合成反応の大規模全成分計算機シミュレーターを世界で初めて開発
研究の背景
タンパク質は生命活動をつかさどる重要な分子の一つです。細胞内において、タンパク質はアミノ酸 が連結して合成されますが、その反応は何千もの分子種 による何万もの化学反応ステップを経ています。タンパク質合成反応のような複雑な反応がどのような振る舞いを見せるかを理解し、さらに反応結果を予測することは、生命システムの動作 原理の解明だけでなく、生命システムの産業利用にも重要です。
タンパク質合成反応の数理モデルを開発し、計算機でシミュレーションを行う手法は、これまでに世界で複数のグループが、その複雑な事象を理解・予測するために用いてきました。しかし、従来のシミュレーションはタンパク質合成反 応の分子種・反応数の多さのため、これを簡単化(粗視化)した数理モデルでしか行われていません。ゆえに、反応に関わっている全成分の様子をつぶさに観測することができず、反応内部で起こっている現象を詳細に捕らえることが困難でした。
研究の内容
松浦友亮准教授らの研究グループでは、最少成分からなるタンパク質合成反応で、全分子種の様子を観測可能とする数理モデルを世界で初めて開発しました。理化学研究所生命システム研究センターの清水ユニットリーダーらは、以前に大腸菌由来のタンパク質合成反応に最小限必要な成分(最少成分)を実験で明らかにしています(Nat. Biotechnol.19,751-755,2001)。今回、同研究グループは、これら最少成分を出発物質として、3アミノ酸からなるタンパク質を合成する数理モデルを開発しました。常微分方程式 からなるこの数理モデルは、241分子種、968反応からなる大規模タンパク質合成反応シミュレーターです。同グループの一人、みずほ情報総研の谷村直樹シニアコンサルタントらが構築法を工夫したことで、容易かつ短時間(30秒程度)で大規模モデルが構築できるようになりました。 これにより世界で初めて、最少成分からなるタンパク質合成反応で全成分濃度の時間変化を観測することが可能となりました (図2) 。
同グループは、さらにこの数理モデルを用いてタンパク質合成反応のシミュレーションを行い、結果を詳しく検証し、実際の実験結果との整合性からシミュレーターの信頼性を示しました。大規模シミュレーションの一般的な問題点として、膨大なデータが生成され、そこから意味のある情報を取り出すのが難しくなる一面があります。しかし、同研究グループでは、成分濃度がほとんど変化しない擬定常状態(quasi-stationary state: QSS)に着目する解析手法を開発し、タンパク質合成反応の新しい特徴を発見しています。具体的には、QSS成分が構成するネットワークが時間経過に伴い離合集散を繰り返すことを初めて明らかにしました (図3) 。離合集散する性質は、細胞内の多くの反応でも起こっていると推測されます。
図2 タンパク質合成反応シミュレーションの結果例。全241成分の濃度変化が観測できる。
図3 QSS成分が構成するネットワークが離合集散する様子。○はQSS成分を、線はつながりを示す。
本研究成果が社会に与える影響(本研究成果の意義)
今回新たに開発したタンパク質合成反応シミュレーターおよびQSSに着目したデータ解析手法は、細胞内反応の大規模時系列データの解析に利用可能です。これにより、細胞内反応が共通して持つ普遍的な性質を明らかにでき るなど今後の進展が期待されます。応用面でも、シミュレーターを活用する事で再構成型無細胞翻訳系を用いた有用タンパク質生産量の向上などが期待されます。
特記事項
本研究成果は、2017年2月7日(火)午前5時(日本時間)に米国科学誌『米国科学アカデミー紀要(Proceedings of the National Academy of Sciences)』(オンライン)に掲載されました。
タイトル:“Reaction dynamics analysis of a reconstituted Escherichia coli protein translation system by computational modeling”
著者名:Tomoaki Matsuura*, Naoki Tanimura, Kazufumi Hosoda, Tetsuya Yomo and Yoshihiro Shimizu* (*責任著者)
なお、本研究は、科学技術振興機構ERATOプロジェクト、文部科学省科学研究費助成事業・新学術領域研究「動的秩序と機能」などの支援を受けて行われました。また、みずほ情報総研株式会社サイエンスソリューション部バイオ・ ナノチームの協力のもと行われました。
研究者のコメント
実験と理論科学の融合の重要性が言われているが、研究者間の価値観が大きく異なるため困難である場合が多い。本研究は実験科学と計算科学を専門とする研究者が共同で実施した研究である。ただし、計算科学を専門とす る研究者は共著者のなかで1名だけであった。従って、実験科学を専門とする研究者が主導し、その価値観で進めた全く新しい形の理論研究になった。結果的に、本研究は未開拓の研究領域を確立できたと考えている。最後に、昨今ビッグデータの解析が話題になっているが、本研究で開発した解析手法はタンパク質合成反応だけでなく、さまざまな複雑なシステムの時系列を可視化する上で、全く新しい見方を提供できる可能性がある。
参考URL
工学研究科生命先端工学専攻(渡邉研究室)
http://www.bio.eng.osaka-u.ac.jp/ez/index.html
用語説明
- タンパク質合成反応
タンパク質は細胞内の化学反応の触媒、細胞の形態形成などをつかさどる重要な分子である。タンパク質は20種類 のアミノ酸を直鎖状に連結することでできあがる。細胞内では、この連結反応(タンパク質合成反応)は何千もの分子種と何万もの化学反応ステップから構成されている。
- 計算機シミュレーター
計算機シミュレーション:
複雑な現象について、その現象を支配する法則(数式など)を計算機に入力し、計算機上でその現象を模擬すること。スーパーコンピュータ「京」で地震や気候をシミュレーションする例が有名。
- 分子種
異なる種類の分子。例えば、アミノ酸には20種類あるので20の分子種がある。
- 擬定常状態(quasi-stationary state:QSS)
段階的に進行する化学反応があるとき、反応内の一つの物質の生成と喪失が同時に起こっており、そのバランスにより物質濃度がおおよそ一定している状態。
- 再構成型無細胞翻訳系
細胞を使うことなくタンパク質を試験管内で合成する無細胞翻訳系の一種。大腸菌の翻訳反応の必須成分 69 成分 を単離精製し、これを試験管内で再構成することでタンパク質合成反応が行えるシステム(Shimizu et al., Nat Biotechnol, 2001)。
- アミノ酸
細胞には20種類のアミノ酸が存在し、これらが直鎖状に連結することでタンパク質ができあがる。また、アミノ酸はそれ自体も細胞や生物の生存に必須な栄養素でもある。
- 常微分方程式
微分方程式の一種で自然現象を数式で表現するときによく使われる。
