「再生誘導」とは?皮膚の難病研究から明らかになった 「再生」のメカニズム
医学系研究科・寄附講座教授・玉井 克人
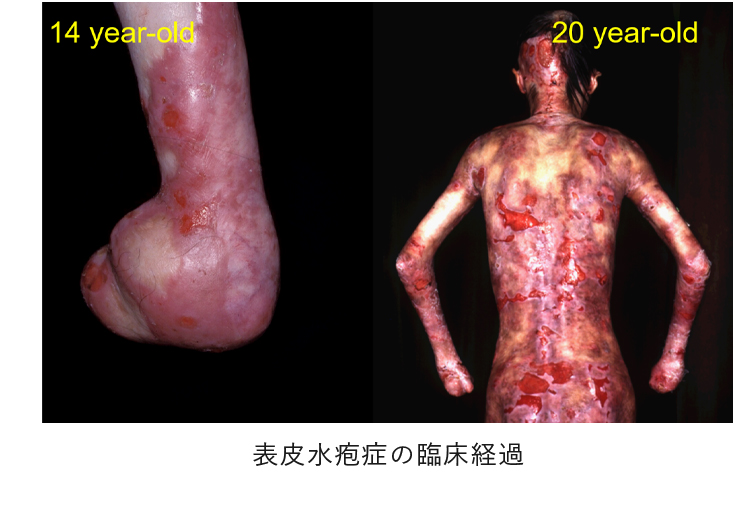
生まれつき皮膚がはがれやすく、やけどを負ったような水ぶくれや、ただれが全身に広がる「表皮水疱症」という遺伝性の難病がある。赤ん坊のころから繰り返し皮膚がはがれ、手足の指が癒着してしまうなどのつらい病気だが、有効な治療法はない。大阪大学医学系研究科の玉井克人寄附講座教授(再生誘導医学寄附講座。以降、玉井教授)は、弘前大学の皮膚科の研修医だったころ、表皮水疱症の少年と出会い、自ら治療法を開発することを決意する。難病の少年と心優しい研究者が約束を交わしてから18年。その約束は、ヒトがもつ「再生」の力を引き出す、極めて大きな可能性を秘めた「再生誘導医薬」として結実の日を迎えつつある。

「治るでしょうか?僕の病気」
ヒトの皮膚の断面を顕微鏡で見ると、一番表面に表皮があり、その下に真皮がある(図)。さらにその間に基底膜という薄い層がある。玉井教授は「掛け布団と敷布団の間に敷かれたシーツのような存在が基底膜」と説明する。私たちがけがをして皮膚を傷つけても、しばらく清潔にしておくと自然に修復され、もとに戻る。それは基底膜に表皮幹細胞という特殊な細胞があり、それが皮膚のもとになる細胞を次々と供給してくれるからだ。
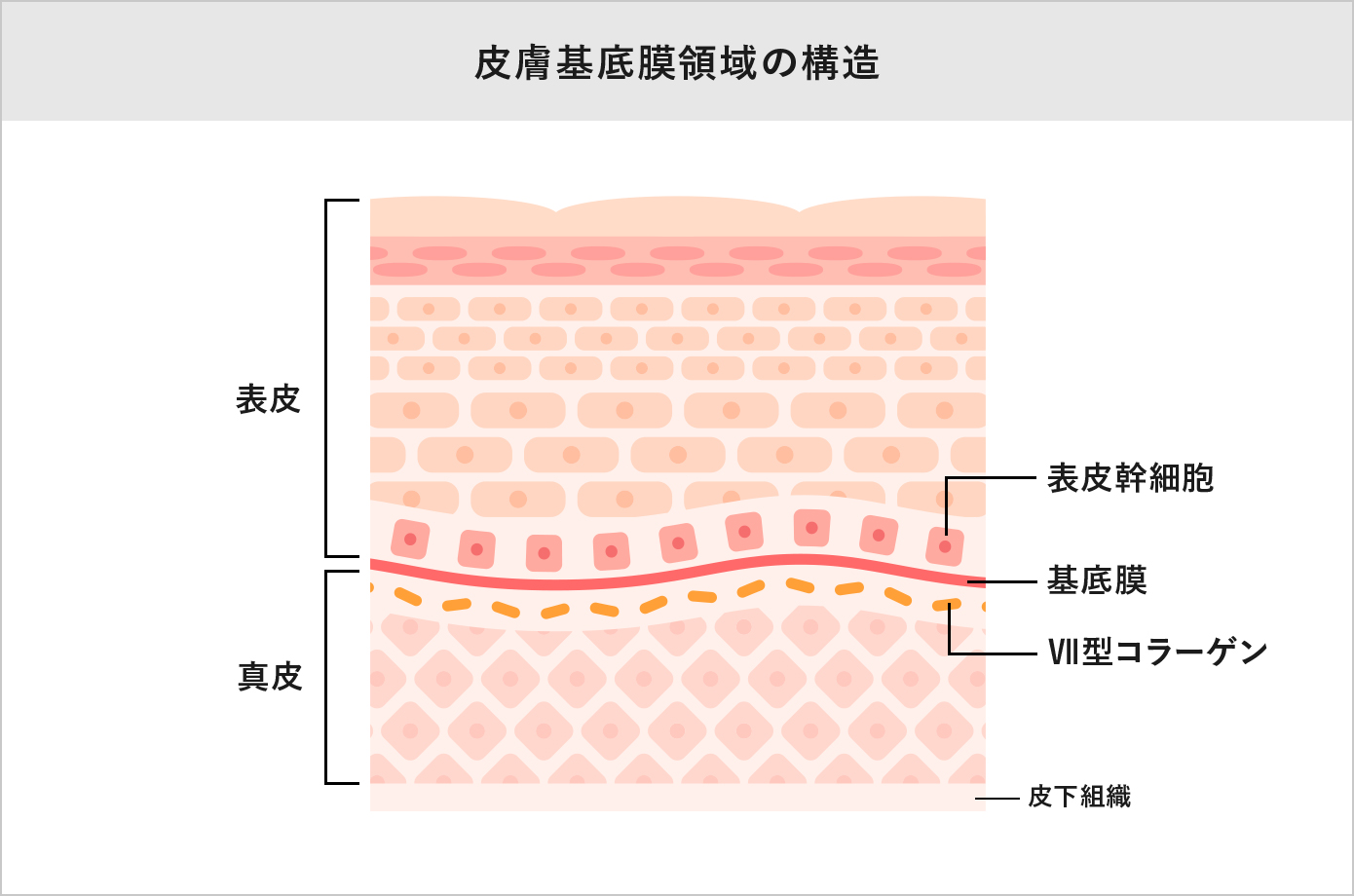
ところが表皮水疱症の患者は、真皮と基底膜を接着する糊の役割を果たす7型コラーゲンというタンパク質を遺伝的につくることができない。このため少しの刺激で表皮が基底膜ごとはがれてしまうばかりか、幹細胞も失うので、はがれた表皮を再生することが難しい。やけどの治療のように皮膚を移植したとしても、糊の成分がないので生着することはない。消毒して軟膏を塗り、ガーゼを巻くような対処療法しか取れないでいた。
玉井教授は弘前大学医学部での研修医時代、中学生だった表皮水疱症の少年に出会った。つらい症状にもかかわらず周りの人たちを気遣い、明るく振る舞う少年とすっかり仲良くなった。「彼ほど素晴らしい人格者に会ったことがない。年齢は離れているが、尊敬すべき親友」と話す玉井教授は、あるときこの少年に「治るでしょうか?僕の病気」と聞かれ言葉につまった。咄嗟に「今の医学の進歩は速い。あと10年も待てば良い治療法ができるだろう。それまで一緒に頑張ろう」と約束した。だが10年たっても有効な治療法は一向に現れない。このままでは約束を果たせない。「この病気は遺伝子の異常によるものだから、遺伝子治療でしか根治させることはできない」。この時玉井教授は40歳を過ぎ、すでに弘前大助教授だったが、遺伝子を学び直すことを決意し、「研究生でいいので置いてほしい」と、厚生労働省の研究班で知り合った金田安史・大阪大学教授(遺伝子治療学)の門をたたいた。2003年には阪大助教授となって、表皮水疱症の根治を目指す研究に取り組んだ。
辿り着いた「再生誘導」のメカニズム
表皮水疱症の診療を続けるなかで不思議に思ったことがあった。それは体表のほとんどの表皮を失った後でも、きわめてゆっくりだが表皮が再生していくことだ。表皮幹細胞がある基底膜ごとはがれているので、普通に考えれば表皮は全く再生できないはずである。玉井教授は「私たちの体には、どこかで大量の幹細胞が失われた場合、そこから何らかのSOSシグナルが発信され、別の組織から幹細胞を補充する仕組みがあるのではないか」という仮説を立てた。仮説が正しければ、その幹細胞に7型コラーゲンをつくる遺伝子を入れてやれば、表皮水疱症は根治できるはずだ。
さらに「SOSシグナルが伝達されるとすれば血液を介してだろう。それならば末梢の組織や他の臓器に幹細胞を補充するセンターとなるのは、白血球や赤血球などを造る骨髄細胞に違いない」と予想した。
証明のため、表皮水疱症の親友の彼に協力を仰いだ。採取させてもらった20ccの血液を玉井教授は少年からの「贈り物」と評する。自分の血液と、少年の血液をシャーレで培養。2週間後、少年の血液には、自分の血液には見られない血液細胞のコロニーが多数みつかった。コロニーの発見が示唆するもの、それは極めて高い自己複製能力を持つ「幹細胞」の存在だった。
この幹細胞をゲノムレベルで解析すると、骨髄の中にいて、表皮幹細胞と同じ外胚葉由来の間葉系幹細胞であることが確認された。「外胚葉由来」であるということは、この間葉系幹細胞は骨や軟骨だけでなく、中枢神経にも表皮にもなれるということ。それが骨髄にプールされていることが明らかになった。
さらに研究を進めると、表皮が大量にはがれると、壊死した細胞の核から「HMGB1」と呼ばれる核タンパクが血管内に放出され、それがSOSシグナルとなって骨髄内の間葉系幹細胞を血液中に導きだすことが分かった。「壊死」によって「HMGB1」が血中に増えることがキーだったのだ。血管内を遊走する幹細胞は、損傷した細胞が分泌するSDFー1αという物質を目印にして集積する。傷ついた組織が、骨髄の間葉系幹細胞の助けを借りて、機能の再生を誘導するメカニズムが明らかになった瞬間だった。
阪大発創薬ベンチャー「ステムリム」を設立
メカニズムが明らかになったことで、治療への二つの道筋が見えた。一つ目はSOSシグナル物質・HMGB1により血液中におびき出した間葉系幹細胞に、7型コラーゲンを造る正常な遺伝子を組み込み、もとに戻してやること。正常化した幹細胞が皮膚に定着すれば根治が期待できる。二つ目はシグナル物質の投与で、より多くの幹細胞を血液中に動員してやること。患者の幹細胞には7型コラーゲンを造る遺伝子がないので、残念ながら根治はしないが、症状はぐっと改善する。「傷が悪化するスピードより、治るスピードを早めてやればQOL(生活の質)は良くなる」という発想だ。一つ目の方法は動物実験の段階だが、二つ目はいくつもの壁を越えて、2018年1月に表皮水疱症患者を対象にした臨床研究へと至り、2020年1月、良好な結果が報告された。
再生誘導医薬への関係者の関心は高く、「今までにない薬ができる」と創薬を強く勧める声もあった。だが医学研究者だけでは特許取得や製薬会社との提携などは手に負えない。幸い創薬経験の豊富なエキスパートの協力が得られることになり、2006年、阪大発の創薬ベンチャー企業を設立した。現在の会社名「ステムリム」は「幹細胞(Stem cell)」と「再生誘導医療(Regeneration-Inducing Medicine)」に由来する。
当初は資金が足りず、何度も行き詰まりそうになった。だが大手製薬会社との提携が実現し、経営は安定し、研究員を雇用し続けることができた。基礎研究をもとにベンチャーがうまれ、研究が進み、成果が社会実装され、新たな課題が見つかり、また研究が進むというサイクルは、研究室単位での小さな研究開発エコシステムだと玉井教授はいう。
「HMGB1」秘めたる可能性は果てしなく。
大手製薬会社が共同研究に踏み切ったのは、HMGB1が持つ可能性の高さからだ。この核タンパクは生体内のすべての細胞の核内に存在している。だとすれば壊死した組織に外胚葉由来の幹細胞を動員して修復する再生誘導メカニズムは、皮膚だけでなく、あらゆる臓器や組織に共通していると考えられる。国内の患者数約1,000人とされる表皮水疱症だけでなく、ケタ違いに患者の多い脳梗塞や心筋梗塞、
再生が難しいとされている膝軟骨の再生などへの適用が期待される。しかもHMGB1の活性ドメインはペプチドとして化学合成できコストを抑えられるうえ、生体内のメカニズムを利用するため安全性が高い利点もあるからだ。2019年には、すでに脳梗塞をターゲットにした企業治験も実施されている。
これまでにない再生誘導医薬への道を開いた玉井教授は「HMGB1は抗生物質に例えれば発見されて間もないペニシリンみたいなもの。同じような働きをする分子はまだまだあるはずで、その一つ一つが薬のターゲットになる。再生誘導メカニズムの分子基盤を解明し、新しい薬をだして患者さんに還元することが阪大の責任」と話す。
少年との約束の日から、いくつもの壁を越えた先に漸く辿り着いた「再生誘導」のメカニズム。
その物語は、まだ序章だ。
玉井教授にとって研究とは
皮膚は地球を救う 私の出会った表皮水疱症の子供たちは、つらい病気にもかかわらず、他者を思いやる優しい気持ちの持ち主ばかりでした。患者の赤ちゃんたちは、オギャーと生まれてからお母さんが毎日、何時間もかけて肌の手入れをします。肌と肌の触れ合いで優しい心をはぐくむメカニズムが人間の皮膚には備わっているのではないか。私はそれを「スキンシップ遺伝子」と呼び、科学的に証明したいと思っています。母子間の肌のふれあいによって、他者を思いやる心が育まれることをサイエンスで明らかにできれば世界中の教育が変わり、表皮水疱症の子どものような優しい心を持った人々が世界中にあふれます。そうなれば、世界中から戦争などなくなります。サイエンスで世界を救うのが私の夢です。
●玉井 克人(たまい かつと)
大阪大学大学院医学系研究科再生誘導医学寄附講座 寄附講座教授
1986年弘前大学医学部卒業。90年同大学大学院医学研究科博士課程修了。同年弘前大学医学部附属病院皮膚科助手。青森県立中央病院皮膚科、弘前大学医学部皮膚科助手などを経て、91年米国ジェファーソン医科大学皮膚科留学。96年弘前大学医学部附属病院皮膚科講師、2003年大阪大学大学院医学系研究科遺伝子治療学助教授、04年同准教授。10年より現職。
■ 再生医療をはじめ人のもつ再生の機能に迫る研究者たちの物語「再生の医学~“志”のスペシャリテ6選~」を引き続きお楽しみください。
再生の医学~“志”のスペシャリテ6選~ #1 医学系研究科 教授 澤 芳樹
再生の医学~“志”のスペシャリテ6選~ #2 医学系研究科 教授 西田 幸二
再生の医学~“志”のスペシャリテ6選~ #3 工学研究科 教授 紀ノ岡 正博
再生の医学~“志”のスペシャリテ6選~ #4 歯学研究科 教授 村上 伸也
再生の医学~“志”のスペシャリテ6選~ #5 医学系研究科 寄附講座教授 玉井 克人
「再生誘導」とは?皮膚の難病研究から明らかになった 「再生」のメカニズム
再生の医学~“志”のスペシャリテ6選~ #6 医学系研究科 教授 加藤 和人
(2019年12月取材)

