慢性アレルギー疾患に関わるヒスタミン受容体の構造解明
新規アトピー性皮膚炎・喘息治療薬の開発に貢献
概要
京都大学大学院医学研究科 林到炫 (イム ドヒョン) 助教、岩田想 同教授 (兼 理化学研究所放射光科学研究センターグループディレクター)、浅田秀基 同特定准教授らの研究グループは、大阪大学蛋白質研究所 加藤貴之 教授、京都工芸繊維大学 応用生物学系 岸川淳一 准教授 (論文投稿時は大阪大学蛋白質研究所に在籍)、京都大学医生物学研究所 野田岳志 教授、杉田征彦 同准教授 (兼: 白眉センター准教授) らとの共同研究により、ヒスタミンH4受容体 (H4R)の立体構造を、クライオ電子顕微鏡法 (Cryo-EM)を用いて解明しました (図1)。生体アミンの一種であるヒスタミンは、ヒスタミン受容体を刺激することによりアレルギーや炎症に関与します。4種類のヒスタミン受容体の中でH4R は、アトピー性皮膚炎や喘息などの慢性アレルギー疾患の治療標的として注目されています。本研究により、今まで未知であったH4Rの立体構造が明らかになり、薬理学的特徴が異なる2種類の作動薬 (ヒスタミン、イメチット) の結合構造をそれぞれ決定することで、H4Rが持つ特異的なリガンド認識機構を解明しました。特にイメチットの結合によるPhe344の構造変化は、新たな空洞「Aromatic slot」を形成し、サブタイプ選択性に重要な役割を果たしていることが分かりました。これらの結果は、ヒスタミン受容体のサブタイプ選択性の分子的基盤を洞察し、H4Rを標的とする薬剤の合理的なデザインに貢献できることが期待されます。本成果は、2023年10月20日に国際学術誌「Nature Communications」にオンライン掲載されます。
図1. 慢性アレルギー疾患の作用機序とヒスタミンH4受容体のCryo-EM構造
研究の背景
アトピー性皮膚炎と喘息は、花粉症と同様に代表的なアレルギー疾患です。アトピー性皮膚炎は、皮膚のバリア機能の低下によるかゆみを伴う湿疹が全身に現れるのが特徴であり、喘息は、慢性的な炎症から気管支が狭くなったことによる呼吸困難を伴う咳が特徴です。これらのアレルギー疾患は、外部からのアレルゲン (アレルギー症状を起こす物質) の侵入により免疫細胞が過剰に刺激されることで発症すると考えられていますが、これらの発症メカニズムはまだ解明されておらず、症状を緩和させる対処療法しかないのが現状です。
Gタンパク質共役受容体 (GPCR)であり、4種類あるヒスタミン受容体の中で最後に見つけられたヒスタミンH4受容体 (H4R) は、主に好酸球や肥満細胞などの炎症細胞に発現しており、これらの炎症部位への走化と炎症物質 (サイトカインなど) の放出に関与しています。それによって主要な炎症細胞が組織部位に動員されやすくなり、慢性炎症が引き起こされると考えられています。そのため、H4Rはアトピー性皮膚炎や喘息など慢性アレルギー疾患の新規治療標的として注目されており、H4Rを標的とした新しい治療薬の開発が試みられていますが、未だ効果的な治療薬は存在していません。本研究は今まで未知であったH4Rの立体構造を明らかにすることに成功しました。また、内因性炎症物質であるヒスタミンが結合したH4Rの構造とH4R選択的作動薬のイメチットがどのようにH4Rに結合しているのかを明らかにすることで、2つの異なる薬理学特徴を構造から説明することができました。特に、H4Rの1つのアミノ酸 (Phe344) の構造変化が、「Aromatic slot」を形成することがイメチットの結合および選択性において重要な役割を果たしていることが分かりました。アトピー性皮膚炎や喘息の発症に重要な役割を担っているヒスタミンH4受容体 (H4R) の立体構造が明らかになることで、これらの疾患の治療法確立に貢献できると考えられます。
研究手法・成果
本研究において私たちは、生体アミンであるヒスタミンおよびH4R選択的作動薬のイメチットが結合したH4Rの立体構造をCryo-EM単粒子解析法により原子レベルで解明しました。Cryo-EMは、タンパク質の立体構造を決定する革新的技術として2017年にノーベル化学賞を受賞した方法です。Cryo-EMは、膜タンパク質の構造決定法として非常に強力な技術であり、私たちのH4RのようなGPCRを含む多くの膜タンパク質の構造決定に利用されています。私たちはスクリーニング測定用と本測定用の2種類のクライオ透過型電子顕微鏡 (cryo-TEM) を用いた効率的な構造決定法を確立しました。スクリーニングCryo-EMでは京都大学医生物学研究所に設置されているGlacios cryo-TEMを用いて野田岳志 教授、杉田征彦 准教授らと、本測定Cryo-EMでは大阪大学蛋白質研究所のTitan Krios cryo-TEMを用いて加藤貴之 教授、岸川淳一 助教 (当時。現在は 京都工芸繊維大学応用生物学系 准教授) らと連携し、今回の構造を決定することができました。
ヒスタミンは4種類存在するヒスタミン受容体の全てに結合しますが、イメチットはH4Rにのみに強く結合することが知られています。私たちはヒスタミンとイメチットが結合したH4Rの立体構造を決定しました。これら2つの構造を比べると、4つのアミノ酸残基 (Tyr319、Phe344、Gln347、Trp348) から成る「Aromatic slot」において、H4R選択的作動薬であるイメチットが結合する時にPhe344の向きが変わること、この変化がヒスタミンよりイメチットの結合により適していることを明らかにしました (図2)。さらに、ヒスタミンが結合したH1Rとの比較から、H1Rではアスパラギン (Asn198) であるアミノ酸残基がH4Rではグルタミン酸 (Glu182) となっており、これがヒスタミンに対するH1RとH4Rの結合親和性の差となっていること、また「Aromatic slot」を構成するアミノ酸のうち、イメチットの結合に重要なフェニルアラニン (Phe344) がH1Rではイソロイシン (Ile454) となっており、これがイメチットのH4R選択性に重要であることが分かりました (図3)。これらの結果は、薬により結合の仕方に違いがあり、その違いが薬の効果に大きく影響を与える可能性があることを『形』から教えてくれます。このように薬が結合している形を知ることは、薬の最適化につながるものと期待されます。
図2. 内因性炎症物質ヒスタミンとH4R選択的作動薬イメチットが結合したH4Rの構造比較
ヒスタミンとイメチットの結合様式の比較により、ヒスタミンが結合した構造からは見えなかった、4つのアミノ酸からなる「Aromatic slot」の変化が観察されました。特にPhe344が変化することで、H4R選択的作動薬であるイメチットと「Aromatic slot」の相互作用がより強くなっており、これがイメチットのH4Rに対する親和性向上に寄与していることが示されました。
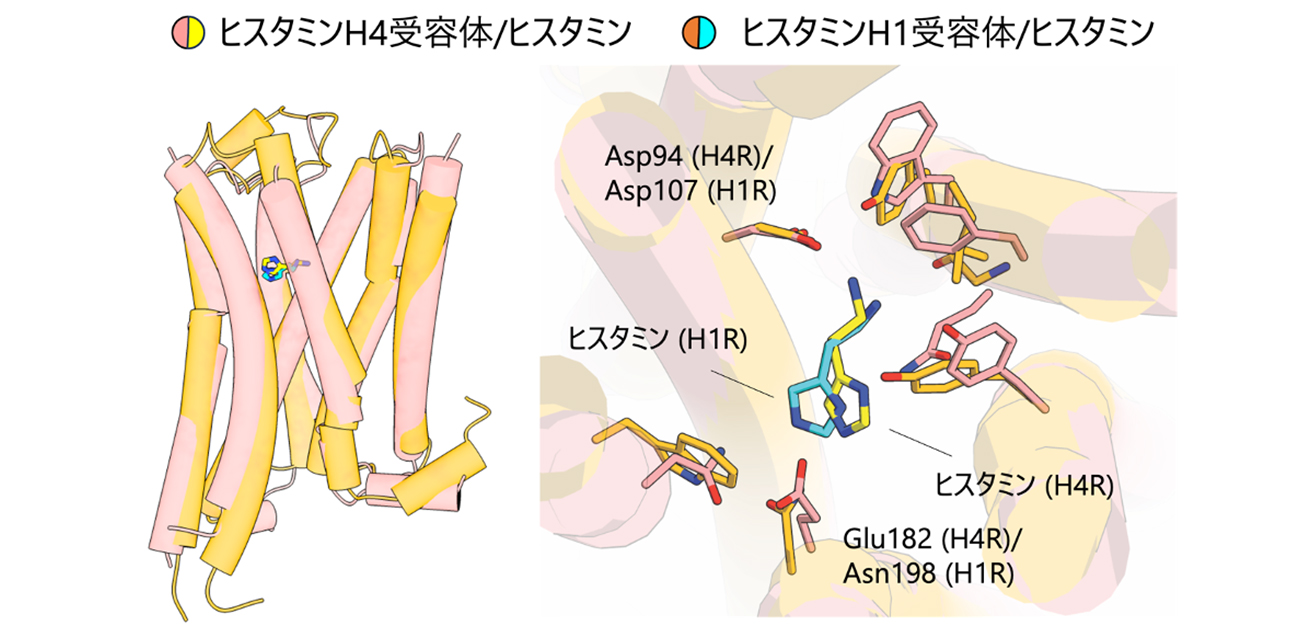
図3. ヒスタミンが結合したH1Rとヒスタミン、イメチットが結合したH4Rの構造比較
これらの構造において、ヒスタミンの結合に重要であるアスパラギン酸 (Asp94/107) はどちらも保存されていますが、イミダゾール環と相互作用するアミノ酸残基 (Glu182/Asn198) に違いがあることが分かりました。ヒスタミンは、全てのヒスタミン受容体と結合しますが、その結合親和性は大きく異なり、H1RよりH4Rに強く結合することが知られています。H4RのGlu182はH1RのAsn198よりヒスタミンと強く相互作用することから、この親和性の差の説明が可能となりました。一方、「Aromatic slot」を構成し、イメチット結合に重要な役割を担うアミノ酸がH1R (Ile454) とH4R (Phe344) で異なっているため、H1Rのスロットとして機能はH4Rに比べて弱いことが明らかとなりました。イメチットはH1Rには結合せず、H4Rに強く結合することが知られていますが、この選択性の差が「Aromatic slot」の違いによるものであることが示されました。
波及効果、今後の予定
今回、私たちが決定したヒスタミンおよびイメチットが結合したH4Rの構造から、H4Rに対する選択性の違いによってH4Rの「Aromatic slot」と名付けた領域の構造が変化し、その結合様式の差が受容体選択性に重要であることを原子レベルで明らかにすることができました。
H4Rはアトピー性皮膚炎や喘息と深い関係がある受容体であると考えられています。そのため、多くの研究が行われておりますが、これらのH4R関連疾患に対する効果的な治療薬は未だ存在しないのが現状です。その最大の原因は、十分な受容体選択性を持つ治療薬の開発が難しいことです。ヒスタミン受容体は4つのサブタイプが存在しており、H4Rだけでなく他のサブタイプに結合することが副作用の要因になります。残念ながら今回構造を決定したイメチットもこの点において不完全な薬剤です。しかし、私たちの構造から提示された結果は、ヒスタミン受容体に対する選択性がどのように生じるのかという問いに対する1つの解答であると考えられます。従って、この違いを利用することでアトピー性皮膚炎などのH4R関連疾患に対してより効果的なH4R選択的薬剤開発が可能になることが期待されます。
特記事項
<論文情報>
タイトル:Structural Insights into the Agonists Binding and Receptor Selectivity of Human Histamine H4 Receptor
(ヒトヒスタミンH4受容体のアゴニスト結合と受容体選択性に関する構造的洞察)
著 者:Dohyun Im, Jun-ichi Kishikawa, Yuki Shiimura, Hiromi Hisano, Akane Ito, Yoko Fujita-Fujiharu, Yukihiko Sugita, Takeshi Noda, Takayuki Kato, Hidetsugu Asada, and So Iwata
掲 載 誌:Nature Communications
DOI:10.1038/s41467-023-42260-z
本研究は、日本学術振興会 (JSPS) の科学研究費助成事業、国立研究開発法人日本医療研究開発機構 (AMED) の創薬等先端技術支援基盤プラットフォームなどの多くの支援を受けています。
研究者のコメント
アレルギーは今や国民病と言える疾患です。その中でもアトピー性皮膚炎や喘息は対処療法しか存在しない難治性疾患であり、その症状は耐え難いものです。現在も多方面の研究が行われており、これらの疾患に対する治療薬の開発は続けられています。しかし、特に選択性の欠如に伴う副作用など改善すべき点が多く存在するため、有効な治療薬は存在していません。今回、H4R選択的作動薬が結合したH4Rの構造を決定したことで、原子レベルでなければ分からなかった変化を直接『見る』ことに成功しました。今回見えた構造がこれらの疾患に対する治療法確立に利用されることを期待しており、今後もこれらの疾患に対する治療薬の開発に資する構造情報を提供していきたいと考えています。
本研究は、多くの共同研究者の協力なしでは遂行することはできませんでした。特に、Cryo-EM技術なしではこの結果を得ることはできませんでした。これらの技術を支えてくれた共同研究者の方々を初め、本研究に携わった全ての方々に感謝致します。
用語説明
- ヒスタミン受容体
ヒスタミンを受容するGPCR。H1RからH4Rまでの4つのサブタイプが存在している。H1Rは平滑筋や血管内皮細胞などに発現しており炎症やアレルギーを、H2Rは胃の細胞などに発現しており胃酸分泌を、H3Rは中枢神経に発現し神経伝達物質の放出を、H4Rは肥満細胞などに発現し、免疫細胞の遊走を担っている。
- Cryo-EM (Cryogenic electron microscopy)
クライオ電子顕微鏡法。タンパク質などの凍結した生体試料に電子線を照射し、試料の観察を行うために透過電子顕微鏡(TEM)を用いる。試料から得られた2次元投影像を単粒子解析技術により3次元再構成し、生体分子の立体構造を決定する。
- ヒスタミン
生体アミンの1つ。肥満細胞などにより生産される。血圧降下、血管透過生亢進、平滑筋収縮などの薬理作用を担う。
- Gタンパク質共役受容体(GPCR)
細胞膜に存在する受容体。ヒスタミンなどの細胞外の物質を受容し、その情報を細胞内にGタンパク質を介して伝達することで恒常性維持の調節などを行う。
