「2度目の敵には 素早く攻撃」免疫反応の仕組み解明
メモリーB細胞を人為的に制御し効果的なワクチン開発へ
リリース概要
免疫学フロンティア研究センターの黒崎知博教授(理化学研究所統合生命医科学研究センター兼任)を中心とする共同研究グループは、免疫記憶を司っている主要な免疫細胞であるメモリーB細胞 が再度の感染に素早く反応するのは、転写因子 Bach2の発現量低下が要因であることを、マウスを使った実験で明らかにしました。
研究の背景
私たちの体は、1度出会った細菌やウイルスなどの抗原に再び出会うと、1度目よりも大量の抗体 を迅速に作り出して速やかに細菌、ウイルスを除去し生体を防御します(免疫メモリー反応)。この反応を典型的に用いているのがワクチン療法です。これは、1度目の免疫反応で細菌・ウイルスの抗原を記憶した、メモリーB細胞が2度目の細菌・ウイルスの侵入の時に素早く反応するためです。この迅速反応は、「B細胞の表面に発現しているB細胞抗原受容体(BCR)の型の違いに起因する」という説と、「B細胞の細胞内部に発現している分子群の違いが引き起こしている」という説が唱えられていましたが、いまだ実証されていませんでした。
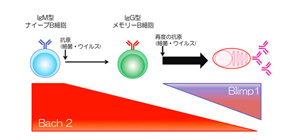
ナイーブB細胞はBach2発現量が高いのに対し、メモリーB細胞は発現量が低い。そのため、メモリーB細胞は抗体産生細胞の分化に必要なBlimp1の発現が増加しやすく、迅速に抗体産生細胞へ分化できる。
本研究成果が社会に与える影響(本研究成果の意義)
黒崎教授らのグループは、遺伝子改変マウスなどを用いた解析の結果、従来の仮説を覆し、細胞内における転写因子Bach2の発現量低下が、記憶B細胞から抗体産生細胞への分化に重要であることを突き止めました。メモリーB細胞の不足は感染防御に対する能力を低下させます。逆に、過剰な活性化はアレルギーや自己免疫疾患を引き起こします。今後、転写因子Bach2を標的とした効果的なワクチン開発につながることが期待できます。
特記事項
本研究は、独立行政法人科学技術振興機構(JST)の戦略的創造研究推進事業チーム型研究(CREST)「アレルギー疾患・自己免疫疾患などの発症機構と治療技術」研究領域(菅村和夫研究総括)における研究課題「液性免疫制御による新しい治療法の開発」(研究代表者:黒崎知博)の一環として行われました。
研究の詳細な説明
研究の背景
最初に細菌・ウイルスといった抗原に遭遇したIgM型ナイーブB細胞は、抗体産生細胞に分化し、抗体を作る様になります。その時同時に、胚中心B細胞を経てIgG型メモリーB細胞を作ります (図1) 。生体が、最初に遭遇したのと同じ抗原に遭遇すると、IgG型 メモリーB細胞はより迅速に抗体を作り出して効率的に抗原を排除します (図2) 。
しかしながら、「IgG型メモリーB細胞がどのようなメカニズムを用いて素早く抗体を産生する様になるのか」は不明のままでした。それを説明する仮説として、大きく2つが存在していました。IgG型BCRはIgM型BCRよりも細胞内にシグナルを伝達する能力が高いことが知られています。従って、第一の仮説は、「B細胞の活性化・分化のしやすさは、細胞表面に発現しているBCR分子の型に起因する」というものです。一方、「ナイーブB細胞とメモリーB細胞は細胞内に発現している分子群にも違いがあり、このことが活性化・分化の能力の違いを引き起こしている」という仮説も唱えられていました。しかしながら、そのどちらが正しいのかは長く議論されていましたが、今まで決着はついていませんでした (図3) 。
そこで共同研究グループは、未だ抗原にさらされていないナイーブB細胞がIgG型BCRを有する(IgG型ナイーブ)マウスを人為的に作製し、仮説の検証に取り組みました。
研究手法と成果
通常のマウスは (図2) 、仮説1の検証に必要なIgG型のBCRを持ったナイーブB細胞(IgG型ナイーブB細胞)を持ちません。そこで共同研究グループは、先天的にIgG型ナイーブB細胞を持つクローンマウスを作製しました。そして、IgG型ナイーブB細胞とIgM型ナイーブB細胞に抗原を投与し、抗体産生細胞への分化能力を評価したところ、同程度でした (図4) 。このことから、BCRの型の違いだけでは、抗体産生細胞への高い分化能力を説明できないと分かりました。
次に、仮説2を検証するためにメモリーB細胞とナイーブB細胞の主立った遺伝子の発現量を比較したところ、メモリーB細胞の方が転写因子「Bach2」をコードするBach2遺伝子の発現量が5分の1に低下していることが分かりました。そこで、分子生物学的手法によりIgM型ナイーブB細胞のBach2の発現量を減らすと、減らす前より抗体産生細胞に分化しやすくなりました (図5) 。これらの結果から、B細胞から抗体産生細胞への分化を抑制する機能を持つ転写因子Bach2の発現量が、メモリーB細胞では低下するため、抗体産生細胞への分化能力が高くなると分かりました (図6) 。
今後の期待
今回、メモリーB細胞では、転写因子Bach2の発現量が厳密に制御されていることが、同じ抗原に再び出会ったときの迅速な応答に必要であることを明らかにしました。つまり、メモリーB細胞におけるBach2の発現量が正しく制御されないと、抗体が異常に作られてアレルギー反応や自己免疫疾患を引き起こしたり、抗体が十分に作られずに抗原に対する防御機能が低下したりしてしまう可能性を示唆しています。
メモリーB細胞の働きを理解することは、近年、猛威を振るっているインフルエンザなどに対する効果的なワクチンを開発するうえでも重要です。今後転写因子Bach2は、ワクチンや免疫疾患の創薬開発において新しい標的となると期待できます。
発表論文
・Kohei Kometani, Rinako Nakagawa, Ryo Shinnakasu, Tomohiro Kaji, Andrei Rybouchkin, Saya Moriyama, Koji Furukawa, Haruhiko Koseki, Toshitada Takemori and Tomohiro Kurosaki.
・“Repression of Bach2 contributes to predisposition of IgG1 memory B cells toward plasma cell differentiation”
・Immunity
2013年7月11日(12:00pm 米東海岸)(日本時間: 7月12日(金)午前1時) online掲載予定
参考図

図1 抗原に出会った時のそれぞれのB細胞の抗体産生細胞への分化
IgM型ナイーブB細胞は抗原に出会うと胚中心B細胞へ分化し、一部が抗体産生細胞に分化する。一方、IgG型メモリーB細胞は、抗体産生細胞へ迅速に大量に分化する。
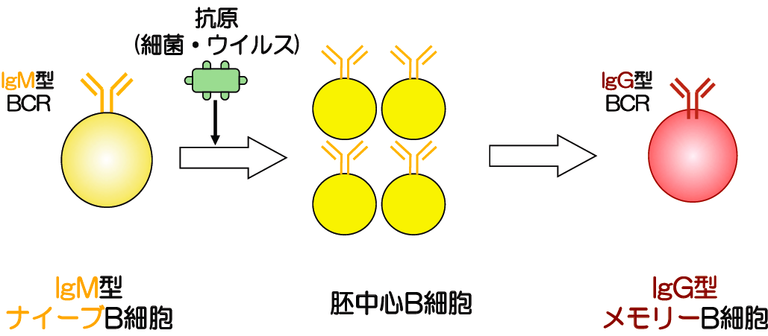
図2 IgM型ナイーブB細胞からIgG型メモリーB細胞への分化
IgM型ナイーブB細胞は細菌やウイルスといった抗原に出会うと活性化し、胚中心B細胞と呼ばれる活発に増殖し細胞の数を増やし、質の良いBCRを作り出す状態へと変化する。その後その一部は、メモリーB細胞となる。この過程で、BCRの型がIgM型からIgG型へと変化する。
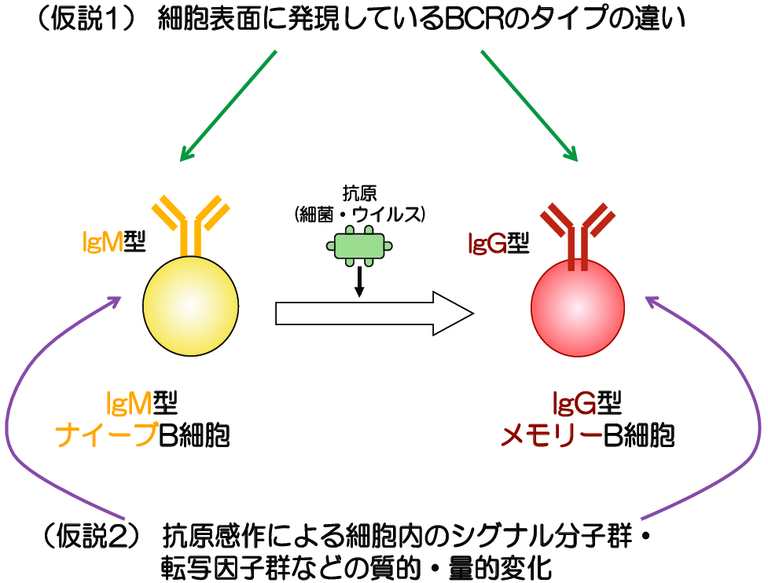
図3 2つの仮説
IgM型ナイーブB細胞とIgG型メモリーB細胞の分化能力の違いに関する2つの仮説がある。仮説1は、細胞表面に発現しているBCRの型の違い(IgM型かIgG型)により引き起こされるという説。仮説2は、抗原に出会い一度活性化することで生じるシグナル分子群・転写因子群などの質的・量的違いが原因であるという説。

図4 BCRの型の違いによるナイーブB細胞の抗体産生細胞への分化能力の比較
仮説1を検証するためにIgG型ナイーブB細胞の分化能力を検討した。IgG型ナイーブB細胞の分化能力は、IgG型メモリーB細胞よりも、IgM型ナイーブB細胞に似た分化能力を示した。このことは、BCRがIgG型になるだけでは迅速反応を引き起こせないということを示している。

図5 転写因子Bach2の減少による抗体産生細胞への分化能力の変化
IgM型ナイーブB細胞のBach2遺伝子発現量を減少させ、抗体産生細胞への分化能を測定した。転写因子Bach2を低下させた細胞は、抗体産生細胞(CD138+)が1.8倍増えた。
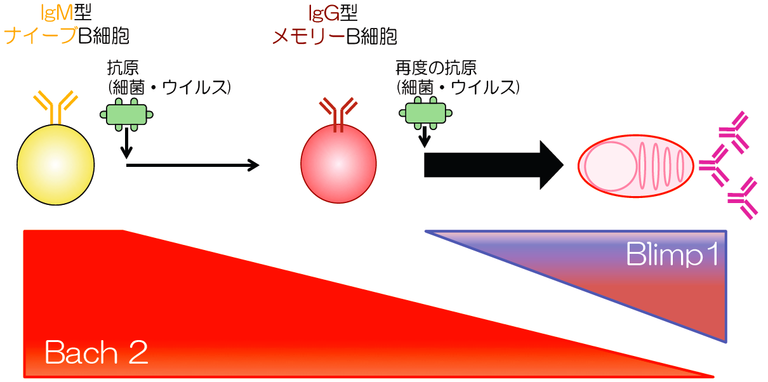
図6 それぞれのB細胞の抗体産生細胞への分化イメージ
IgM型ナイーブB細胞はBach2発現量が高いのに対し、IgG型メモリーB細胞は発現量が低い。Bach2は抗体産生細胞の分化に必要なBlimp1分子の発現を抑える働きをしている。そのため、IgG型メモリーB細胞は再度の抗原(細菌・ウイルス)暴露により、Blimp1の発現が増加しやすいため抗体産生細胞へ迅速に大量に分化できる。
参考URL
免疫フロンティア研究センター 分化制御研究室
http://lymph.ifrec.osaka-u.ac.jp/index_j.html
用語説明
- B細胞
免疫細胞の一種で、表面にあるB細胞抗原受容体(BCR)と呼ばれるタンパク質で病原体などの抗原を認識し、抗体を産生する。
- 転写因子
遺伝子の働きをオンにしたりオフにしたりする機能を持つタンパク質。DNA上に存在する転写を制御する領域に結合し、遺伝子発現のタイミングや量を調節する。
- 抗体
B細胞が分泌するタンパク質で、抗原に結合し生体防御に働く。抗体が結合した抗原は破壊されるか体から排除される。
- IgG型
IgG型、IgM型:
ある1つの抗原を認識する抗体がさまざまな機能を発揮するために、抗体は一部分を異なる形に変更したものを作り出すことができる。元々の型をIgM型といい、そこからIgG型、IgA型、IgE型という異なる型の抗体を作り出す。
