細胞の仕組みを知り難病克服へ
エネルギー産生プロセスを司る酵素活性調節分子を発見
医学系研究科 生命機能研究科・准教授・新谷泰範
ほとんどの生物には、酸素を使ってエネルギーを取り出し、ATP(アデノシン3リン酸)に変換するプロセスが組み込まれている。人体にもこのエネルギー産生プロセスが存在し、ミトコンドリアはその仕組みを担っている。ところがこのエネルギー産生プロセスがうまく働かなくなる難病がある。「ミトコンドリア病」だ。ミトコンドリア病は、有効な治療法がいまだに見つかっていない。新谷泰範准教授は、ミトコンドリア病の治療薬開発をめざし、チトクロームcオキシダーゼという酵素の研究を行っている。また、近年再び発症者が増えている結核の新薬研究にも取り組んでいる。

エネルギー産生効率を上げる電子の流れに着目
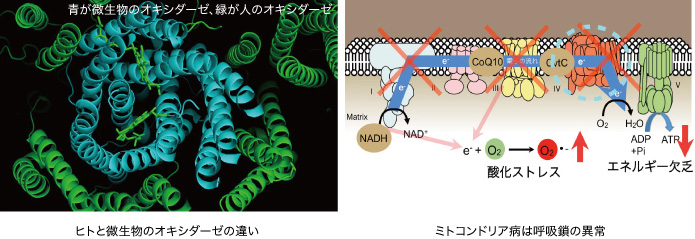
酸素を使ってエネルギーを生み出せなくなる難病、ミトコンドリア病(呼吸連鎖異常症)。症状が脳に出ればけいれん、てんかんを、心臓に出れば心不全、不整脈を引き起こす。さらに低身長、糖尿病、筋力低下などの症状が起きる場合もある。患者数は4300人に1人と推定されており、先天性の代謝異常の中では最も多い病気である。日本で難病登録をしている人は1087人(平成24年度)だが、実数はもっと多く、2万人に上ると予想されている。
「チトクロームcオキシダーゼという酵素は、ミトコンドリアが酸素を使ってエネルギーを作りだす過程で働き、電子の伝達をATP合成に変換する仕組みにおいて必須の酵素です。ところが、ミトコンドリア病になると、エネルギーを十分に作れなくなります。原因となる遺伝子の異常を特定できなくても、チトクロームcオキシダーゼの活性を促進し、電子の流れを全体として良くすれば、ATP合成速度を上げることができるのではと考えて研究を始めました」

酵素の活性を調節し、ミトコンドリア病の治療薬を
その結果、チトクロームcオキシダーゼを活性化させる分子Higd1a(ヒグディー・1・エー)を心筋細胞で発見。「低酸素状態にした魚の心臓では、ATP産生量が減ってしまいますが、Higd1aを投入すると、チトクロームcオキシダーゼが活性化し、酸素が少なくてもATP合成速度が保持され、魚の心臓の拍動もよくなるという結果が出ました」。Higd1aによりチトクロームcオキシダーゼの活性を調整すれば、ミトコンドリア病の治療効果が上がることが分かったのだ。
その後、新谷准教授は、全国の研究者に開かれた約22万種の化合物ライブラリーを利用して、チトクロームcオキシダーゼの酵素活性を調節する化合物探しを始めた。「『薬のたね』になりそうな化合物の候補が見つかったので、今はマウスを使い、さらに検証を進めています。人に使えるものに磨き上げるのはその次のステージ。10から15年かかる創薬プロセスの中で、3年目ぐらいのところに来ています」
結核の治療薬開発にも乗り出す
一方、チトクロームオキシダーゼの活性を抑えることで結核と戦う薬の開発研究も始めている。結核は、第2次世界大戦後に特効薬が登場。治療の目処がついたと考えられ、新しい薬が作られなくなった。しかし、1990年前後より世界的流行が再燃。もともと結核菌は死滅しにくく、治療が終わる前に服薬をやめてしまったり、既存の薬が効かない耐性菌も増え、今では三大感染症(HIV、マラリア、結核)のなかで最も死者数が多い病気となっている。
そこで、新谷准教授は、結核菌を死滅させるのではなく、結核菌がもっているチトクロームオキシダーゼの活性を抑えることで、結核菌のエネルギー産生を阻害すればよいと考えた。「結核菌のチトクロームオキシダーゼと人のチトクロームオキシダーゼは形が違います。X線結晶構造解析により原子レベルで構造の違いを解き明かし、薬を作ろうというアイデアで、製薬会社との共同研究を進めています」

新谷准教授にとって研究とは
やればやるほど奥深い。難しい。でもおもしろい。もともと循環器内科の医師。人工心臓など新規に確立された治療の効果を目の当たりにし、自身も創薬を実現し、医療に役立つ研究をしたい。
●新谷泰範(しんたに やすのり)
2005年大阪大学大学院医学系研究科修了、博士(医学)。07年英国William Harvey Research Institute博士研究員、13年大阪大学大学院医学系研究科助教を経て、17年から現職。
未知の世界に挑む研究者の物語 『究みのStoryZ』 に戻る
阪大生と卒業生の物語 『阪大StoryZ』 に戻る
(2018年3月取材)
