セマフォリンは鼻ポリープ形成を誘導する鍵分子
難治性ちくのう症の新たな診断と治療のターゲット
研究成果のポイント
・難治性の副鼻腔炎において、セマフォリンというタンパク質がアレルギー反応や鼻ポリープの形成を誘導していることを発見した。
・セマフォリンの血中濃度が高い患者さんは、この病気が重症かつ難治であった。
・セマフォリンを抑制する抗体治療を行うと、動物モデルにおいて好酸球性副鼻腔炎が著明に軽快することを見出し、同疾患の今後の診断や治療に役立つことが大いに期待できる。
概要
大阪大学大学院医学系研究科の西出真之助教 1 、津田武医師 2 、猪原秀典教授 2 、熊ノ郷淳教授 1 らの研究グループ( 1 呼吸器・免疫内科学、 2 耳鼻咽喉科・頭頚部外科学)は、セマフォリンというタンパク質が、鼻ポリープを形成する難治性のちくのう症である「好酸球性副鼻腔炎」の病態形成に重要な役割を果たしており、治療の標的となることを明らかにしました。
好酸球性副鼻腔炎は鼻ポリープを高い確率で合併し、手術やステロイド投与による既存の治療法では、一度治療した後の再発率が高く、正確な病態の理解に基づいた、安全かつ効果的な治療方法が求められています。
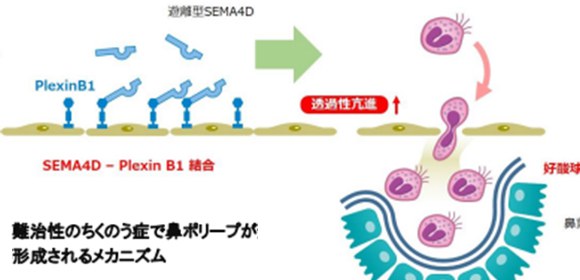
今回、津田武医師、西出真之助教らの研究グループは、好酸球上に発現しているセマフォリン4D(SEMA4D)が、好酸球の活性化に伴って細胞から遊離し、血管の内皮細胞や鼻腔の上皮細胞に働きかけ、血管や上皮の結合を緩めて好酸球を通り抜けやすくすることが、アレルギー反応を悪化させ、鼻ポリープの形成に関与していることを解明しました (図1) 。さらに、SEMA4Dは、炎症を引き起こす様々な分子(サイトカイン)を上皮から分泌させることもわかりました。
実際の患者さんにおいても、SEMA4Dの血中濃度は好酸球性副鼻腔炎の重症度と相関しており、SEMA4D濃度が高い患者さんはこの病気が重症かつ難治性であることが分かりました。さらに、SEMA4Dを中和する抗体を用いると、動物モデルにおいて好酸球性副鼻腔炎が著明に軽快することを見出したことから、今後の診断や治療に役立つことが大いに期待されます。
本研究成果は、臨床アレルギー学のトップジャーナルのひとつである米国アレルギー・喘息・免疫学会(AAAAI)の機関誌「The Journal of Allergy and Clinical Immunology」に、2月6日(木)0時(日本時間)に公開されました。

図1 難治性のちくのう症で鼻ポリープが形成されるメカニズム
研究の背景
好酸球性副鼻腔炎は鼻ポリープを高い確率で合併し、多くの患者さんは鼻づまり・どろどろの鼻汁・嗅覚(におい)の障害を訴えます。日本では、中等度から重症以上の患者さんの数が約2万人存在すると言われています。治療は内視鏡により鼻ポリープを切除する手術や、ステロイドの投与などが行われますが、一度治療した後の再発率が高く、正確な病態の理解に基づいた、安全かつ効果的な治療方法が求められています。
セマフォリンは、もともと神経発生を誘導する因子として発見されたタンパク質ですが、近年では腫瘍免疫や、骨代謝・自己免疫疾患との密接な関連が報告されています。さらに好中球などの「顆粒球」と呼ばれる白血球におけるセマフォリンの機能もここ数年で明らかになり、血管炎やアレルギー疾患に対する創薬ターゲットとしても注目を集めています。しかし、難治性ちくのう症におけるセマフォリンの効果は調べられておらず、実際に診断や治療のターゲットになるのか詳細は分かっていませんでした。
研究グループが注目したセマフォリン4D(SEMA4D)という分子は、通常は色々な細胞の膜表面に存在する分子として存在していますが、細胞表面で刺激を受けて切断されます。切断された遊離型のSEMA4Dは、細胞間のシグナル伝達に関わります。今回、研究グループは、鼻ポリープを形成する難治性の副鼻腔炎である「好酸球性副鼻腔炎」の患者さんの血液から、SEMA4Dとの関わりを調べ、治療の標的となるのかを検証しました。
本研究の成果
研究グループにより、好酸球副鼻腔炎の患者さんの血中では、遊離型SEMA4D濃度が上昇しており、その濃度が重症度に相関していることが発見されました。また好酸球副鼻腔炎の患者さんの白血球においては、好酸球特異的に膜型SEMA4Dが減少しており、好酸球上のSEMA4Dが切断され、膜上の発現が低下、その結果として血中の遊離型SEMA4D濃度が上昇していました。好酸球性炎症において遊離型SEMA4Dがどのような役割を持っているか、さらに追求するために、鼻腔上皮細胞株に対する刺激実験を行った結果、SEMA4Dは鼻腔上皮細胞において細胞内タンパク質のRhoAの活性化を介した、透過性の亢進に寄与することが示されました。
これは、好酸球上に発現しているセマフォリン4D(SEMA4D)が、好酸球の活性化に伴って細胞から遊離し、SEMA内皮細胞や鼻腔の上皮細胞に働きかけ、血管や上皮の結合を緩めて好酸球を通り抜けやすくすることが、アレルギー反応を悪化させ、鼻ポリープの形成に関与していることを示します。
さらに、SEMA4Dは、インターロイキン6(IL-6)などの炎症を引き起こす様々な分子(サイトカイン)を上皮から分泌させることもわかりました。
これらを踏まえて、好酸球性副鼻腔炎の動物モデルにおいて、SEMA4Dに対する抗体を用いて中和実験を行ったところ、好酸球性炎症が軽快することを見出しました。
本研究成果が社会に与える影響(本研究成果の意義)
本研究により、日本国内で患者さんが多い難治性のアレルギー疾患である好酸球性副鼻腔炎において、セマフォリン分子がアレルギー反応や鼻ポリープの形成を誘導していることを発見しました。患者さんの中でも、セマフォリンの血中濃度が高い方は重症かつ難治性であることが分かりました。さらに、セマフォリンを中和する抗体を用いると、動物モデルにおいて好酸球性副鼻腔炎が著明に軽快することを見出しました。
この結果から、血清の遊離型SEMA4D濃度は、好酸球性副鼻腔炎の病勢を反映するマーカーとして有用であり、好酸球由来のSEMA4Dはアレルギー炎症を増悪させる因子として、好酸球性副鼻腔炎における新たな治療ターゲットとなることが考えられます。
研究者のコメント(津田武医師)
好酸球性副鼻腔炎の患者様は様々な病気の経過をたどります。軽快しやすい患者様もいらっしゃれば、逆になかなか改善しない患者様もいらっしゃいました。「なぜ同じ病気でもこのように経過が全く異なるのだろう」という疑問をスタートとして、その病態解明の一助となる研究を行えたことを大変意義深く感じています。今後も好酸球性副鼻腔炎の患者様の治療に注力していきたいと思っています。よろしくお願いいたします。
特記事項
本研究成果は、2020年2月6日(木)0時(日本時間)に米アレルギー・喘息・免疫学会(AAAAI)の機関誌である「The Journal of Allergy and Clinical Immunology」(オンライン)に掲載されました。
タイトル:“Pathological and therapeutic implications of eosinophil-derived Semaphorin 4D in eosinophilic chronic rhinosinusitis”
著者名:Takeshi Tsuda MD 1,2,3,∔ , Masayuki Nishide MD, PhD 2,3,∔,* ,Yohei Maeda, MD, PhD 1 ,Yoshitomo Hayama, MD,PhD 4 ,Shohei Koyama, MD, PhD 2.3 , Satoshi Nojima, MD, PhD 3,5 , Hyota Takamatsu, MD, PhD 2,3 , Daisuke Okuzaki, PhD 6 ,Takayoshi Morita, MD, PhD 2,3 , Takeshi Nakatani, MD 2,3 ,Yasuhiro Kato, MD, PhD 2,3 ,Yoshimitsu Nakanishi, MD 2,3 , Yu Futami, MD 2,3 , Yasuhiko Suga, MD 2,3 , Yujiro Naito, MD 2,3 , Hachiro Konaka, MD 2,3 , Shingo Satoh, MD 2,3 , Maiko Naito MD 2,3 , Mayuko Izumi, MD 2,3 , Sho Obata, MD 1,2,3 , Ayaka Nakatani, MD 1 , Takashi Shikina, MD, PhD 1,7 , Kazuya Takeda, MD, PhD 8 , Masaki Hayama, MD, PhD 1 , Hidenori Inohara, MD, PhD 1 and Atsushi Kumanogoh, MD, PhD 2,3,9,* (∔同等貢献、*責任著者)
1 大阪大学 大学院医学系研究科 耳鼻咽喉科・頭頸部外科学
2 大阪大学 大学院医学系研究科 呼吸器・免疫内科学
3 大阪大学 免疫学フロンティア研究センター 感染病態学
4 近畿中央病院 呼吸器内科
5 大阪大学 大学院医学系研究科 病態病理学
6 大阪大学 微生物病研究所附属 遺伝情報実験センター
7 市立池田病院 耳鼻いんこう科
8 大阪市立総合医療センター 耳鼻咽喉科
9 大阪大学 先導的学際研究機構
本研究は、JSPS科研費(18H05282、18K16146、16H06958)、国立研究開発法人日本医療研究開発機構(AMED)難治性疾患実用化研究事業(JP19ek0109307)、国立研究開発法人科学技術振興機構(JST)研究成果展開事業「センター・オブ・イノベーション(COI)プログラム」の支援によって行われました。
参考URL
大阪大学 大学院医学系研究科 呼吸器・免疫内科学
http://www.imed3.med.osaka-u.ac.jp/
