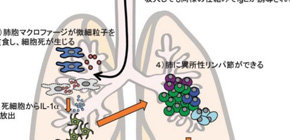
微細粒子の吸入によるアレルギー性炎症の発症機構を解明
PM2.5や黄砂によるアレルギー性炎症の新治療法開発に期待
本研究成果のポイント
・PM2.5や黄砂など大気中に存在する微細粒子 は免疫系を刺激する「アジュバント効果」を有しており、アレルギー性炎症を誘導・増悪することが示唆されていたが、その仕組みは明らかにされていなかった
・今回、肺に入った微細粒子が肺の掃除屋である肺胞マクロファージの細胞死を誘導し、IL-1アルファ の放出と異所性リンパ節の誘導を介して、アレルギーの原因因子の一つであるIgEが誘導されることを解明
・今後、肺胞マクロファージの細胞死を抑えたり、死細胞由来の免疫刺激物質を抑えたりすることで、微細粒子によるアレルギー性炎症発症の制御が可能
概要
大阪大学免疫学フロンティア研究センターの石井健特任教授(兼:医薬基盤・健康・栄養研究所上席研究員)および黒田悦史特任准教授(兼:医薬基盤・健康・栄養研究所客員研究員)らの研究グループは、微細粒子の吸入によるアレルギー性炎症の発症機構を解明しました (図1) 。
今後、微細粒子によって誘導される免疫刺激因子をコントロールすることによって、PM2.5や黄砂によって引き起こされるアレルギー性炎症の新規治療法の開発が期待されます。
本研究成果は、米国の科学雑誌『Immunity』(日本時間12月21日午前2時)にオンライン掲載されました。
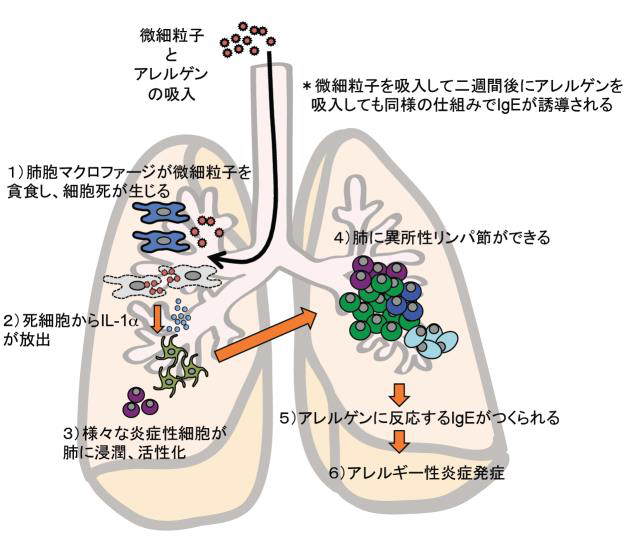
図1 微細粒子の吸入によるアレルギー性炎症の発症機構
研究の背景
アレルギー性疾患は先進国を中心に増加の一途をたどっており、その要因の一つとして大気中に浮遊する微細粒子(PM2.5、黄砂、ディーゼル粒子など)の関与が示唆されています。これまで多くの報告から、このような微細粒子は免疫を刺激するアジュバント効果を有しており、アレルギー因子のIgEを誘導しアレルギー性炎症を引き起こすことが示されていますが、その詳細は不明でした。
本研究の内容
PM2.5をはじめとする微細粒子は吸入されると気道の奥まで到達し、炎症反応を引き起こすことが報告されています。炎症反応への対応として、肺に常在する肺胞マクロファージが微細粒子を貪食し、体外へ排出させると考えられています。
そこで、マウスから回収した肺胞マクロファージを使って様々な種類の微細粒子を貪食させたところ、アレルギー性炎症を引き起こす微細粒子を貪食した際にのみ、肺胞マクロファージが細胞死を起こし、IL-1アルファという免疫刺激物質(サイトカイン)を放出することがわかりました。また微細粒子をマウスの肺に投与すると、肺の中でIL-1アルファが二週間にわたって肺に放出され続け、その間にアレルゲンを吸入することでIgEが誘導されることを認めました。
このことは、微細粒子を吸入した後は長期的にIL-1アルファの放出が続き、アレルゲンに感作されやすい状態が続いていることを示しています。また肺には異所性リンパ節といわれるリンパ組織が形成され、それがIgE誘導に関与する可能性が示唆されました。
本研究成果の意義
多くの研究において、PM2.5、黄砂、ディーゼル粒子などの大気中の微細粒子は免疫反応を活性化するアジュバント効果を有しており、アレルギー性炎症の発症に関与することが報告されていましたが、その仕組みに関しては不明のままでした。今回その仕組みが明らかになったことにより、微細粒子によるアレルギー性炎症、ひいては肺の炎症性疾患の予防や治療法につながることが期待されます。
本研究成果では幾つかの重要なことが明らかになりました。まず一つ目はすべての微細粒子がアレルギー性炎症を引き起こすわけではない点です。アレルギー性炎症を引き起こす粒子の特徴として、貪食によって肺胞マクロファージの細胞死を誘導し、その結果としてIL-1アルファが放出されるという点が挙げられます。実際にアレルギーを引き起こさない微細粒子では細胞死やIL-1アルファの誘導がなく、IgEの誘導が認められません。二つ目はIL-1アルファが長期間誘導される点です。これにより微細粒子に曝露された後、しばらくの間はアレルゲンに感作されやすい体の状態が続きます。すなわち、大気汚染がひどい地域で過ごした後に自宅に戻り、そこでダニなどのアレルゲンに感作され、アレルギー性疾患を発症する可能性があることを示しています。このように微細粒子によるアレルギー性炎症の仕組みを紐解いたことで、新しい予防あるいは治療戦略が期待されます (図2) 。
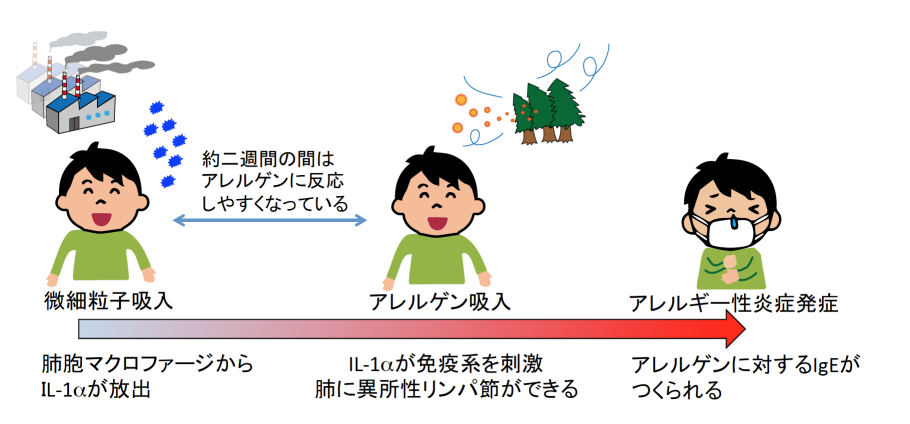
図2 微細粒子吸入後、しばらくはアレルゲンに感作されやすくなる
掲載論文・雑誌
著者:Etsushi Kuroda, Koji Ozasa, Burcu Temizoz, Keiichi Ohata, Christine X. Koo, Tomohiro Kanuma, Takato Kusakabe, Shingo Kobari, Masanori Horie, Yasuo Morimoto, Saeko Nakajima, Kenji Kabashima, Steven F. Zieglar, Yoichiro Iwakura, Wataru Ise, Tomohiro Kurosaki, Takahiro Nagatake, Jun Kunisawa, Naoki Takemura, Satoshi Uematsu, Masayuki Hayashi, Taiki Aoshi, Kouji Kobiyama, Cevayir Cobanand Ken J. Ishii
タイトル:Inhaled Fine Particles Induce Alveolar Macrophages Death and Interleukin 1a Release to Promote Inducible Bronchus-Associated Lymphoid Tissue Formation.
掲載紙:Immunity (日本時間12月21日午前2時オンライン掲載)
特記事項
本研究は、文部科学省イノベーションシステム整備事業地域イノベーション戦略支援プログラムの一環で行われました。また。公益財団法人持田記念医学薬学振興財団ならびに公益財団法人武田科学振興財団からの研究助成を受けております。
大阪大学免疫学フロンティア研究センター(IFReC)は、日本が科学技術の力で世界をリードしていくため「目に見える世界的研究拠点」の形成を目指す文部科学省の「世界トップレベル研究拠点プログラム(WPI)」に採択されています。
参考URL
免疫学フロンティア研究センター ワクチン学 石井健研究室
http://www.nibiohn.go.jp/adjuvant/index.html
研究の解説
研究の背景
先進国を中心にアレルギー性疾患は増加の一途をたどっています。そこには様々な因子が関与しており、環境因子もその一つです。近年では大気中の微細粒子(PM2.5、黄砂、ディーゼル粒子など)のアレルギー性疾患への関与が示唆されています。このような微粒子はそれ自体アレルゲンではなく、アレルゲンに対する免疫反応を増強させる作用を有していると考えられています。このような効果を「アジュバント効果」と言います。多くの研究報告から、大気中の微細粒子がアレルギー性炎症を誘導・増悪するアジュバント効果を有していることが明らかにされていますが、その詳細な仕組みは不明のままでした。
今回研究グループは、微細粒子を吸入することで、肺においてどのような免疫反応が生じているのかをマウスを用いたモデルで明らかにしました。
本研究成果の内容
PM2.5をはじめとする微細粒子は吸入されると気道の奥まで到達し、炎症反応を引き起こすことが報告されています。そのような粒子は肺に常在する肺胞マクロファージにより貪食され、体外へ排出されると考えられています。そこで、マウスから回収した肺胞マクロファージを使って様々な種類の微細粒子を貪食させたところ、アレルギー性炎症を引き起こす微細粒子(アルミニウム塩やシリカ)を貪食した時にだけ肺胞マクロファージが細胞死を起こし、細胞内に蓄積されているIL-1アルファというサイトカインを放出することがわかりました。そのような微細粒子(アルミニウム塩)をマウスの肺に投与すると、肺の中でIL-1アルファが二週間にわたって放出され続けることも明らかになりました (図3) 。さらに研究グループは、このような長期間のIL-1アルファの放出がアレルギー性炎症の発症に関与するか否かを調べました。微細粒子をマウスの肺に投与して3、7あるいは14日後にアレルゲン(卵白アルブミン)の吸入曝露を行ったところ、微細粒子を肺に投与して14日後にアレルゲンを曝露してもアレルゲン特異的なIgEの上昇が認められました (図4) 。この結果は、アレルギーを起こしやすい微細粒子を吸入すると、しばらくはアレルゲンに感作されやすく、アレルギー性炎症を発症しやすい体の状態になっていることを示しています。
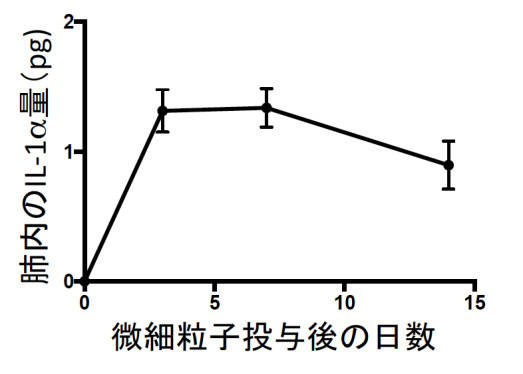
図3 微細粒子投与後の肺内のIL-1αの量の変動

図4 微細粒子投与後日数とアレルゲン曝露によるIgE誘導との関係
さらにこのような状態のマウスの肺を観察すると、肺に異所性リンパ節とよばれるリンパ組織が形成されており、このような組織がアレルギー性炎症の増悪に関与する可能性が示唆されました (図5) 。
一方で、アレルギー性炎症を引き起こさない微細粒子ではマクロファージの細胞死もIL-1アルファの放出も認められず、IgEの誘導も認められませんでした。この結果から、微細粒子を貪食した肺胞マクロファージの細胞死がアレルギー性炎症のトリガーになっていることが明らかになりました。
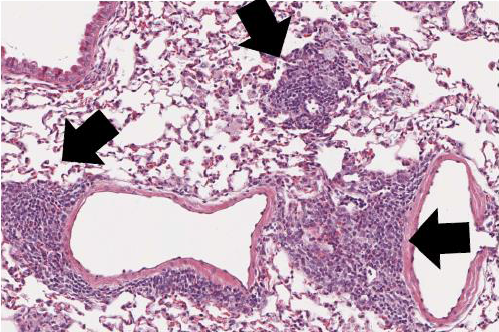
図5 微細粒子は肺内に異所性リンパ節を誘導する
本研究成果の意義
最近ではPM2.5をはじめとする微細粒子の人体への影響が懸念されています。疫学的な調査では大気中の微細粒子の増加によって小児喘息患者の発作のリスクが上昇するとの報告もあります。しかしながらなぜ微細粒子の吸入がアレルギー性炎症の発症や増悪に関与するのかについての詳細な仕組みは不明のままでした。今回の研究成果から、肺胞マクロファージの細胞死とIL-1アルファの放出が重要であることが明らかになり、微細粒子によって引き起こされるアレルギー性炎症に対する新しい予防および治療法の開発が期待されます。
さらに本研究成果から微細粒子が肺において長期にわたってIL-1アルファを誘導するため、微細粒子の曝露後はアレルゲンに感作されやすい体の状態が続くことも明らかになりました。これまで多くの報告から微細粒子とアレルゲンは同時期に曝露される必要があると考えられていましたが、微細粒子の曝露とアレルゲンの曝露に数日のズレがあってもアレルギー性炎症が発症すると考えられます。このような体の仕組みは、本来は病原体に対する効果的な防御反応の一つであったと考えられますが、現代社会においてはアレルギー性疾患という形で現れてきているのかもしれません。この結果から、微細粒子の曝露を受けた後の数日間はアレルゲン曝露への注意が必要と考えられます。
用語説明
- 微細粒子
大気中の微細粒子は気道の奥まで到達し、炎症反応を引き起こすことが示唆されている。実際に小児喘息患者では発作のリスクが大気中の微細粒子の増加によって上昇するとの報告がある。
- IL-1アルファ
IL-1アルファ(インターロイキン-1アルファ; interleukin-1α):
サイトカインと呼ばれる免疫担当細胞が産生され、炎症反応を誘導する免疫刺激因子の一つ。マクロファージをはじめ、さまざまな免疫担当細胞から産生される。
