多剤排出タンパク質の発現にブレーキを掛ける機構を解明!
細菌の抗菌薬抵抗性制御への戦略的治療へ光
リリース概要
大阪大学産業科学研究所の西野邦彦准教授らは、病原細菌サルモネラが抗菌性物質を感知して多剤耐性化の原因となる多剤排出タンパク質の発現抑制を解除するメカニズムを明らかにしました。サルモネラは代表的食中毒菌であり、食中毒は大型の事例が多く、様々な施設等で多発しています。特に近年、サルモネラでは複数の抗菌薬に耐性の「多剤耐性化」が問題となっています。
今回、サルモネラの多剤排出タンパク質の発現にブレーキをかける抑制タンパク質(リプレッサー)がデカリニウムをはじめとした5つの抗菌性物質を感知して、その抑制を解除するメカニズムを明らかにしました。本研究では、サルモネラ多剤排出タンパク質ブレーキ役のリプレッサータンパク質と抗菌性物質との共結晶構造決定に世界で初めて成功し、細菌の抗菌薬抵抗性制御の新たなメカニズムを明らかにしました。本成果は、多剤耐性菌感染症克服にも役立てられると期待されます。
研究の背景
複数の抗菌薬で治療することのできない多剤耐性の病原細菌による感染症流行は、人々の健康を脅かす存在です。細菌多剤耐性化の重要なメカニズムの一つとして、多剤排出タンパク質による抗菌薬の能動的排出があります。中でも、AcrAB多剤排出システムは、グラム陰性菌において、細菌の獲得耐性と自然耐性の両方に関係している因子として注目されています。
細菌では、多剤排出タンパク質をコードしている遺伝子の多くが、アクセル役のアクチベータータンパク質とブレーキ役のリプレッサータンパク質によって、その発現がコントロールされています。サルモネラ、エンテロバクターやクレブシエラといった病原細菌においては、AcrABのアクチベータータンパク質としてRamAが存在しています。また、最近の研究により、その上流に、このアクチベーター発現を抑制するリップレッサータンパク質RamRが存在することが分かっていました( 図1 )。
これまでに、臨床から分離された多剤耐性病原細菌の解析から、ブレーキ役であるRamRが破壊されると、細菌の多剤排出活性が促進され、RamRは病原細菌の抗菌薬抵抗性を制御する重要な因子であることが分かっていました。しかしながら、抗菌薬抵抗性のブレーキ役を担っているRamRがどのような構造をしており、また、ブレーキがどういった時に解除されるのかは、分かっていませんでした。
今回、本研究により、RamRタンパク質の結晶構造が明らかになりました。RamRタンパク質は、DNA結合領域と抗菌性物質を認識する領域から構成されています( 図2 )。スクリーニングの結果、デカリニウム(消毒剤)をはじめとして、ベルベリン、クリスタルバイオレット、臭化エチジウム、ローダミン6Gといった抗菌性物質がRamRタンパク質に結合することが分かり、これら化合物とRamRタンパク質の共結晶構造を解くことにも成功しました( 図3 )。各抗菌性物質は、RamRタンパク質の異なるアミノ酸の組み合わせによって、マルチサイト結合を介して認識されていることが分かりました。病原細菌は、抗菌性物質が無い状況では、ブレーキ役のRamRタンパク質がDNAに結合して、多剤排出タンパク質AcrABのアクチベーターRamAの発現を抑制しています。しかしながら、細菌が抗菌性物質に曝されることにより、RamRタンパク質がこれら物質を認識して、ブレーキを解除し、多剤排出活性が促進されるという病原細菌の新たな抗菌薬抵抗性メカニズムが明らかになりました。
本研究成果が社会に与える影響(本研究成果の意義)
本研究により、病原細菌が複数の抗菌性物質に順応し、薬剤抵抗性を誘導する新たなメカニズムが明らかになりました。本成果は、細菌の抗菌薬抵抗性機構の理解を深めるものであり、将来、多剤耐性菌による感染症を克服する新たな治療戦略にもつながることが期待されます。
特記事項
本研究成果は英国Nature Publishing Groupの「Nature Communications」のオンライン速報版で6月26日(英国時間10時、日本時間18時)に公開されます。
論文タイトル: The crystal structure of multidrug-resistance regulator RamR with multiple drugs(多剤耐性制御因子RamRと複数の薬剤との共結晶構造)
著者: Yamasaki S., Nikaido E., Nakashima R., Sakurai K., Fujiwara D., Fujii I. and Nishino K.
山崎優1、二階堂英司1、中島良介1、櫻井啓介1、藤原大佑2、藤井郁雄2、西野邦彦1
(1大阪大学産業科学研究所、2大阪府立大学大学院理学系研究科)
本研究は最先端・次世代研究開発支援プログラム「薬剤排出ポンプによる細菌多剤耐性化・病原性発現制御機構の解明と新規治療法開発」(研究代表者:西野邦彦准教授、研究期間:平成23年2月〜現在[平成26年3月終了予定])の助成によりなされたものです。
参考図
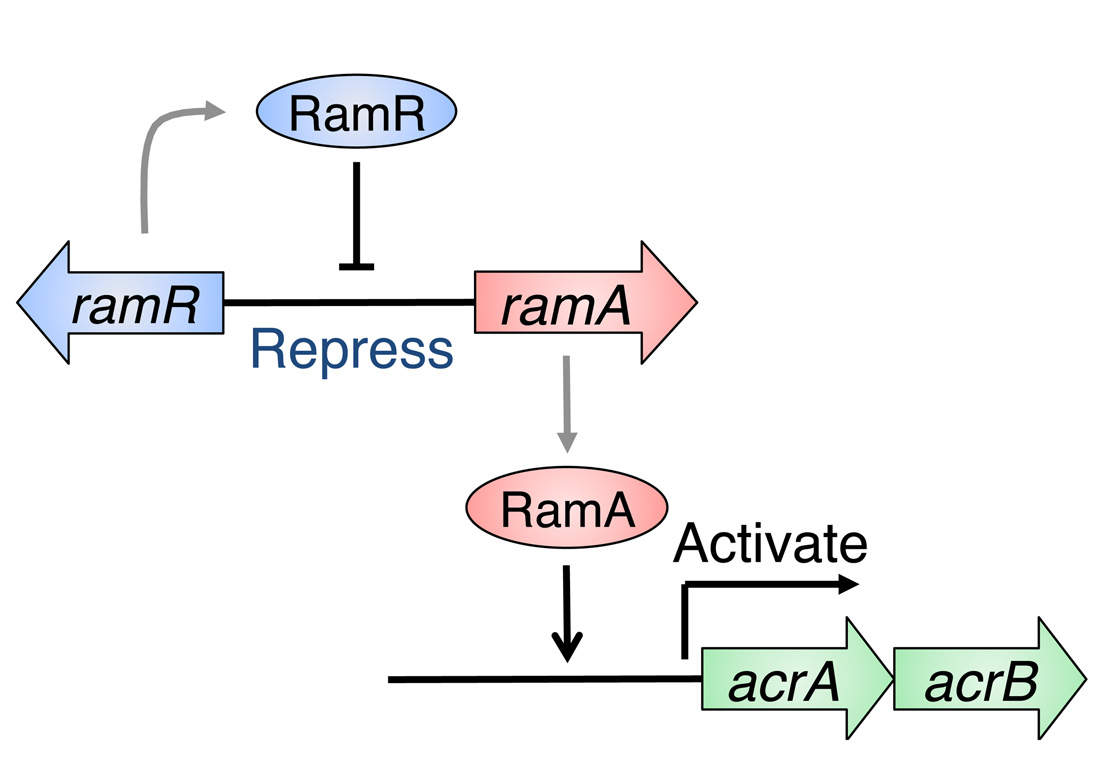
図1 病原細菌サルモネラの薬剤抵抗性制御ネットワーク
多剤排出タンパク質遺伝子acrABは、アクチベータータンパク質(アクセル役)RamAと、リプレッサータンパク質(ブレーキ役)RamRによって、その発現がコントロールされている.
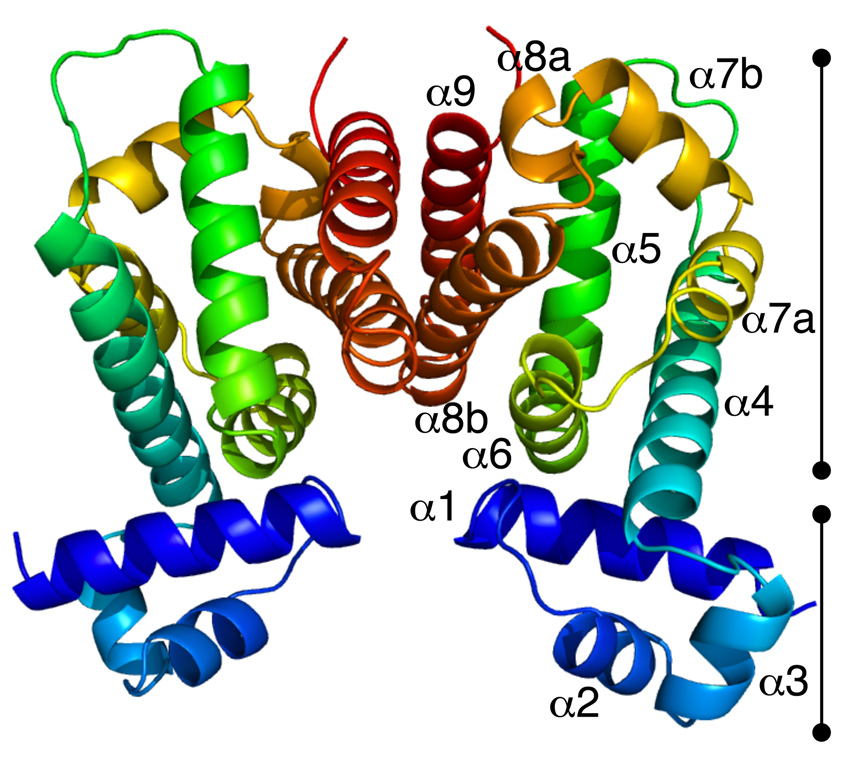
図2 RamRタンパク質の構造
抗菌薬抵抗性制御のブレーキ役を担うRamRタンパク質は、DNA結合ドメイン(下部)と抗菌性物質認識ドメイン(上部)から構成されている.
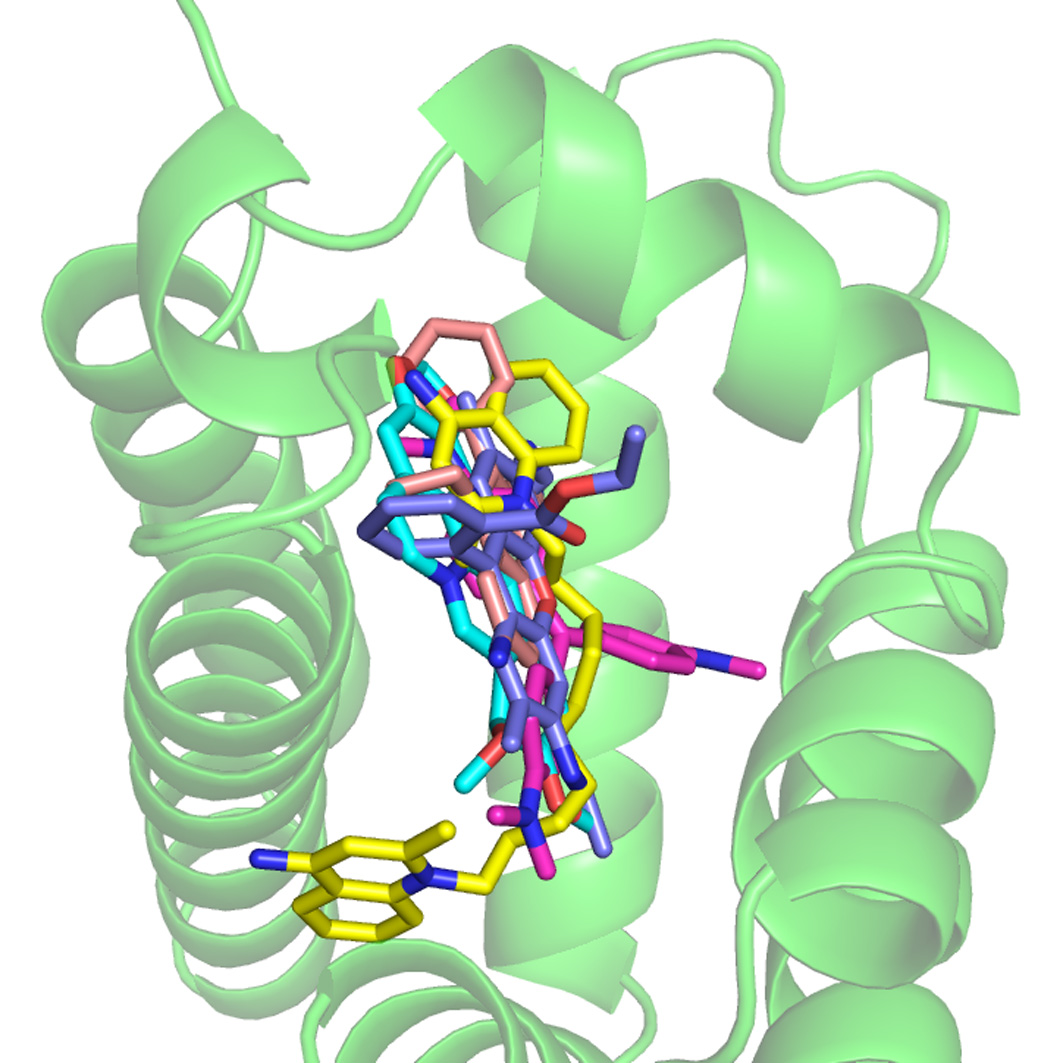
図3 RamRタンパク質と多剤(複数の抗菌性物質)との共結晶構造
RamRタンパク質はマルチサイト結合により複数の化合物を認識する.
参考URL
大阪大学 産業科学研究所 感染制御学研究分野
http://www.sanken.osaka-u.ac.jp/jp/organization/srp/srp_02_01.html
