制御性T細胞発生に関わる重要なタンパク質を同定
自己免疫疾患やアレルギーの治療に光
本研究成果のポイント
・制御性T細胞のマスター転写因子 がFoxp3であることは同定されていたが、どのようにFoxp3が発現し制御性T細胞が発生するかは不明だった
・今回、ゲノムオーガナイザーSatb1によるエピゲノム の成立が制御性T細胞の発生に関わっていることを解明
・今後、本メカニズムを更に研究することで、自己免疫疾患やアレルギーの病因を理解し、これらの疾患を根本的に治療することが可能に
リリース概要
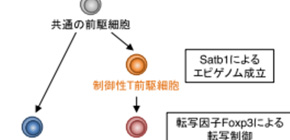
大阪大学免疫学フロンティア研究センターの坂口志文特任教授(常勤)らの研究グループは、ゲノムオーガナイザーSatb1による制御性T細胞発生のメカニズムを解明しました (図) 。
制御性T細胞発生メカニズムを把握すれば、自己免疫疾患やアレルギーの病因を理解し、これらの疾患を根本的に治療することが可能になります。
本研究成果は、英国科学雑誌『Nature Immunology』(日本時間12月20日(火)午前1時)にオンライン掲載されました。
図 制御性T細胞発生メカニズム
研究の背景
1980年代に坂口志文特任教授(常勤)は制御性T細胞を発見し、これらが自己免疫疾患、アレルギーなどの免疫疾患防止に必須であることを明らかにしました。2003年には同グループが制御性T細胞のマスター転写因子としてFoxp3を同定しました。免疫制御に必須な細胞として制御性T細胞の研究はその後さらに盛んになり、Foxp3による転写制御などについて多くのグループが研究を進めましたが、どのようにFoxp3が発現し制御性T細胞が発生するかは不明でした。
本研究の内容
制御性T細胞のほとんどは幼少期に胸腺で発生します。研究グループは、核内分子Satb1によるエピゲノムの成立が、制御性T細胞の発生に関わっていることを、マウスを用いた実験で明らかにしました。Satb1欠損マウスモデルでは胸腺での制御性T細胞の発生に障害が起き、多臓器で自己免疫疾患が観察されました。これらの結果から、制御性T細胞発生期のエピゲノム成立と自己免疫疾患のつながりが明らかになりました。
本研究成果の意義
これまでの研究から自己免疫疾患やアレルギーには制御性T細胞による免疫制御の異常が関連している可能性が考えられます。しかし、実際に制御性T細胞の減少や異常が観察されている疾患はごく僅かです。今回得られた知見から、制御性T細胞発生期の異常により、特定の制御性T細胞の減少、発生の遅れなどが原因で免疫疾患が起こることが考えられます。実際、ヒトのSatb1遺伝子付近の突然変異は自己免疫疾患と関連があります。これら病因の理解はより効果的な治療法模索に役立つと期待できます。
また本研究成果は、制御性T細胞を用いた免疫細胞療法にも役立つことが考えられます。通常のT細胞を制御性T細胞に分化させ細胞療法に用いると自己免疫疾患やアレルギーの抑制に効果的であることが期待されますが、現時点で安定した制御性T細胞を試験管内で作製することは難しいです。本研究で示した制御性T細胞発生初期のエピゲノム成立は、そのような試験管内での制御性T細胞作製の指標となると期待されます。
掲載論文・雑誌
著者:Yohko Kitagawa, Naganari Ohkura, Yujiro Kidani, Alexis Vandenbon, et al.
タイトル:Guidance of regulatory T cell development by Satb1-dependent super-enhancer establishment
掲載誌:Nature Immunology
日本時間12月20日(火)午前1時オンライン掲載
特記事項
本研究課題は、国立研究開発法人日本医療研究開発機構(AMED)、革新的先端研究開発支援事業(AMED-CREST)の研究開発領域「炎症の慢性化機構の解明と制御に向けた基盤技術の創出」(研究開発総括:宮坂昌之)における研究開発課題「制御性T細胞による慢性炎症制御技術の開発」(研究開発代表者:坂口志文)の一環で行われました。大阪大学免疫学フロンティア研究センター(IFReC)は、日本が科学技術の力で世界をリードしていくため「目に見える世界的研究拠点」の形成を目指す文部科学省の「世界トップレベル研究拠点プログラム(WPI)」に採択されています。
研究の解説
研究の背景
制御性T細胞は過剰な免疫反応を抑えるのに必須な細胞です。制御性T細胞の欠損または異常は致命的な自己免疫疾患やアレルギーを引き起こします。また、制御性T細胞は移植された臓器の拒絶防止に貢献します。このような疾患との関わりから、制御性T細胞を増やすと治療に役立つことが期待されています。そのためには制御性T細胞がどのように発生するのかを理解することが必要です。
1980年代に坂口志文教授が制御性T細胞を発見して以来、この細胞の機能、分化について多くのグループが研究を進めてきました。2003年には同グループが制御性T細胞のマスター転写因子としてFoxp3を同定しました。その後、Foxp3による転写制御などについて研究が進みましたが、どのようにFoxp3が発現し制御性T細胞が発生するかは不明でした。
本研究成果の内容
本研究では、制御性T細胞発生時にFoxp3が発現する前に何が起こるか、すなわちどのように制御性T細胞の分化が引き起こされるかということに焦点を置きました。発生段階のエピゲノムの変化を網羅的に調べた結果、制御性T細胞特異的なスーパーエンハンサー領域の活性化が制御性T細胞前駆細胞でFoxp3が発現する前に起こることが明らかになりました。さらに、この現象に必要な分子としてゲノムオーガナイザーSatb1を同定しました。Satb1欠損マウスでは制御性T細胞の胸腺での発生が顕著に減り、様々な臓器で自己免疫反応による炎症が起こりました (図1) 。
これらの結果からSatb1によるエピゲノム成立は胸腺での制御性T細胞発生において現時点で最も初期のイベントであり、後に制御性T細胞の転写制御を担うFoxp3の発現に必須であることが明らかになりました (図2) 。Satb1は細胞を制御性T細胞に分化できるように整えることから、制御性T細胞発生のパイオニア因子の一つであると考えられます。
図1 Satb1欠損マウスの制御性T細胞発生異常と自己免疫疾患
図2 制御性T細胞発生メカニズム
本研究成果の意義
本研究で明らかになった制御性T細胞発生メカニズムは、制御性T細胞を用いた免疫細胞療法に役立つことと考えられます。通常のT細胞を制御性T細胞に分化させ細胞療法に用いると自己免疫疾患やアレルギーの抑制に効果的であることが期待されますが、現時点で安定した制御性T細胞を試験管内で作製することは難しいです。本研究で示した制御性T細胞発生初期のエピゲノム成立は、そのような試験管内での制御性T細胞作製の指標となると期待されます。
また、本研究により、制御性T細胞発生初期の異常は免疫疾患に繋がる可能性が考えられます。実際、ヒトのSatb1遺伝子付近の突然変異は自己免疫疾患と関連があります。これら病因の理解はより効果的な治療法模索に役立つと期待できます。
参考URL
大阪大学免疫学フロンティア研究センター(IFReC)HP
http://www.ifrec.osaka-u.ac.jp/jpn/
用語説明
- マスター転写因子
転写因子とは遺伝子発現をコントロールするタンパク質で、どのような転写因子が出ているかによりどのような細胞になるかが決まる。マスター転写因子はその中でも一番重要とされ、細胞のアイデンティティーを決める。
- エピゲノム
遺伝子配列はすべての細胞で同じであるが、細胞によって違ったパターンのマークが配列につく。このようなパターンをエピゲノムと呼ぶ。転写因子はこのようなマークを認識して遺伝子発現コントロールを行う。
