自己免疫性関節炎の発症・慢性化の原因となる 新たな細胞群と炎症ネットワークメカニズムの発見
研究成果のポイント
・TNFやIL-6阻害剤などの新しい抗リウマチ薬の登場により、関節リウマチ患者のQOLは劇的に改善したが、いまだに30%の関節リウマチ患者の治療は難しく、新たな治療法開発が待たれている。
・今回、関節炎発症、増悪に関わり、炎症滑膜組織に存在するGM-CSF 産生自然リンパ球を新たに発見した。また、インターロイキン-17(IL-17)を産生する炎症性T細胞(Th17)が関節炎発症期、慢性炎症期に、他の炎症性細胞と炎症性ネットワークを形成することで関節炎を増悪させる仕組みを明らかにした。
・本研究で得られた炎症ネットワークを標的とすることで、新しい免疫治療法の開発が期待できる。
概要
これまで関節リウマチの発症・慢性化に関わる要因について詳しく分かっておらず、新規治療法の開発のためには、これらの詳細な分子機構の理解が必要です。大阪大学免疫学フロンティア研究センターの廣田圭司招へい准教授(兼京都大学ウイルス・再生医科学研究所准教授)、坂口志文特任教授(常勤)らは、関節リウマチの臨床検体とそのマウスモデルを用い、自己免疫性関節炎を引き起こす炎症性T細胞が、関節炎の発症および慢性化維持に関わる新たな仕組みを明らかにしました。インターロイキン-17を産生する炎症性T細胞が、関節滑膜組織において、滑膜細胞および新しく見出した自然リンパ球と炎症ネットワークを形成することで、関節炎の発症および増悪に寄与していました。現在の抗リウマチ薬に対して応答性が低い患者群が存在することから、本研究で得られた炎症ネットワークを標的とすることで、新しい免疫治療法の開発が期待できます。
本研究成果は、国際科学雑誌「Immunity」のオンライン版(日本時間5月23日(水)午前1時)に掲載されました。
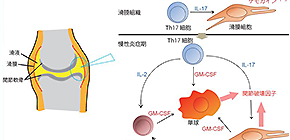
図1 本研究で得られた炎症のメカニズム
関節炎発症期には、Th17細胞の産生するIL17が、滑膜細胞からの炎症性サイトカイン とケモカイン の産生に重要である。特にGMCSFの産生が関節炎発症に大きな役割を果たす。慢性炎症期では、Th17細胞、滑膜細胞、自然リンパ球による細胞間および、炎症性サイトカインによる炎症ネットワークの形成が関節破壊を引き起こす。
研究の背景
関節リウマチは日本で約70万人の患者がおり、一年に1万人以上が新しく発症しています。病態は、全身性の炎症性疾患で、関節の腫脹を特徴とします。関節炎が起きた箇所にはさまざまな免疫細胞が集まり、正常なコントロールを失った炎症性の免疫細胞および滑膜細胞によって関節が破壊されます。最近、TNF阻害剤などの新しい抗リウマチ薬の登場によって、関節リウマチ患者の治療効果は大きく改善してきました。しかし、30%の関節リウマチ患者はこれらの治療に対する効果が低く、新しい免疫治療法の開発が待たれています。本研究プロジェクトでは、関節炎が起きた箇所の細胞群と炎症性サイトカインが新しい免疫治療法の標的となりうることに着目し、自己免疫性関節炎を引き起こす炎症性T細胞との細胞間の、および炎症性サイトカインとの炎症ネットワークを形成する因子を探索しました。
研究手法
坂口特任教授(常勤)らの開発した関節リウマチのモデルマウスと炎症性サイトカインGM-CSF(顆粒球単球コロニー刺激因子)欠損マウスを用いて、炎症滑膜組織に集まる免疫細胞を選別し、フローサイトメトリー(蛍光抗体を使った免疫細胞解析・分取装置)を用いて解析しました。また、取り分けた自然リンパ球および滑膜細胞の遺伝子の発現を解析し、GM-CSFが産生される条件とともに検討しました。次に、関節リウマチ患者の末梢血および滑膜液サンプルに含まれるGM-CSFを産生する自然リンパ球のフローサイトメトリー解析をおこない、ヒト関節リウマチの病因としての意義を検討しました。
本研究の成果
関節炎が起きた箇所に存在するGM-CSF産生細胞は、炎症性Tヘルパー(Th17)細胞、滑膜細胞であることを見いだしました。加えて、これまで知られていなかった免疫細胞としてGM-CSFを産生する自然リンパ球を発見しました。
関節炎発症期には、Th17細胞の産生するインターロイキン-17(IL-17)が、滑膜細胞からの炎症性サイトカインとケモカインの産生に重要であり、特に滑膜細胞のGM-CSFの産生が関節炎発症に重要な因子であることを明らかにしました。慢性炎症期においては、Th17細胞、滑膜細胞、自然リンパ球による細胞間および、炎症性サイトカインによる炎症ネットワークを形成し、それぞれの細胞から産生されたGM-CSFが単球細胞に作用することにより関節破壊に向かうことを示しました。
また、GM-CSFを産生する制御の仕組みは、それぞれの細胞によって異なることを明らかにしました。すなわち、Th17細胞は、関節炎が起きた箇所に存在する自己抗原に反応してGM-CSFを産生すること、滑膜細胞はTh17細胞から産生されたIL-17に反応しGM-CSFを産生すること、そして、自然リンパ球はTh17細胞から産生されたインターロイキン-2(IL-2)と傷害を受けた滑膜細胞から放出されるインターロイキン-33(IL-33)の共刺激に反応して多量のGM-CSFを産生することを示しました。
それぞれの細胞のGM-CSFだけを欠損させることによって、関節炎発症を有意に予防でき、GM-CSFが関節炎の発症・増悪化に重要な炎症性サイトカインであることを明らかにしました。また、関節リウマチ患者の滑膜液中にも、GM-CSFを産生する自然リンパ球が増加していることを示しました。これらの知見により、これまで不明であった関節リウマチの発症・慢性化の分子メカニズムの一端を明らかにすることができました。
本研究プロジェクトで見出した炎症ネットワーク形成に関わる細胞群、炎症性サイトカインを標的とすることによって、関節リウマチに対する新しい免疫療法の開発に結びつくことが期待されます。
今後の課題と期待
現在の抗リウマチ薬は炎症を抑制する対症療法で、そのため継続的な薬剤投与が必要です。関節リウマチの病態の中心は、コントロールを失った炎症性の免疫細胞で、これらの細胞を正常化するための免疫療法の開発は、疾患を根治することができる治療法となる可能性があります。今回明らかにされた炎症ネットワークを標的とした新しい免疫療法開発は、現在の抗リウマチ薬に反応性が低い患者群(30%のリウマチ患者)に対する有効な治療法となり得ます。
論文情報
タイトル:"Autoimmune Th17 Cells Induced Synovial Stromal and Innate Lymphoid Cell Secretion of the Cytokine GMCSFto Initiate and Augment Autoimmune Arthritis"
著者名: Keiji Hirota, Motomu Hashimoto, Yoshinaga Ito, Mayumi Matsuura, Hiromu Ito, Masao Tanaka, Hitomi Watanabe,Gen Kondoh, Atsushi Tanaka, Keiko Yasuda, Manfred Kopf, Alexandre J Potocnik, Brigitta Stockinger, Noriko Sakaguchi, Shimon Sakaguchi
本研究成果は、2018年5月23日(水)午前1時(日本時間)に米国科学誌「Immunity」のオンライン版で公開されました。
特記事項
本研究は、科学技術振興機構(JST)戦略的創造研究推進事業CREST「制御性T細胞による慢性炎症制御技術の開発(研究代表者:坂口志文)」、文部科学省科学研究費補助金「制御性T細胞による免疫応答制御の包括的研究(研究代表者:坂口志文)」、「炎症組織Th17細胞を起点とした炎症ネットワーク形成の分子基盤(研究代表者:廣田圭司)」、武田科学振興財団医学系研究奨励「炎症性Tヘルパー細胞と自然リンパ球細胞(ILCs)の炎症局所におけるクロストーク(研究者:廣田圭司)」の支援を受けて行われました。また、関節リウマチ患者の臨床検体を用いた解析は、京都大学医学部附属病院リウマチセンターとの共同研究プロジェクトであり、京都大学医学部附属病院医の倫理委員会の承認を得ています。
また本研究は、京都大学医学部附属病院リウマチセンター、スイス・チューリッヒ工科大学、英国フランシス・クリック研究所、英国エジンバラ大学と共同で行われました。
参考URL
大阪大学 免疫学フロンティア研究センター 実験免疫学研究室
http://www.ifrec.osaka-u.ac.jp/jpn/laboratory/shimon_sakaguchi/
用語説明
- GM-CSF
GM-CSF(Granulocyte Macrophage colony-stimulating Factor:顆粒球単球コロニー刺激因子)は、骨髄幹細胞に働き白血球分化を促す液性因子(サイトカイン)の一種です。古くから造血性のサイトカインとして知られていましたが、最近では様々な自己免疫疾患の発症に関わる炎症性サイトカインとして注目されています。
- 炎症性サイトカイン
サイトカインの中でも、炎症反応を引き起こすサイトカインを炎症性サイトカインといいます。具体的には、インターロイキン-6、インターロイキン-17、GM-CSF、腫瘍壊死因子(TNF)、などが知られていて、自己免疫疾患を含む難病の炎症病態に関わっていることが明らかになってきました。近年、これらの液性因子を標的とした抗体医薬の開発が進められています。
- ケモカイン
免疫細胞を引き寄せる役割を担う液性因子。炎症が起きている組織、細胞からは様々なケモカインが産生されていて、体中を循環中の免疫細胞を引き寄せます。このメカニズムで炎症組織、感染組織、がん組織に免疫細胞を集め、様々な免疫反応を起こします。
