患者の視力を取り戻せ。
角膜上皮細胞シート移植、そして眼球の再現へ。
医学系研究科・教授・西田幸二
ⅰPS細胞(人工多能性幹細胞)で角膜上皮細胞シートを作り、角膜に疾患のある患者さんへの移植を世界で初めて行った西田幸二教授。これまでに、ⅰPS細胞を使い眼を構成するそれぞれの細胞の発生を二次元で再現することにも世界で初めて成功している。さらに血管内皮幹細胞の発見など、数々の世界的な成果を挙げているが、「大きな目標を設定したことはない。目の前の課題を一つ一つ解決するために日々努力するタイプ」と話す。

口腔粘膜が取り組みのスタート
西田教授は、眼科医として角膜移植に取り組んできた。だが、他人の角膜の移植は拒絶反応が問題になるうえ、そもそも国内ではドナー(提供者)が不足している。
そこで2000年ごろから患者自身の細胞を利用した再生医療の研究を始めた。ターゲットとして選んだのは患者自身の口腔粘膜だ。発生学的にみると、角膜の上皮と口腔粘膜の組織はよく似ている。その上、口の中の細胞なら採取しやすいことも大きな利点となる。患者本人の口腔粘膜組織から幹細胞を採取、培養してシート化し、これを移植すれば本人の組織なので拒絶反応は起こらない。そして2004年に、口腔粘膜から作った角膜上皮代用物の世界初の移植について発表した。視力0.01未満の患者さんが0.9まで回復するなど、これまでに素晴らしい実績を残している。現在、医師主導治験も終わり、間もなくシートの製造販売承認が得られる段階まで到達した。
だが、口腔粘膜から作った上皮細胞のシートには「限界」があることもわかった。
「口腔粘膜の細胞シートは、確かに角膜上皮の代用にはなります。しかし、やはり角膜上皮そのものではないのです」。構造が角膜上皮にそっくりでも、口腔粘膜の性質はひそんでいる。そのため、角膜上皮とは性質の異なるところがあり、血管が発生して角膜が濁り、再び視力の低下につながるケースがあるのだ。
「角膜上皮そのものが必要だ」。そこで浮上したのが、ⅰPS細胞の利用だった。
衝撃のⅰPS細胞との出会い

西田教授は、ⅰPS細胞について初めて聞いた時の衝撃を今でもはっきりと記憶している。
京都大学の山中伸弥教授がマウスのⅰPS細胞の論文をまとめた2006年、その論文が一般に発表される数ヶ月前に、50~60人ほどが集まったクローズの研究会だった。山中教授がマウスの細胞からⅰPS細胞を作製したことを報告した。「これはすごい、ノーベル賞を取る研究だ」と衝撃を受けた。既によく知られているとおり、ⅰPS細胞は体細胞を初期化し、あらゆる細胞に分化できる能力を持たせた幹細胞だ。山中教授は07年にヒトの細胞からもⅰPS細胞の作製に成功し、実際に12年、ノーベル生理学・医学賞を受賞することになる。
「細胞の分化を戻す、初期化できるなんて普通は考えられない。驚きました」。しかし研究会の会場内は落ち着いていた。その場で聴いている研究者たちを見渡して「もっと騒いでもいいのではないかと、思った」と振り返る。「衝撃と驚きが大き過ぎて、ほとんどの人がそれを表現できなかったのかもしれません。実は、僕もそうでした」
西田教授はその後すぐに山中教授にメールを送り、ⅰPS細胞を提供してもらえるよう依頼した。ⅰPS細胞を利用して、患者さん由来の細胞で角膜移植が可能になれば、拒絶反応の問題もクリアできる。ⅰPS細胞から角膜上皮細胞を作る研究のスタートだった。
目の細胞群「SEAM」を作製、角膜上皮の移植へ
西田教授らが2016年にネイチャーに発表した成果が、世界を驚かせた。ⅰPS細胞を使って眼の後部から前部にかけての各種の細胞を規則正しく発生させ、層構造にすることに成功したのだ。
同心円状の4層の細胞群で、SEAM(self-formed ectodermal autonomous multi-zone)と名付けた。神経網膜や網膜色素上皮が2層目に、水晶体が2層目と3層目の間、角膜上皮が3層目に、4層目には目の表面の皮膚や上皮細胞が出現した。つまり、目の後ろから前にかけての細胞が順番にそろっているのだ。二次元ではあるが、眼全体の発生を再現しており、三次元にすることができれば眼そのものになり得る。
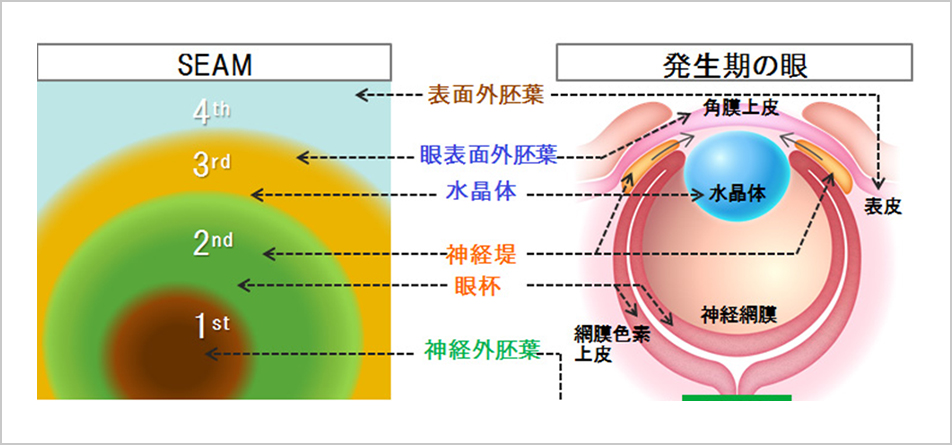
西田教授らは3層目に出現した角膜上皮の前駆細胞を単離、培養し、シート状に組織化する一連の技術も開発した。そして遂に2019年7月、完成させた厚さ0.05ミリ、直径約35ミリの角膜上皮細胞シートを、患者さんへ移植した。角膜と同じたんぱく質が発現していることも確認でき、ヒトの角膜上皮と同様であるということも証明できた。
今後は22年3月までに4人の患者さんに移植をして安全性と有効性を検証し、治験を経て25年ごろに保険適用の承認を得たいと考えている。
オルガノイド研究へ
二次元の「眼」ともいえるSEAMは、オルガノイドに近いコンセプトを持つ成果だ。オルガノイドとは、ⅰPS細胞などから分化誘導した三次元の器官で、生体でみられるような構造や機能を持つ、いわば「ミニ臓器」ともいえるもの。
「ⅰPS細胞やES細胞(胚性幹細胞)を使った従来の研究は、各種の細胞にどう分化させるかという方法を探求するものでした。しかし最近は、単なる細胞ではなく、オルガノイドを作る研究にシフトしてきました」と西田教授は研究のトレンドを説明する。そして、こう付け加えた。「SEAMの研究でいろいろな知見を得たので、いつか眼球そのものを作れればと思っています」
とはいえ、眼球を作るにはまだまだハードルがある。その理由は、眼球が多くの種類の細胞で構成された複雑な器官だからだ。神経細胞である網膜、皮膚に近い角膜や水晶体などいろいろな組織でできている。むしろ、神経細胞だけでできている脳や、肝細胞で構成されている肝臓などのほうが再現しやすいと考えられている。
未知の発見を求めて

ⅰPS細胞を使った研究のほかに、西田教授は、阪大微生物病研究所の髙倉伸幸教授らとの共同研究で、損傷した血管を修復する役割を持つ血管内皮の幹細胞を発見した。血管中のごく一部の特殊な細胞が、CD157という分子を発現していることを突き止め、これが傷ついた血管を再生させる幹細胞だということが分かった。
失明につながる糖尿病網膜症や加齢黄斑変性といった病気は、網膜に不要な血管ができることが要因。これらの病気で新しくできた血管は、正常な血管と違って脆弱で、いろいろな成分が漏れ出して症状を起こす。
西田教授は、網膜のどの部位に血管内皮の幹細胞があるのかを解明し、不要な血管が新生するメカニズムを研究することで、新しい治療法につなげることを目指している。
研究、教育、診療、教室運営……といった大学教授としての各種の仕事の中で、西田教授が一番大切にしているのは「研究」だと言い切る。
「研究のモチベーションとなるのは、未知のものを発見する喜びです。そして、研究が結果的に社会実装につながるとすれば、それは非常に幸運なことと思います」
西田教授にとって研究とは
次の世代につなげていく『バトン』です。一つの世代で発見できることは限界があり、評価も難しい。研究の成果は、次の世代につないでいって、長い歴史の中で評価されるべきです。そして、私個人にとって研究は『ライフワーク』でもあります。
●西田 幸二(にしだ こうじ)
大阪大学大学院医学系研究科 教授
1988年大阪大学医学部卒業、医学博士。大阪厚生年金病院などを経て、2000年大阪大学大学院医学系研究科助手、06年東北大学大学院医学系研究科 教授。10年より現職。

■ 再生医療をはじめ人のもつ再生の機能に迫る研究者たちの物語「再生の医学~“志”のスペシャリテ6選~」を引き続きお楽しみください。
再生の医学~“志”のスペシャリテ6選~ #1 医学系研究科 教授 澤 芳樹
再生の医学~“志”のスペシャリテ6選~ #2 医学系研究科 教授 西田 幸二
患者の視力を取り戻せ。角膜上皮細胞シート移植、そして眼球の再現へ。
再生の医学~“志”のスペシャリテ6選~ #3 工学研究科 教授 紀ノ岡 正博
再生の医学~“志”のスペシャリテ6選~ #4 歯学研究科 教授 村上 伸也
再生の医学~“志”のスペシャリテ6選~ #5 医学系研究科 寄附講座教授 玉井 克人
再生の医学~“志”のスペシャリテ6選~ #6 医学系研究科 教授 加藤 和人
(2019年12月取材)
