インターフェロンの過剰産生により生じる 脳症の発症メカニズムを解明
エカルディー・グティエール症候群 (AGS)の治療法確立への期待
研究成果のポイント
- 先天性自己炎症性疾患AGSのモデルマウスを用いて、主症状である脳症の形成メカニズムを解明
- 脳内で1型インターフェロン (IFN)を過剰産生する細胞群を同定し、脳室内にたまったIFNが脳症形成に不可欠であることを証明
- 脳内の1型IFNシグナル経路を遮断することでAGSの治療法が確立されることに期待
概要
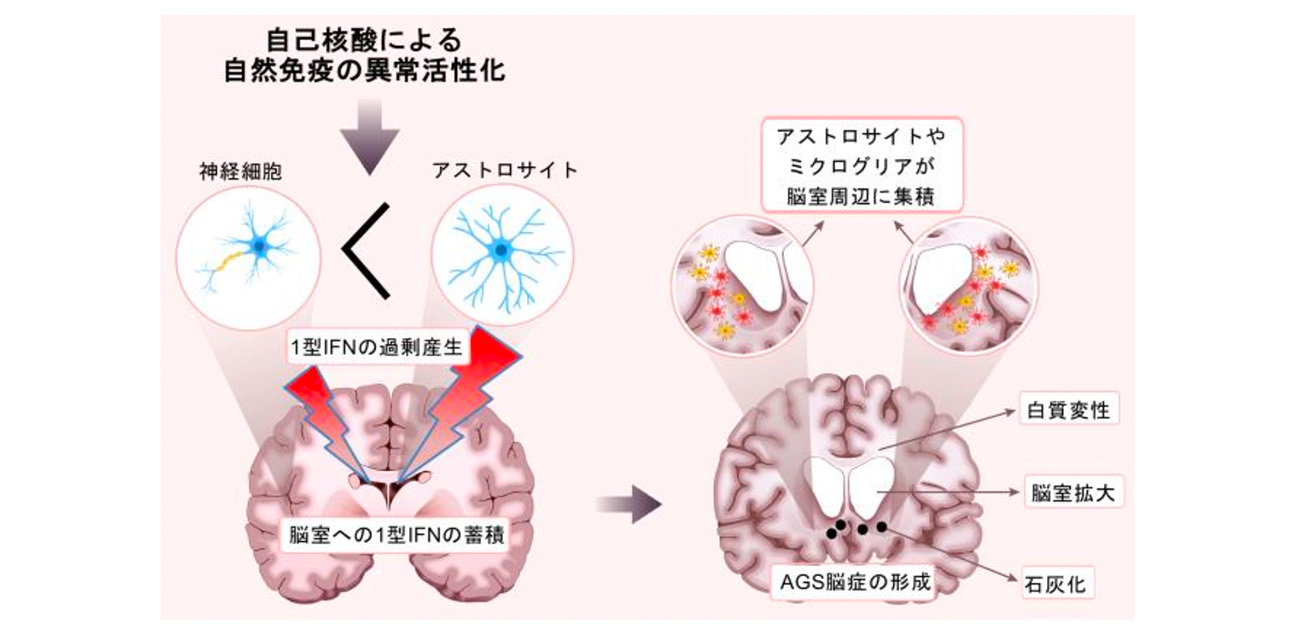
大阪大学大学院生命機能研究科のHyebin Yooさん (博士後期課程)、医学系研究科の中濱泰祐助教 (生命機能研究科兼任、創発研究者)、河原行郎教授 (生命機能研究科兼任)らの研究グループは、先天性自己炎症性疾患エカルディー・グティエール症候群 (AGS) の主症状である脳症が、脳室内に蓄積した1型インターフェロン (IFN)によって形成されることを世界で初めて明らかにしました (図1)。また、1型IFNが脳内のアストロサイトや神経細胞から過剰産生されることを突きとめました。
AGSでは、1型IFNが過剰産生されることが知られていますが、これが主症状である脳症形成に関係するのかどうか、またどの細胞群から産生されてくるのか、長年不明でした。
研究グループは、2021年にAGS脳症を再現するモデルマウスの開発に成功し (Nakahama et al, Immunity, 2021)、このマウスを詳細に解析することで1型IFNを過剰産生する細胞群を突きとめました。また、1型IFNが脳室内に蓄積し、脳室周辺から病態が進行していくことを明らかにしました。
こうしたAGS脳症を再現するモデルマウスを用いることで、薬剤の効果を評価することが可能となったことから、1型IFNシグナル経路を遮断し、脳症の進行を抑制する薬剤の確立が効率的に進むことが期待されます。
本研究成果は、米国科学誌「Cell Reports」の電子版に、3月18日(水)に公開されました。
図1. 1型IFNの過剰産生による脳症形成メカニズム
研究の背景
ウイルスなど異物が体内に侵入すると、我々の体内ではこれを迅速に感知する自然免疫というシステムがあります。ヒトを含めた哺乳類には、外来のDNAやRNAなどの核酸を認識するセンサー分子が発現しており、ウイルスの侵入を感知すると自然免疫が活性化して1型IFNが分泌され、ウイルスを排除するように作用します。こういった外来核酸のセンサー分子は、自己核酸への目印の付加や、迅速に分解されるため、宿主側の自己核酸には反応しません。しかし、こうした機構に異常が生じると、外来核酸のセンサー分子が自己核酸を認識し、自然免疫が異常活性化します。AGSは、先天的な自己炎症疾患でこれまで9つの原因遺伝子が同定されています。いずれも核酸代謝に関与する遺伝子であり、自己核酸への目印付加や分解処理が正常に作動しないため、自然免疫が異常活性化し、1型IFNが過剰産生されています。1型IFNが過剰産生される疾患群はインターフェロノパシーと総称されますが、中でもAGSは脳症を主症状とします。
AGS脳症は、脳室拡大、脳室周辺の石灰化、白質変性など、脳室周辺に強く症状が出現します。しかし、これまでAGSの原因遺伝子変異をマウスに挿入しても脳症を再現することができませんでした。このため、なぜ脳症が脳室周辺に強いのか、1型IFNが関与しているのか、関与しているなら1型IFNはどの細胞群で産生されているのか、といった多くのことが未解明でした。RNA編集酵素をコードするADAR1は、AGS原因遺伝子の1つですが、中でもZ型 (左巻き)RNA結合ドメイン中に多く変異が同定されています。研究グループは、AGSでこのドメイン中に同定されている変異と近傍にあり、Z型RNAへ完全に結合できなくなる別の変異を挿入したマウスを作成したところ、AGS脳症をよく再現するマウスを樹立することに成功しました (Nakahama et al, Immunity, 2021)。今回、このモデルマウスを活用することで、長年不明であったAGS脳症の発症メカニズムを解き明かすことに成功しました。
図2. ADAR1の遺伝子変異によるRNA編集活性の低下は、AGSの原因となる
研究の内容
研究グループでは、AGSモデルマウスを用いて、1型IFNシグナル経路を遮断すると、脳症が完全に消失したことから、脳症形成に1型IFNが必要不可欠であることを明らかにしました。次に、脳室内の1型IFN濃度が、血清中よりも高いことを明らかにし、脳内で直接1型IFNが過剰産生されていることを突きとめました。1型IFNによって誘導される各種遺伝子の発現が、特に脳室周辺で高まっており、脳室周辺で細胞の変性・脱落など病理学的変化が特に強いことを見出しました。
最後に、脳内の主要な構成因子である神経細胞、アストロサイトなど細胞特異的にADAR1の機能を低下させたマウスを作成し、いずれの細胞群も1型IFNの産生に関与していましたが、特にアストロサイトの関与が大きいことを解明しました。AGS脳症の発症病態を解明しただけでなく、Z型RNA制御の異常が疾患発症につながることを実証した成果と言えます。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、AGSの治療法の確立に向けた様々な取り組みを加速することが期待されます。これまで病態を再現するモデル動物がなかったことから、候補治療薬の効果を評価することが困難でした。特に、1型IFNシグナル経路を遮断するような薬剤を経口で内服することや、静脈から点滴した場合に、これらの薬剤がどの程度脳内に届き、効果を発揮するのか不明でした。研究グループが開発したモデルマウスを用いることで、どういった薬剤をどの経路から投与することが最も効果的なのか、各薬剤の評価が可能となりました。
特記事項
本研究成果は、2026年3月18日(水)に米国科学誌「Cell Reports」(オンライン)に掲載されました。
タイトル:“Aberrant Multicellular Interferon Signaling Underlies Adar1 Mutation-Driven Aicardi-Goutières Syndrome-like Encephalopathy”
著者名:Hyebin Yoo1,6, Taisuke Nakahama1,2,3,4,6,*, Reiichi Sugihara2, Yu Gao2, Yuta Ishizawa2, Jingqi Yang2, Zihan Ni2, Miyu Iwasaki2, Yuki Kato1,2,3 and Yukio Kawahara1,2,3,4,5,* (*責任著者)
所属:
1. 大阪大学 大学院生命機能研究科
2. 大阪大学 大学院医学系研究科 神経遺伝子学教室
3. 大阪大学 先導的学際研究機構 (OTRI) 生命医科学融合フロンティア研究部門、RNAフロンティアサイエンス部門
4. 大阪大学 感染症総合教育研究拠点 (CiDER)
5. 大阪大学 大学院医学系研究科 ゲノム編集センター
6. 共同第一著者
DOI:https://doi.org/10.1016/j.celrep.2026.117113
なお、本研究は、科学研究費助成事業 学術変革研究A 「攪乱RNA学創成」領域研究 (河原行郎)、JST 創発的研究支援事業(中濱泰祐 JPMJFR240F )などの一環として行われました。
参考URL
SDGsの目標
用語説明
- エカルディー・グティエール症候群 (AGS)
1型インターフェロン (IFN)の過剰産生と脳症を主症状とする先天性自己炎症性疾患。多くは生後まもなく発症し、10歳までに死に至る。本邦における患者数は50人以下の希少性難病。脳室拡大、脳室周辺の石灰化、白質変性に加え、進行すると脳萎縮が加わる。知的障害、発育遅滞、痙攣などの精神・神経症状を呈する。これまで9つの原因遺伝子が同定されており、いずれも核酸代謝に関わる遺伝子である。このため、自己のDNAやRNAなどに目印を付加したり、迅速に分解処理する過程が正常に機能しないことで、本来ウイルスなどに由来する外来性のDNAやRNAを感知するセンサー分子が自己核酸を異物と誤認してしまい、自然免疫の暴走によって1型 IFNが過剰産生されることが背景にあると考えられている。
- 1型インターフェロン (IFN)
抗ウイルス防御に働く物質サイトカインの一種。IFNには1型と2型があり、1型の方が抗ウイルス反応が強い。1型IFNは、多発性硬化症の治療などに用いられている。その一方で、1型IFNの過剰産生を背景とした疾患群はインターフェロノパシーと総称され、AGSもその1つである。
- アストロサイト
哺乳類の中枢神経系に最も多いグリア細胞の一種。神経細胞を物理的に支持するだけでなく、エネルギーを供給したり、神経伝達物質を回収するなど多様な機能を担っている。
- RNA編集
DNAはA, T, G, Cの4つの塩基で構成されているが、RNAはA, U, G, Cの4つの塩基で構成されている。しかし、RNAは転写後に様々な修飾を受けており、RNA編集もその一種である。中でも、RNA中のA (アデノシン)をI (イノシン)へと置換するRNA編集はADARファミリーに触媒される。Iを含むRNAは、自己RNAの目印となり、外来RNAのセンサー分子による感知を逃れる (図2)。しかし、RNA編集活性が低下すると、自己RNAが生体を攪乱してしまう。
- Z型 (左巻き)RNA
2本鎖のDNAやRNAは、通常右巻きのらせん構造が安定である。しかし特殊な配列を持つ場合や高塩濃度などの条件にすると左巻きらせん構造を形成することがあり、これをZ型とよぶ。RNA編集酵素ADAR1には、このZ型RNAに結合するドメインが存在しており、このドメイン中にAGSの原因遺伝子変異が見つかることから、Z型RNAの制御異常が発症病態の背景にあると考えられている。


