\分子の”働き方”が”居場所”を左右する!/ 神経興奮を司るカリウムチャネルの機能性が 軸索起始部(AIS)への局在性を決める仕組みの解明
てんかんの病態理解や新たな治療戦略に期待
研究成果のポイント
- 神経細胞の興奮を抑えるカリウムチャネル(KCNQ2/3)が軸索起始部(AIS)へ適切に配置されるためには、チャネル自身が正常な機能性を持つ必要があることを発見
- 1分子イメージング技術により、KCNQ2/3の機能不全が、AISの足場タンパク質(アンキリンG)との結合を弱め、AISへの集積を減少させることを実証
- てんかんに代表されるKCNQ2/3関連神経疾患の病態解明や新しい治療法の開発への貢献に期待
概要
大阪大学大学院医学系研究科の好岡大輔助教、岡村康司教授らの研究グループは、神経細胞の興奮性を制御する重要なカリウムチャネルであるKCNQ2/3が、活動電位の開始場所である軸索起始部(AIS)に集まるための新しい仕組みを発見しました。
神経興奮を制御するためには、KCNQ2/3がAISへ適切に「局在」し、かつ正常に「機能」することが求められます。KCNQ2/3が働かないと神経が過剰に興奮し、てんかんなど多くの神経・精神疾患の原因となります。これまで、KCNQ2/3のAIS局在はアンキリンGとの結合により制御される一方、そのチャネル機能は膜電位の感知に伴う一連の構造変化により制御されることが知られていました。しかし、これら2つの制御機構は長らく独立した別物とみなされ、両者の関連性は不明でした。
今回、研究グループは、てんかん関連変異を含む多様な機能不全KCNQ2/3変異体の解析により、KCNQ2/3の機能性が低いほど、AISへの局在効率も低くなるという因果関係を発見しました(図1)。さらに、1分子イメージング技術を組み合わせることで、KCNQ2/3が正常に働ける「構造」をとるとアンキリンGへの結合が強まり、AISに安定して配置されるという分子機構を解明しました(図2)。逆に、てんかんに関連する遺伝子変異によって機能が低下したKCNQ2/3はアンキリンGと十分に結合できず、AISに留まれなくなることが明らかになりました。これは、正常な分子だけを選んで“適材適所”に配置するという「品質管理機構」がKCNQ2/3自身に備わっていることを示しています。
本研究成果は、てんかんを含む様々な神経・精神疾患の原因となるKCNQ2/3の機能不全が同時に、その局在異常も引き起こす可能性が高いことを示唆しており、将来的にこれら疾患の発症機序の解明や新しい治療法の開発に貢献することが期待されます。
本研究成果は、米国科学誌「Proceedings of the National Academy of Sciences of the United States of America (PNAS)」に、3月2日(月)に公開されました。
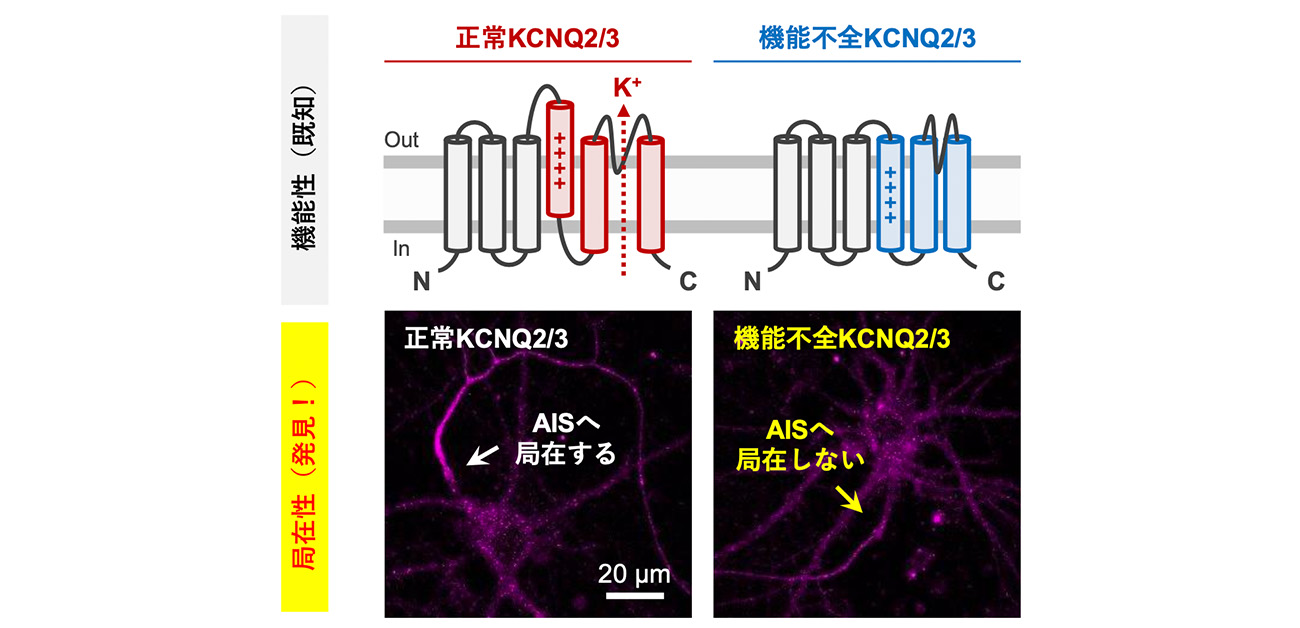
図1. KCNQ2/3の機能・局在連関の発見
正常なKCNQ2/3がAISに強く局在する一方、機能不全のKCNQ2/3ではAIS局在効率が著しく低下することを明らかにした。
研究の背景
私たちの脳は、およそ860億個もの神経細胞が互いに情報をやり取りすることで働いています。神経細胞は、細胞膜の内外に存在するイオンの流れを利用して「電気信号(活動電位)」を発生させ、軸索を通じてその情報を次の細胞へと伝えます。この神経細胞の興奮と抑制の精密なバランスが適切に保たれることが、正常な脳機能にとって不可欠です。
電位依存性カリウムチャネル(KCNQ2/3)は神経細胞の興奮を抑える、言わば”ブレーキ”としての重要な役割を担い、特に活動電位が最初に生じる軸索起始部(AIS)に集まることで、その機能を最大限に発揮します。もし、KCNQ2/3が正常に機能できないと、神経の興奮性が過度に高まってしまい、てんかんをはじめとする数多くの神経・精神疾患の原因となることが知られています。
これまで、KCNQ2/3がAISに局在する仕組みとして、足場タンパク質(アンキリンG)との結合が重要であることが明らかになっていました。一方で、チャネルの開閉を担う機能そのものは、膜電位の変化に応じた構造変化によって制御されることも知られていました。しかし、KCNQ2/3の「局在性」と「機能性」を制御する2種類の機構が互いに関連しているのかについては、長年不明のままでした。
研究の内容
研究グループは、まず、てんかんに関連する変異を含む様々な遺伝子変異を導入してKCNQ2/3の働きを弱めた変異体を多数作製し、その分子局在を詳細に解析しました。その結果、変異の導入部位に依らず、KCNQ2/3の機能性が低下すると、そのAIS局在効率も低下することが明らかになりました(図1)。重要なことに、今回変異を導入した部位には、既知の局在制御部位が1つも含まれていませんでした。
また、1分子イメージング技術を用いて、神経細胞の表面で1つ1つのKCNQ2/3チャネルがどのように動くのかを可視化することにも成功しました。これにより、機能が低下したKCNQ2/3では、三次元的な分子輸送経路の全てに異常が生じ、特に膜挿入の抑制と内在化の促進によってAISに留まれなくなることが明らかになりました。
さらに、1分子イメージング技術を応用し、生きた細胞内でKCNQ2/3とアンキリンGの結合強度を直接測定する新しい手法も開発しました。これにより、KCNQ2/3が正常に働ける「活性化構造」をとることでアンキリンGとの結合が強まり、AISに安定して配置されるという新たな分子メカニズムを世界で初めて示しました(図2)。
これらの結果は、KCNQ2/3が「正常に機能できる分子だけをAISに集める」という“品質管理機構”を自ら備えていることを意味します。つまり、チャネルの“働き方”そのものが、自身の“居場所”であるAISへの局在を左右していたのです。
図2. KCNQ2/3の機能性に依存したアンキリンG結合
KCNQ2/3が正常な機能性を持つと、アンキリンGに安定して結合しやすくなる。これにより、KCNQ2/3のAIS表面での膜挿入が促進され、逆に内在化が抑制される。一方、KCNQ2/3の機能性低下はアンキリンGへの結合を阻害する。これにより、機能不全KCNQ2/3のAIS表面での膜挿入は抑制され、逆に内在化が促進される。
本研究成果が社会に与える影響(本研究成果の意義)
KCNQ2/3の異常は、てんかんをはじめとする多くの神経・精神疾患の原因となることが知られています。本研究が明らかにした、KCNQ2/3の機能と局在を担う二大機構を統合する新たな原理は、これら疾患の病態理解を深めるとともに、新規治療戦略の開発に有益な洞察をもたらすと期待されます。
まず、チャネルの働きを弱める遺伝子変異は、AISにおける局在異常も同時に引き起こすことが示唆されます。従来のてんかん治療薬が主に細胞表面でのチャネル機能回復を目的としていることを踏まえると、KCNQ2/3の局在異常は薬剤耐性てんかんの発症機序を説明できる可能性があります。
一方で、細胞内に滞留する異常チャネルの機能を回復できれば、AISへの配置も同時に正常化し得ることから、新たな治療戦略の可能性も開けます。これはすなわち、チャネルの機能だけでなく局在も標的とする、KCNQ2/3関連疾患に対する新しい創薬の方向性を提示するものです。
特記事項
本研究成果は、2026年3月2日(月)に米国科学誌「Proceedings of the National Academy of Sciences of the United States of America (PNAS)」(オンライン)に掲載されました。
タイトル:“Coupling of Functionality to Trafficking of KCNQ2/3 Potassium Channels at the Axon Initial Segment”
著者名:Daisuke Yoshioka1* and Yasushi Okamura1* (*責任著者)
所属:
1. 大阪大学 大学院医学系研究科 統合生理学
DOI:https://doi.org/10.1073/pnas.2527749123
なお、本研究は、日本学術振興会科研費 20K22631、22K15373(好岡大輔)、21K19350、23K24066、25H01334(岡村康司)、一般財団法人蛋白質研究奨励会(好岡大輔)、公益財団法人上原記念生命科学財団(好岡大輔)、公益財団法人三菱財団(岡村康司)、公益財団法人小野医学研究財団(岡村康司)の助成を受けて行われました。
参考URL
岡村 康司 教授 研究者総覧
https://rd.iai.osaka-u.ac.jp/ja/7f408bd77a9891a8.html
用語説明
- KCNQ2/3
神経細胞に発現する主要な電位依存性カリウムチャネルの一種。電位依存性カリウムチャネルとは、膜電位の変化に応じて開閉し、カリウムイオンを透過する膜タンパク質の総称である。カリウムイオンの流出を通じて神経細胞の興奮性を低下させることで、活動電位の発生を抑制する役割を担う。
- 軸索起始部(AIS)
神経細胞の細胞体から伸びる軸索の起点となる領域。多数のイオンチャネルが高密度に集積し、活動電位が最初に生成される、神経の興奮性を決定づける極めて重要な部位。
- てんかん
脳内の神経細胞が過剰に興奮することで、けいれんや意識障害などの発作を繰り返す神経疾患。KCNQ2/3の遺伝的な機能不全は神経細胞の過度な興奮を引き起こし、特に新生児期や乳児期に発症するてんかんの原因となることが知られている。
- アンキリンG
AISに局在する代表的な足場タンパク質の一種。KCNQ2/3を含む多様な膜タンパク質と相互作用し、それらを繋ぎ止めることでAISを組織化する役割を果たす。
- 1分子イメージング技術
蛍光分子を1分子レベルで可視化するイメージング技術。全反射照明蛍光顕微鏡法では、ガラスと水の境界面でレーザー光を全反射させた際に生じる近接場光を利用することで、膜近傍の蛍光分子のみを選択的に励起し、背景光を大幅に低減できる。さらに、標的分子をごく低濃度で蛍光標識することにより、個々の蛍光分子を識別して検出することが可能となる。
