全臓器・全身の全細胞を網羅する3次元アトラスを構築
次世代の病理診断や創薬研究への展開に期待
研究成果のポイント
- 従来、全臓器や全身レベルで細胞の分布を網羅的に把握することは困難だった。
- 本研究では、マウスの全臓器および全身を対象に、全ての細胞を3次元かつ1細胞解像度で記録した3次元全細胞アトラスを構築した。
- 構築した3次元アトラスは、発達学・生理学・病理学を全身スケールで定量的に解析するための基盤となり、将来的には次世代の3次元病理診断や創薬研究への展開が期待される。
概要
JST 戦略的創造研究推進事業 ERATOにおいて、東京大学 大学院医学系研究科 機能生物学専攻システムズ薬理学分野の上田 泰己 教授(久留米大学 特別招聘教授 兼任)、吉田 将太 客員研究員、松本 桂彦 客員研究員らの研究グループは、全臓器・全身の全細胞を網羅する3次元アトラス(CUBIC Organ/Body Atlas)を構築しました。
従来の病理学や生理学研究では、薄く切った組織を観察する2次元解析が主流であり、臓器全体や個体全体における細胞の配置や数を包括的に把握することは困難でした。そのため、発達過程や病気に伴う変化を臓器全体や全身レベルで定量的に理解するための新たな解析基盤の整備が求められていました。
本研究グループは、臓器や個体の組織透明化処理手法(CUBIC法)を各臓器および新生仔(こ)マウス全身に適用できるよう最適化するとともに、広い範囲を高い解像度で撮影可能な独自の3次元撮影技術を開発しました。さらに、取得した3次元画像から細胞一つ一つの位置情報を抽出し、臓器全体や全身の全細胞から構成される3次元アトラスを構築しました。これにより、異なる個体や実験条件で得られた細胞の分布を、同じ基準の基で重ね合わせて比較することが可能になりました。
本成果は、発達学・生理学・病理学を全身スケールで定量的に解析するための基盤となり、疾患の理解や新たな医療技術の創出に貢献するとともに、将来的には次世代の3次元病理診断や創薬研究への展開が期待されます。
本研究は、がん研究会 がん化学療法センターの高木 聡 主任研究員、順天堂大学 大学院医学研究科の洲崎 悦生 教授、大阪大学 大学院医学系研究科の森井 英一 教授、東京大学 大学院医学系研究科の牛久 哲男 教授、岩手医科大学 医歯薬総合研究所の吉岡 芳親 客員教授らの研究グループと共同で行われました。
本研究成果は、2026年2月25日(米国東部時間)に米国科学誌「Cell」オンライン版で公開されました。
研究の背景
生命現象や疾患を理解する上で、細胞は最小の構成単位であり、臓器や個体の機能は、細胞の数や配置、相互関係によって規定されています。病理学や生物学の研究では、これまで主に薄く切った組織切片を用いた2次元解析が行われてきましたが、この方法では臓器全体や全身における細胞分布を包括的に把握することは困難でした。特に、病変の不均一性や希少な細胞集団の存在は、2次元解析では見落とされる可能性があることが指摘されていました。
近年、医療や創薬においては、疾患を単一の臓器や局所の異常として捉えるのではなく、全身レベルでの変化として理解する重要性が高まっています。薬剤の有効性や副作用、免疫応答、発達過程における変化などは、複数の臓器や組織にまたがって生じることが多く、臓器横断的かつ定量的に解析できる基盤の必要性が広く認識されています。
このような現状を踏まえ、本研究グループは脳を対象として、脳全体を3次元的に観察し、全細胞を解析する研究を進めてきました。脳は、極めて多様な細胞種が高度に組織化され、空間配置と機能が密接に対応している代表的な臓器であり、細胞分布を3次元的に把握する意義が特に大きい組織です。こうした背景のもと、マウスの脳全体を3次元的に観察し、脳に含まれる全細胞を共通の座標系上で比較可能とする3次元全細胞アトラスを構築することで、全細胞解析の概念と解析基盤を提示してきました。
一方で、脳以外の臓器や全身においては、3次元アトラスに基づく全細胞解析は十分に行われておらず、個体全体を対象として全細胞の情報を取得し、複数サンプルを比較統計解析するための技術基盤は十分に整備されていませんでした。さらに、全身や肝臓などの大型臓器を対象とした解析では、観察範囲と解像度を両立させることが難しく、得られた全細胞のデータを異なる個体間で比較するための解析手法も確立されていませんでした。
研究の内容
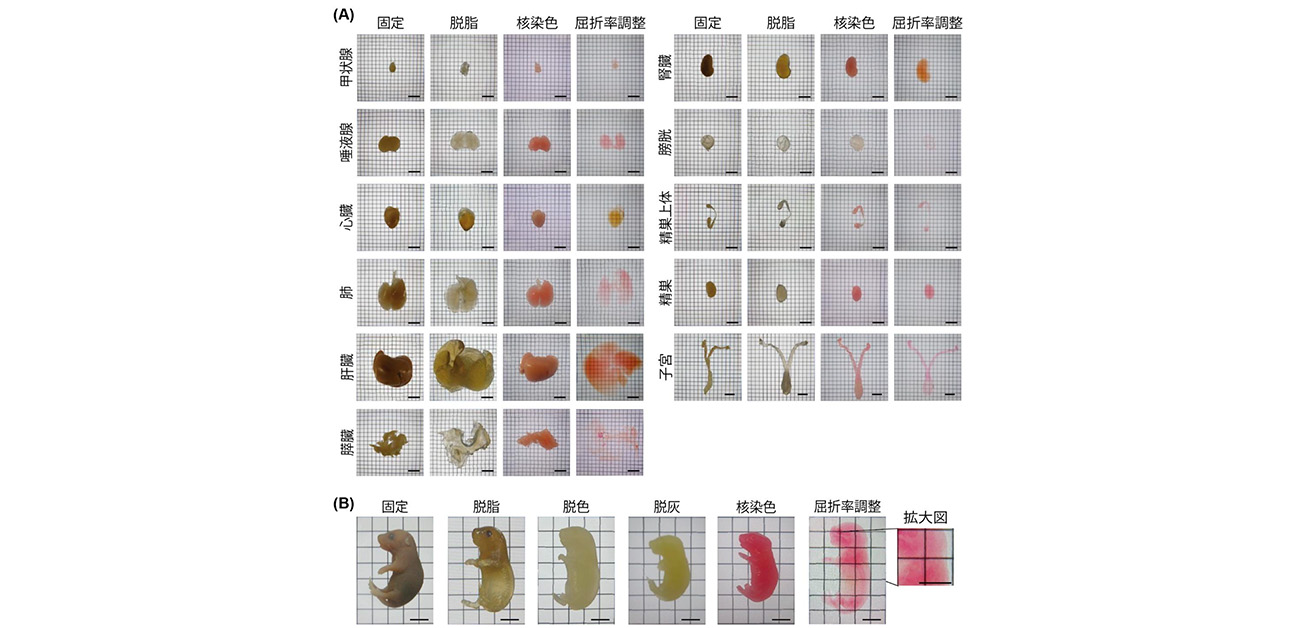
本研究グループはまず、成体マウスの主要臓器および新生仔マウス全身を対象として、臓器や個体の立体構造を保持したまま内部を観察できる組織透明化処理手法(CUBIC法)を適用しました。特に、臓器の種類や全身では脱脂効率や屈折率調整効率が大きく異なることから、処理手順を臓器ごとに最適化することで、均一な透明化と高品質な3次元観察を可能にしました(図1)。例えば、腎臓では脱脂期間として通常の2倍にあたる10日間が必要であり、肝臓では屈折率調整液の濃度を段階的に上げていくことが重要であることが分かりました。
図1. 組織透明化のプロセス
脱脂および屈折率調整の処理時間や方法を最適化することで高い透明度を達成した。
(A)成体マウスの11臓器の組織透明化。
(B)新生仔マウス全身の組織透明化。
透明化したサンプルは、薄い光のシートで試料内部を走査しながら撮影できるライトシート顕微鏡を用いて観察します。しかし従来のライトシート顕微鏡では、高解像度でありながら厚みのある試料全体を撮影することが困難でした。そこで本研究では、深い観察範囲と高い解像度を両立させるため、独自のライトシート顕微鏡を開発しました。この技術により、数十ミリメートル規模の臓器や個体全体を対象としても、細胞一つ一つを識別可能な解像度で3次元画像を取得できるようになりました。さらに、取得した3次元画像から各細胞の位置情報を網羅的に抽出しました。例えば、新生仔マウス全身では、雄では平均約6.1億個、雌では平均約5.3億個の細胞が存在することを明らかにしました。これら全ての細胞の位置情報を基に、臓器全体および全身に含まれる全細胞から構成される3次元アトラスを構築しました(図2)。
図2. 3次元アトラス(CUBIC Organ/Body Atlas)の作成
(A)成体マウスの臓器に含まれる全細胞の検出。各パネルは、左上にライトシート顕微鏡で撮影した2次元断面画像、右上にその拡大画像、右下に検出された細胞を赤色でハイライト表示した拡大像、左下に検出した核の密度を3次元で再構成した図を示す。
(B)臓器の3次元アトラスの作成。核の密度から再構成した臓器の3次元画像をもとに、解剖学的な領域ごとに色分けを行い、臓器の3次元アトラスを構築した。上段にアトラスの全体像を示す。下段に体を左右に分ける方向(矢状断)で切った断面像を示す。
(C)透明化した新生仔マウス全身の撮影。矢状断での画像とその拡大図。全身に含まれる全細胞を検出した。
(D)全身の3次元アトラスの作成。検出した全身の核の密度を3次元で再構成した図から3次元的に各臓器を色分けし、全身の3次元アトラスを作成した。
さらに本研究グループは、新たに構築した3次元アトラスを用いて、発達段階や疾患モデル、薬剤投与条件などに応じた細胞分布の変化を、臓器全体のスケールで解析できることを示しました。具体的には、腎臓の発達過程における領域ごとの細胞数変化や、薬剤投与による臓器障害、炎症に伴う免疫細胞の全身的な分布変化などを、3次元的かつ定量的に捉えることに成功しました。また、3次元アトラスを利用し、特定の細胞種を全身スケールで解析する応用例も示しました。免疫応答に重要な役割を果たすマクロファージに着目し、マクロファージのマーカーであるIBA1の3次元免疫染色と3次元撮影を組み合わせることで、マクロファージの分布を全身スケールで可視化しました。そのデータを3次元アトラス上にマッピングした結果、マクロファージの数や密度、空間的分布が臓器ごとに異なることを明らかにしました(図3)。特に、脾臓(ひぞう)など特定の臓器ではマクロファージが局所的に集まって存在していることが確認されました。このような特徴的な配置は、マクロファージが臓器ごとに異なる役割や機能を担っている可能性を示唆しており、今後のさらなる研究によってその生理的意義の解明が期待されます。
図3. 3次元アトラスを用いたマクロファージ分布解析
(A)新生仔マウス全身アトラスを用いたマクロファージ解析のワークフロー。
まず、サンプル中の全ての細胞を可視化した核染色画像と、マクロファージだけを光らせた免疫染色画像を撮影する。次に、核染色画像を3次元アトラスの画像と比較し、サンプルの形や向きをどのように変形すればアトラスにぴったり重ねられるかをコンピューターで計算する。この計算によって得られた位置合わせの情報を、検出されたマクロファージ陽性細胞の位置データに適用することで、それぞれの細胞が体のどの臓器のどの場所にあるかを自動的に割り当てることができる。これにより、観察した細胞を3次元アトラス上にマッピングし、臓器ごとのマクロファージの分布を詳しく解析することが可能になった。
(B)検出された全マクロファージの分布(左)、アトラス情報を付加した全身のマクロファージ分布(臓器ごとに色分けして表示)(右)。
(C)各臓器におけるマクロファージ分布の定量解析。各組織において、それぞれのマクロファージと、最も近接するマクロファージとの距離を計算し、ヒストグラムにした。局所的にマクロファージが集まっている場合、ヒストグラムは左に寄る。解析の結果、脾臓など特定の臓器ではヒストグラムが強く左方に偏り、マクロファージが局所的に集簇(しゅうぞく)して存在していることが示された。これは、マクロファージが臓器ごとに異なる機能的役割を担っている可能性を示唆している。
今後の展開
本研究で構築した全臓器・全身の3次元細胞アトラスは、発達学・生理学・病理学などの研究において、細胞分布や細胞数の変化を全身スケールで定量的に評価するための基盤技術として活用されることが期待されます。本技術により、これまで局所に限定されていた解析を、臓器や全身の文脈の中で比較・検討することが可能になります。さらに、取得した3次元アトラスデータを既存の遺伝子発現情報や空間トランスクリプトームなどの2次元空間解析データと組み合わせることで、形態情報と分子情報を統合した解析へと発展させることができます。このような統合解析は、より高い精度での疾患の理解や、新たな病態解析指標の創出につながる可能性があります。本研究で確立した解析基盤は、将来的なヒト組織への応用を見据えつつ、従来の2次元病理診断を補完・拡張する次世代の3次元病理診断へと展開可能な基盤として、基礎研究から応用研究まで幅広い分野での活用が期待されます。
特記事項
【論文情報】
“Whole-organ and Whole-body 3D Atlases Enable Cellome-wide Profiling”
(全臓器・全身の3次元アトラスによる全細胞プロファイリング)
DOI:10.1016/j.cell.2025.12.057
本成果は、以下の支援によって得られました。
戦略的創造研究推進事業 総括実施型研究(ERATO)
研究領域:「上田生体時間プロジェクト」(JPMJER2001)
研究総括:上田 泰己(東京大学 大学院医学系研究科 教授/久留米大学 特別招聘教授)
研究期間:2020年10月~2026年3月
本プロジェクトでは、睡眠・覚醒リズムをモデル系として「ヒトの理解に資するシステム生物学」を展開し、分子から社会に生きるヒト個体までを通貫する「生体時間」情報の理解を目指しています。
その他、JST ムーンショット型研究開発事業(課題番号:JPMJMS2023)、文部科学省 光・量子飛躍フラッグシッププログラム(Q-LEAP)(課題番号:JPMXS0120330644)、日本学術振興会(JSPS) 科学研究費補助金(課題番号:JP20K06885、JP20K16626、JP23K27391、JP22H02824、JP22H04926、JP23K20044)の支援を受けて実施されました。
用語説明
- 3次元アトラス(CUBIC Organ/Body Atlas)
臓器や全身の3次元の参照データ。臓器や全身の3次元画像データに臓器や構造の位置情報が付加されている。本研究では、臓器全体や全身に存在する全細胞の位置を3次元的に記録し、領域分けしている。
- 組織透明化処理手法(CUBIC法)
2014年に理化学研究所で開発された、臓器や全身を対象として3次元的に観察するための組織透明化技術。生体組織に含まれる脂質や色素を除去し、屈折率を調整することで組織を透明化し、臓器や個体の立体構造を保ったまま内部を3次元的に観察することを可能にする。CUBICは Clear, Unobstructed Brain/Body Imaging Cocktails and Computational analysisの略。
- マクロファージ
免疫細胞の一種で、体内に侵入した異物の除去や、炎症反応の制御などに重要な役割を果たす。
- IBA1
IBA1(Ionized calcium binding adaptor molecule 1)は、主にマクロファージやミクログリアに特異的に発現するたんぱく質で、これらの免疫細胞を同定するための代表的なマーカーとして広く用いられている。本研究では、組織中に存在するマクロファージを可視化し、その分布や数を解析する目的でIBA1抗体による染色を行った。
