iTregの分化・安定性・機能を強化する方法を発見
自己免疫疾患に対する画期的治療法の可能性
研究成果のポイント
- ヒトin vitro誘導型制御性T細胞(iTreg)において全ゲノムCRISPRスクリーニングを実施し、FOXP3発現の新規抑制性因子としてRBPJを同定した
- Perturb-icCITE-seqを用いたシングルセル解析により、FOXP3発現制御の分子ネットワークをカタログ化した
- RBPJノックアウトiTregでは、FOXP3およびTreg関連遺伝子の発現が増強され、免疫抑制能およびFOXP3の安定性が向上した
- RBPJはNCOR複合体と協調し、ヒストン脱アセチル化を通じてFOXP3発現を直接的に抑制する
- RBPJノックアウトは、マウス病態モデルにおけるiTregのパフォーマンスを向上させ、自己免疫疾患の新規治療アプローチとしての可能性を示した
概要
大阪大学免疫学フロンティア研究センター (WPI-IFReC) のKelvin Chen 特任助教(常勤)、坂口 志文 特任教授(常勤)らの研究グループは、中外製薬株式会社の木林達也氏らと共同で、ヒトCD4+ T細胞において転写因子RBPJを除去することで、iTregの分化、安定性、および免疫抑制能が向上することを発見しました。この発見は、自己免疫疾患の治療において、iTreg細胞療法の障壁となる課題を克服する可能性を提示しました。
iTreg細胞療法における課題の一つは、抑制するべき炎症環境がiTregを不安定にする可能性があるということです。そのような条件下では、iTregは抑制能を失い、場合によっては炎症促進に寄与し、病態を悪化させる可能性があります。
今回の研究では、RBPJをFOXP3の新規調節因子として同定し、RBPJがNCOR抑制性複合体と協調して局所的なヒストンアセチル化レベルを調節することで、FOXP3発現に影響を与えることを明らかにしました。RBPJをノックアウトすることで、iTregの免疫抑制機能が強化され、炎症条件下でも安定なiTregの作製に成功しました。(図1)
本研究成果は、英国科学誌「Nature」に、3月27日(木) 午前1時(日本時間)にオンラインで公開されました。
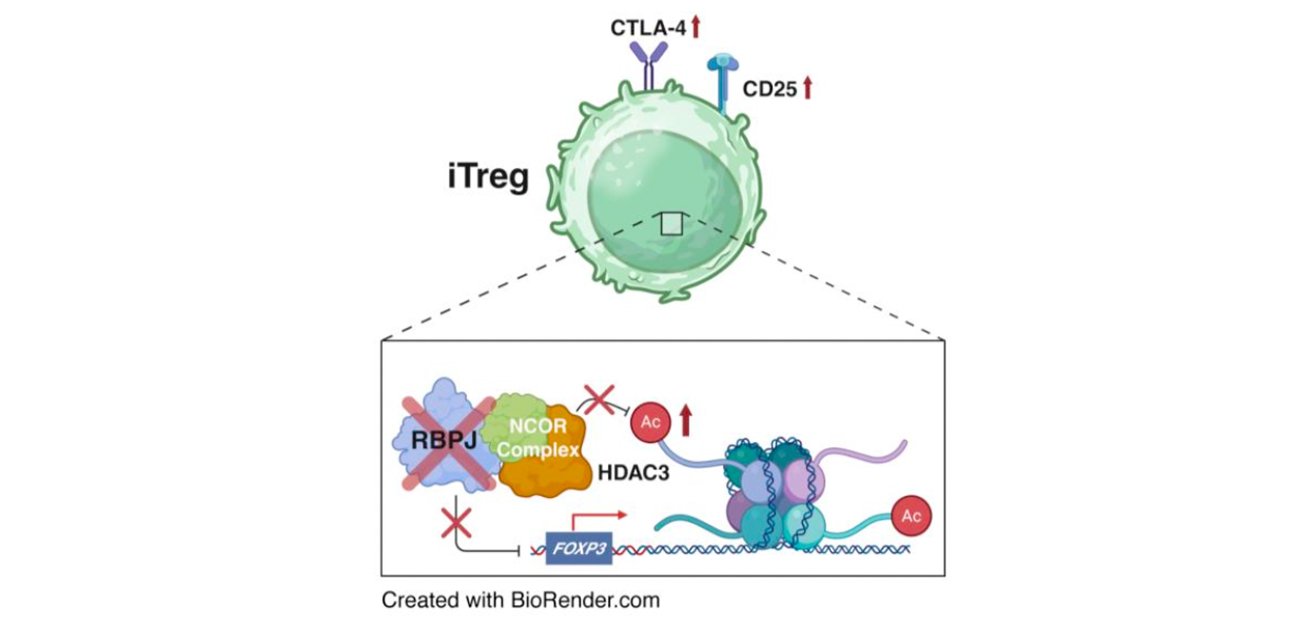
図1. 本研究の概要
RBPJはNCOR複合体と協調してFOXP3遺伝子座に結合し、HDAC3を介したヒストン脱アセチル化によって、その転写を抑制する。したがって、RBPJ除去によりこの抑制を解除することで、iTregにおけるFOXP3発現が亢進し、CTLA-4やCD25を含むTreg関連遺伝子の発現も増加する。
研究の背景
Tregは、自己免疫寛容の確立と維持に中心的な役割を果たしており、自己免疫、アレルギー反応、移植免疫、腫瘍免疫などの様々な免疫応答の調節において重要です。従来のCD4+ T細胞からin vitroで誘導されるiTregは、生体内で分化するTregの機能を模倣し、自己免疫疾患に対する細胞治療への応用が期待されています。しかし、iTregの効率的な誘導、安定性、抑制能、および生体内持続性などの課題が、臨床応用のボトルネックとなっています。Tregの機能とアイデンティティの重要な決定因子は転写因子FOXP3であり、これはTreg系統を定義するだけでなく、その抑制活性にも不可欠です。これまでのCRISPRスクリーニングを用いた報告では、マウスモデルにおけるFoxp3の調節因子が特定されていましたが、ヒトiTregにおけるFOXP3発現を制御する因子はほとんど解明されていませんでした。
研究の内容
CRISPRノックアウトスクリーニングを利用し、従来のCD4+ T細胞をiTregに転換する過程においてFOXP3発現を正または負に制御する可能性のある数百の候補を特定しました。しかし、フローサイトメトリーを用いる従来の方法では、通常、FOXP3タンパク質などの限定的なパラメータ解析にとどまり、CRISPRノックアウトによる広範な表現型の変化を一度に効率よく解析することができませんでした。
この制約を克服するため、Perturb-icCITE-seqという新しいシングルセルRNA-seq解析手法に目を向けました。この手法はスケーラビリティにおいて大きな利点があり、各標的ノックアウトによるFOXP3タンパク質発現と転写プロファイルの両方を直接測定することができます(図2)。この方法により、各候補がFOXP3に与える影響だけでなく、iTreg分化中に生じる表現型変化についても深く理解することが可能となりました。このアプローチは、iTreg分化制御に関わる複雑な調節ネットワークへの貴重な洞察をもたらしました。
図2. 新規シングルセル解析手法によるハイスループット表現型解析
CRISPR技術を用いた遺伝子編集により数百遺伝子にわたる数千のノックアウト細胞が調製され、それらはドロップレットマイクロ流体技術によりシングルセル化されることで、個々の細胞に対する高解像度の表現型解析が可能となる。Perturb-seqは、各標的遺伝子による影響を体系的に統合させることで、複雑な遺伝子調節ネットワークのマッピングを可能にし、遺伝子間の相互作用と細胞の挙動への影響を明らかにする。今回の研究では、この手法によりFOXP3調節に関連する遺伝子ネットワークをマッピングした。
今回の研究では特にRBPJという遺伝子に着目しました。前述の解析から、RBPJのノックアウトによりFOXP3発現が増加し、かつ、既知の相互作用分子もFOXP3調節因子として同定されたため、FOXP3を抑制するための協調的なメカニズムの存在が示唆されました。そのため、T細胞においてRBPJの発現を制御することで、「より良いiTreg」を作製できるかを検討しました。
RBPJ遺伝子をノックアウトしたiTreg (RBPJ KO-iTreg) では、対照と比べてより高くFOXP3を発現することを確認しました。次に、免疫抑制能を測定する共培養アッセイを用い、RBPJ KO-iTregの機能を対照と比較しました。その結果、RBPJ KO-iTregはより高い抑制能を有することが明らかとなりました。また、炎症促進性サイトカインへの繰り返し曝露によるストレステストでは、RBPJ KO-iTregは高い耐性を示し、FOXP3を安定して発現することが確認されました。これらの結果は有望なものでしたが、同時に「RBPJがどのようにFOXP3を制御するのか」について解析する必要がありました。
RBPJによるFOXP3抑制機構を明らかとするため、RBPJのクロマチン占有プロファイルと、RBPJによるエピジェネティック・ランドスケープを検証する一連の実験を行いました。これにより、RBPJがFOXP3遺伝子座に直接結合し、NCOR複合体と協調してヒストン脱アセチル化を通じたクロマチン抑制を促進することを見出しました。RBPJの除去に伴い、FOXP3の局所的なヒストンアセチル化が増加し、クロマチンアクセシビリティとFOXP3発現が増加しました。
最後に、臨床的な応用可能性を評価するため、RBPJ KO-iTregを異種移植片対宿主病 モデルに移入しました。その結果、RBPJ KO-iTregは病態の進行をより効果的に抑制することが明らかとなり、RBPJを標的とすることでiTregを用いた細胞療法の治療効果が高まる可能性が示唆されました。
本研究成果が社会に与える影響(本研究成果の意義)
Tregsが様々な免疫応答調節に関与しているという証拠が増えているにもかかわらず、効果的な細胞療法の開発には依然として大きな課題があります。この研究による発見、特にRBPJ同定とそのFOXP3発現制御における役割の解明は、FOXP3調節の理解を深め、自己免疫疾患における免疫介入の改善に新たな道を開くものです。
特記事項
【論文情報】
掲載紙: Nature 2025年3月27日 (日本時間午前1時) オンライン版
タイトル: “Genome-wide CRISPR screen in human T cells reveals regulators of FOXP3”
著者名: Kelvin Y. Chen*‡, Tatsuya Kibayashi*, Ambre Giguelay, Mayu Hata, Shunsuke Nakajima, Norihisa Mikami, Yusuke Takeshima, Kenji Ichiyama, Ryusuke Omiya, Leif S. Ludwig, Kunihiro Hattori, Shimon Sakaguchi‡ (*: equally contributed; ‡: correspondence)
DOI: 10.1038/s41586-025-08795-5
本研究は、日本学術振興会科学研究費助成事業(16H06295)、日本医療研究開発機構(AMED)(18cm0106303、18gm0010005)、日本学術振興会科学研究費助成事業 若手研究者奨励金(23K14545)の支援を受けて行われました。
用語説明
- In vitro誘導型制御性T細胞 (iTreg)
CD4+ ヘルパーT(Th)細胞の一種で、抑制的な応答を促進する。iTregは、通常、TGF-βおよびIL-2刺激を含む特定の培養条件下で従来のCD4+ T細胞から誘導される。iTregはFOXP3を発現し、生体内で分化するTregの機能を模倣して免疫抑制に寄与するが、その安定性と抑制能力は環境によって異なる場合がある。
- CRISPRスクリーニング
ゲノム内のすべての遺伝子をオフ(ノックアウト)して各遺伝子が特定の生物学的プロセスにどのように影響するのかを確認する方法。この全ゲノムスケールのアプローチは、特定の生物学的機能にとって潜在的に重要な遺伝子を迅速に特定するのに役立つ。
- FOXP3
Treg細胞系統を定義し、Tregの分化と機能にとって重要なマスター転写因子です。FOXP3は様々な遺伝子の発現を調節し、T細胞が免疫抑制能力を獲得することを可能にします。
- RBPJ
Notchシグナル伝達の主要な媒介因子として知られる転写因子。RBPJは造血系において重要な役割を果たし、主にT細胞、B細胞、および他の免疫細胞系統の発生と分化を調節する。
- Perturb-icCITE-seq
Perturb-seqは、CRISPR遺伝子編集とシングルセルRNA-seqを組み合わせた技術であり、個々の細胞における遺伝子ノックアウトの表現型の結果を大規模にプロファイリングすることを可能にする。Perturb-icCITE-seqは、Perturb-seqの拡張版で、FOXP3などの細胞内タンパク質のプロファイリング機能を追加したもの。
- Treg関連遺伝子
Tregsにおいて特異的に発現する遺伝子セットを指し、これらの遺伝子はTregsの機能と維持に重要な役割を果たす(例:FOXP3、CD25、CTLA-4)。
- NCOR複合体
特定の遺伝子発現を抑制するために協調するタンパク質群。この複合体には、HDAC3やNCOR1/2などのよく知られたリプレッサータンパク質が含まれる。
- ヒストン脱アセチル化
ヒストンタンパク質からアセチル基が除去され、遺伝子へのアクセシビリティが減少し、転写が抑制されるプロセス。このプロセスは、細胞分化や遺伝子発現などの重要な生物学的機能の調節において重要な役割を果たす。
- クロマチン占有プロファイル
特定のタンパク質(例えば転写因子)がゲノム全体においてDNA結合する場所をマッピングしたもの。
- エピジェネティック・ランドスケープ
DNAおよびヒストンタンパク質の化学修飾を指し、これらは遺伝子活性を調節する。修飾には、DNAメチル化、ヒストンメチル化、およびヒストンアセチル化などが含まれる。
