統合失調症の革新的な新薬につながる 神経ペプチド受容体VIPR2の選択的な阻害ペプチドを創製
研究成果のポイント
- 統合失調症の革新的な新薬につながる神経ペプチド受容体VIPR2に対する選択的な阻害ペプチドを創製し、その効果を動物モデルで初めて実証しました。
- 既存薬とは全く異なる作用機序をもつ化合物で、統合失調症の新しい治療法の開発につながることが期待されます。
概要
広島大学大学院医系科学研究科細胞分子薬理学 吾郷 由希夫 教授、大阪大学大学院薬学研究科薬剤学分野 中川 晋作 教授、一丸ファルコス株式会社 坂元 孝太郎 主席研究員らの研究グループは、統合失調症の革新的な新薬につながる神経ペプチド受容体VIPR2の選択的な阻害ペプチドを創製しました。
統合失調症は、幻覚や妄想などの陽性症状、意欲の低下などの陰性症状、そして注意・集中力の低下や記憶力・判断力の低下といった認知機能障害などを特徴とする精神疾患で、人口の約1%に発症し、その罹患者は日本では約80万人、全世界では2000万人以上いると言われています。
既存の治療薬は、いずれもドーパミンやセロトニンなどの神経伝達物質とよばれる分子の働きを調節する作用機序であるため、限定的な治療効果が課題となっています。
本研究では、これまでの基礎研究や臨床研究から明らかになってきた統合失調症の発症と神経ペプチド受容体VIPR2の過剰な働きとの関連に着目して、VIPR2を選択的に阻害することができるペプチド化合物KS-133を創製し、その効果を動物モデルで初めて実証しました。
今回の結果から、統合失調症の治療薬開発のための新たな道筋が示されたと同時に、精神疾患やその他の疾患においても、本化合物を用いることで、VIPR2の新たな役割が発見されることが期待されます。
本研究成果は、2021年11月4日(木)14時(日本時間)にFrontiers in Pharmacologyに掲載されました。
背景
統合失調症は、幻覚や妄想などの陽性症状、意欲の低下などの陰性症状、そして注意・集中力の低下や記憶力・判断力の低下といった認知機能障害などを特徴とする精神疾患で、人口の約1%に発症し、その罹患者は日本では約80万人、全世界では2000万人以上いると言われています。
既存の治療薬は、いずれもドーパミンやセロトニンなどの神経伝達物質とよばれる分子の働きを調節する作用機序を有していますが、限定的な治療効果が課題となっています。
当研究グループを含む複数の基礎研究ならびに臨床研究の報告から、これまでに、VIPやPACAPとよばれる神経ペプチドの受容体の一つであるVIPR2の発現量の増加や過剰な働きが、統合失調症と強い関連があることが明らかになってきました。このことから、VIPR2の機能を抑える(阻害する)化合物が、新しい統合失調症の治療薬になる可能性が示唆されていましたが、この受容体のもつ構造上の特徴や、神経ペプチドが複数の異なる受容体に結合することなどの理由から、VIPR2選択的な阻害薬の開発は難航していました。
研究成果の内容
今回、従来の統合失調症治療薬として使用されている低分子化合物(分子量400程度)とは異なり、分子量が1500程度の中分子のペプチド化合物を用いることで、VIPR2受容体に対する高い選択性と強力な阻害作用の両方を実現することに成功しました。また、本ペプチド化合物は配列内に2か所の架橋構造(環状化)を有するユニークな構造であり、それによって、血液中で分解されにくく、高い安定性を示すことも分かりました。
さらに、この化合物の効果を統合失調症のモデルマウスを作製して検証したところ、マウスの発育早期におけるVIPR2の過剰な活性化による神経細胞の未成熟状態を改善し(図1)、認知機能障害の発症も抑制する(図2)ことが明らかになりました。
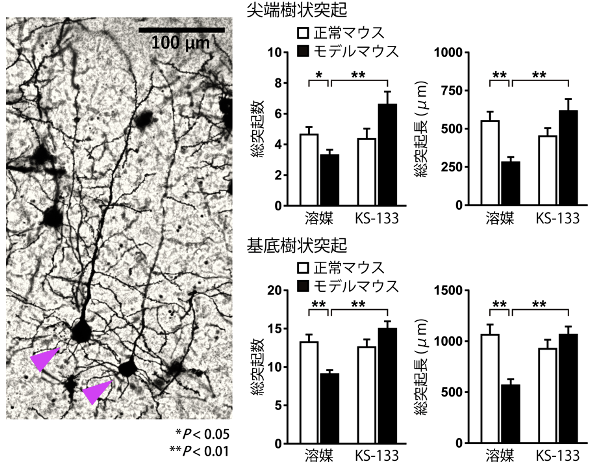
図1. 脳の神経細胞の形態を調べるゴルジ染色法。写真はマウス大脳皮質の神経細胞を示す(矢尻は細胞体の場所)。細胞体から樹状突起とよばれる長短複数の神経突起が伸びている。統合失調症のモデルマウスでは、神経細胞の尖端樹状突起や基底樹状突起の数が低下しており、また正常の状態よりも短い突起が多くみられ、未成熟な状態であることが示唆された。VIPR2に選択的な阻害ペプチドKS-133を投与しておくことにより、この樹状突起の異常な形態はみられなくなる。
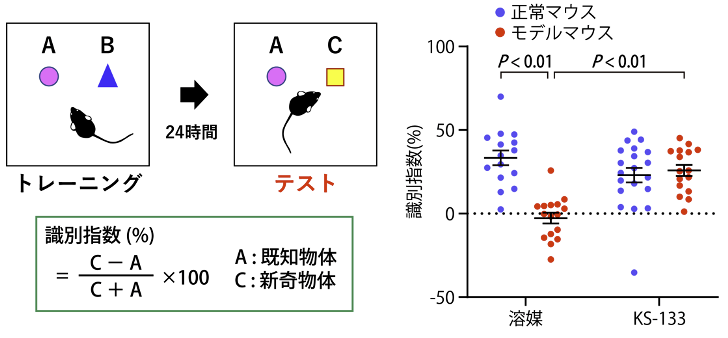
図2. 統合失調症モデルマウスでの認知機能を評価する試験。マウスは新しい環境や物体を積極的に探索する習性をもつ。マウスに二つの新しい物体AとBを探索させて、記憶させる。24時間後に既知物体であるBを新しい物体Cに置き換えて、マウスが物体Cをどれだけ探索するかを計測することで、マウスの物体認知、学習・記憶能力を解析する。物体AとCの総探索時間のうち、どれだけ物体Cを探索していたかを調べる識別指数を用いて評価する。数値が高いほど認知機能が高いことを意味する。統合失調症のモデルマウスの識別指数は、VIPR2に選択的な阻害ペプチドKS-133を投与しておくことにより改善し、正常マウスと同等になる。
今後の展開
今回、神経ペプチド受容体VIPR2の選択的な阻害ペプチドを創製しましたが、この化合物の安全性や体内での薬物動態は不明です。今後、細胞や動物モデルなどを用いた更なる検討、そしてヒトでの臨床試験によって、VIPR2阻害ペプチドの有効性と安全性を確認していくことで、統合失調症の新しい治療薬として登場することが期待されます。
特記事項
<発表論文>
論文タイトル:Generation of KS-133 as a novel bicyclic peptide with a potent and selective VIPR2 antagonist activity that counteracts cognitive decline in a mouse model of psychiatric disorders
著者:坂元 孝太郎1、陳 露2、宮岡 辰典2、山田 めゐ2、桝谷 晃明1、石本 憲司2、樋野 展正2、中川 晋作2、浅野 智志3、吾郷 由希夫3
1. 一丸ファルコス株式会社
2. 大阪大学大学院薬学研究科薬剤学分野
3. 広島大学大学院医系科学研究科細胞分子薬理学
掲載雑誌:Frontiers in Pharmacology
DOI番号:10.3389/fphar.2021.751587
用語説明
- 神経ペプチド受容体VIPR2
血管作動性腸管ペプチド(vasoactive intestinal peptide:VIP)や下垂体アデニル酸シクラーゼ活性化ポリペプチド(pituitary adenylate cyclase-activating polypeptide:PACAP)とよばれる神経ペプチドの受容体の一つ。VIPやPACAPは、血管拡張作用や免疫機能調節作用といった生理作用に加え、神経保護作用などを有することが知られている。脳においてVIPR2は、概日リズムの調節に関与することが分かっているが、精神疾患と関連するメカニズムは未だ不明な点が多い。
PACAPとVIPは3つの異なる受容体、PAC1、VIPR1、VIPR2を異なる親和性で刺激する。これらの受容体は約50%の配列同一性を有している。
- 神経伝達物質
神経細胞の軸索とよばれる長い突起の末端から放出され、次の神経細胞や筋肉細胞などに作用を引き起こす化学物質の総称。ドーパミンやセロトニン、ノルアドレナリン、アセチルコリンなど多くの種類が存在する。
- ペプチド化合物
アミノ酸とアミノ酸がペプチド結合し、2個以上つながった構造のものを指す。アミノ酸の種類と数によって多様な種類が存在する。一般にアミノ酸が50個以上結合したものをタンパク質といい、50個未満のものはペプチドとよばれる。
- 薬物動態
投与された薬物がどのように吸収され、組織に分布し、小腸や肝臓中の酵素により代謝され、排泄されるのかなどを指す言葉。これらの過程は薬物の効果や持続時間のみならず、副作用や薬物相互作用などに関連している。
