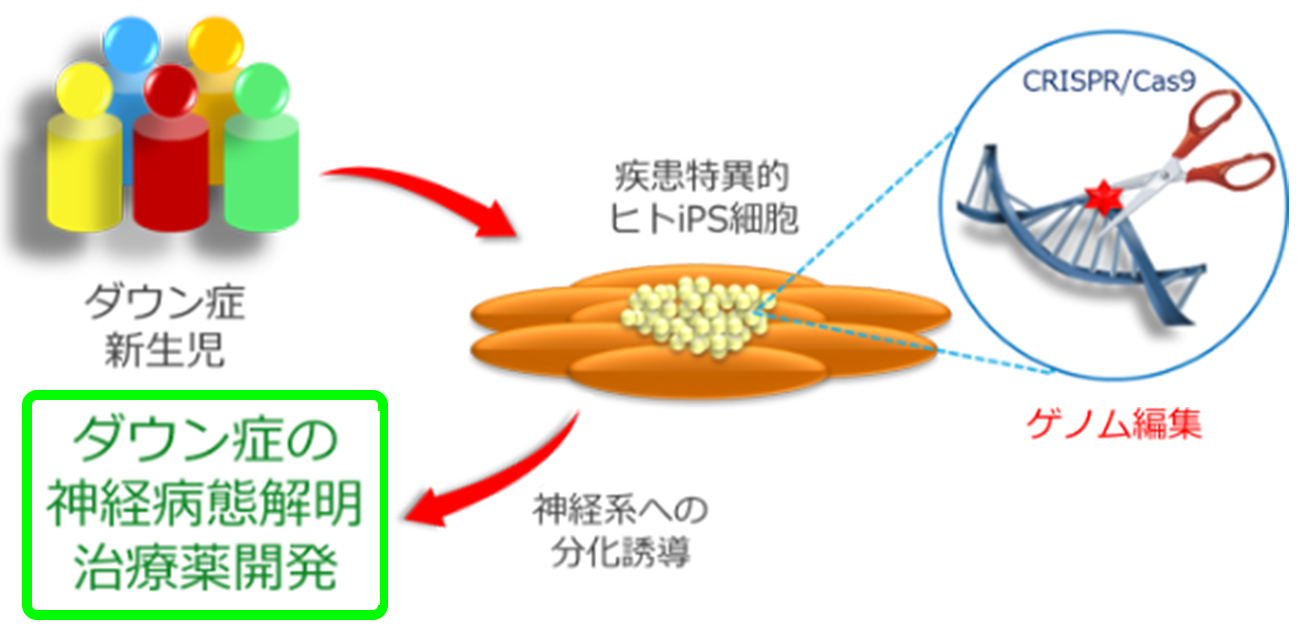
ダウン症児の脳の正常発達を乱す遺伝子を発見
ヒトiPS細胞とゲノム編集技術を駆使し、正確かつ精緻な疾患細胞モデルを樹立
研究成果のポイント
ゲノム編集と呼ばれる新しい遺伝子操作技術をヒトiPS細胞に駆使し、ダウン症候群の疾患モデルを確立
ダウン症候群の知的障害の発症に大きな役割を果たすアストロサイトの異常増殖メカニズムを明らかにし、その責任遺伝子を発見した
ダウン症候群に見られる知的発達障害や認知症の治療法開発の進展に役立つと期待される
概要
大阪大学医学部附属病院 総合周産期母子医療センターの川谷圭司 医員、北畠康司 准教授(小児科)らのグループは、ヒトiPS細胞にゲノム編集技術および染色体工学を組み合わせることで、1人のダウン症候群患者から多様で詳細な疾患モデルiPS細胞を樹立し、同症の知的障害の発症に大きな役割を果たすアストロサイトが異常増殖するメカニズムを明らかにするとともに、その原因遺伝子として21番染色体上にあるDYRK1AとPIGPの同定に成功しました(図1)。
ダウン症候群では多様な合併症が見られます。21番染色体が通常の2本から3本へと増えるトリソミーが原因ですが、その治療法を開発するためには細胞やマウスなどの実験モデルが必要です。しかし正確で適切なダウン症モデルを作成することは簡単ではありません。本研究では、新しい遺伝子操作技術として大きな注目を集めているゲノム編集技術をヒトiPS細胞において駆使することにより、21番染色体を自由自在に改変し、ダウン症候群における『疾患モデルiPS細胞』を樹立しました(図2)。特に神経細胞の維持と病的変化に大きな役割を果たすアストロサイトに注目し、ダウン症細胞モデルをアストロサイト前駆細胞へと誘導して調べることによって、ダウン症候群ではアストロサイトが異常増殖していること、その責任遺伝子がDYRK1AとPIGPの2つであることを見出しました。
本研究成果は、ダウン症患者の知的障害の解明だけでなく、成人期ダウン症の大きな問題となりつつある認知症の診断・治療にもつながる重要な発見であり、今後のダウン症研究を発展させるきっかけになると考えられます。
本研究成果は、2021年6月14日(月)18時(日本時間)、英国の科学誌「Communications Biology」に掲載されました。
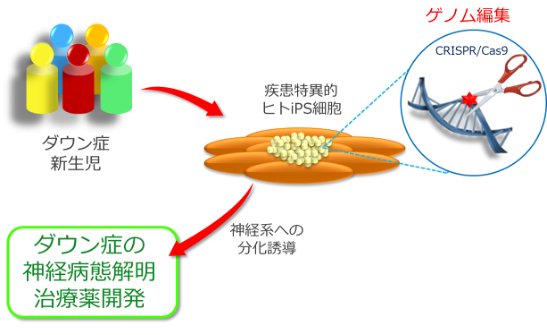
図1. ヒトiPS細胞とゲノム編集技術をもちいたダウン症候群の病態解析
まずダウン症新生児から採取した臍帯血を用いてダウン症特異的iPS細胞を作成しました。このダウン症iPS細胞に、ゲノム編集技術を施すことで、多様な遺伝子改変が可能となります。
このようにして得られたダウン症モデルiPS細胞パネルを、神経細胞やアストロサイトへと分化誘導することで、ダウン症における中枢神経系の病態解明を行うことが可能となります。
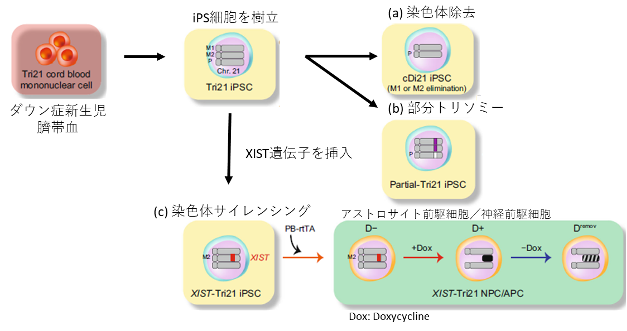
図2. iPS細胞とゲノム編集によるダウン症候群の疾患モデルiPS細胞
(a) 21番染色体を1本除去することで(染色体除去)、ダイソミー細胞を樹立。
(b) ダウン症重要領域と呼ばれる4Mb領域を欠失し、部分トリソミーiPS細胞を樹立しました。
(c) ダウン症iPS細胞に、染色体不活化を引き起こすXIST遺伝子を挿入しました。これにドキシサイクリン(Doxycycline)を加えることで、自由に染色体不活化が起こります。
研究の背景
ダウン症候群は700人に1人という高い頻度で見られ、近年その数はさらに増えつつあります。知的発達障害は同症候群に見られるもっとも重要な合併症ですが、脳のどこに問題があるのかまったく分かっていません。私たちの脳組織はほぼ同数の神経細胞とアストロサイトから構成されるのですが、興味深いことに、ダウン症患者の脳組織では、神経細胞が少なく、アストロサイトが通常の2倍以上存在することが分かってきました。アストロサイトは神経病態形成に深く関わっていることから、「ダウン症ではなぜアストロサイトが異常に多いのか?」を知ることが知的障害の理解と治療法開発につながります。
一方、病気のメカニズムを明らかにするには、正確な実験モデルが不可欠です。しかし、ひとつの遺伝子だけが変化する単一遺伝病とは異なり、ダウン症候群では、330個もの遺伝子をもつ21番染色体が2本から3本に増えることで発症します。このたくさんの遺伝子のうち、いくつの、どの組み合わせの変化が、いったいどのような作用を引き起こして知的障害につながるのか、それを知ることのできる実験モデルはありませんでした。
研究の成果
近年、iPS細胞技術の発明と、さまざまな細胞・動物種における遺伝子操作を可能にする‘ゲノム編集技術’の開発により、正確な疾患モデルを作り出すことが可能になりました。本研究では、ダウン症児の臍帯血から作成したダウン症特異的iPS細胞にゲノム編集を駆使し、以下の改変に成功しました(図2)。
- 染色体を1本減らす(染色体除去)
- ダウン症重要領域だけを欠失する(部分トリソミー)
- 染色体の遺伝子発現をトリソミーからダイソミーへと自由に変化させることができる(染色体サイレンシング)
重要なことは、このようにして得られたiPS細胞は、すべて1人の患者さんの細胞をもとに作られたということです。私たちのゲノム配列はだれでも少しずつ異なっており、その違いが細胞の特性に大きな変化を生じてしまいます。つまり、違う個人から作成したiPS細胞では実験結果に大きな“ぶれ”が生じるのです。しかし今回作成したたくさんのiPS細胞株は、もとになるゲノム配列がまったく単一であり(このような細胞株を遺伝的背景が同一な細胞株;isogenic cell lineと呼びます)、この細胞ごとの“ぶれ”が極めて低くなります。そのため通常なら見逃されるようなわずかな変化も捉えることが可能となったのです。
私たちはこれらのiPS細胞すべてをアストロサイトへと分化誘導し、
- ダウン症では、アストロサイト前駆細胞(まだ未熟なアストロサイト)の段階で、増殖するスピードが著しく早くなる
- ダウン症アストロサイトで増殖速度が増すのは、21番染色体上のDYRK1AとPIGPの2つの遺伝子が原因である
ということを見出しました。しかもDYRK1Aの遺伝子量を3つの対立遺伝子のうちの1つを欠失するだけで、アストロサイトの増殖が正常に戻ることも確認することができました。
興味深いことに、神経前駆細胞(まだ未熟な神経細胞)では、DYRK1Aの過剰発現によって増殖が抑制されました。つまりこのDYRK1Aは、遺伝子数が増えて活性が上がることで、神経前駆細胞の増殖を下げ、一方でアストロサイト前駆細胞の増殖を上げるという二つの役割をもつ重要なファクターであることが分かったのです。
本研究成果が社会に与える影響(本研究成果の意義)
ダウン症候群は、最初の報告から150年という古くからよく知られた疾患ですが、近年妊娠女性の高齢化、新生児医療の発達による生存率の向上、ダウン症候群患者の平均寿命の高齢化など、同症をとりまく社会的環境は大きく変化しています。数百個以上の遺伝子が関与するその病態を明らかにし、治療法の開発を行うことは急務です。
アストロサイトはアルツハイマー病の発症に重要な役割を果たしていると考えられています。そしてダウン症候群の平均寿命が延びるとともに、その90%以上がアルツハイマー病に罹患することが分かり、大きな問題となっています。本研究成果により、ダウン症候群における知的発達障害の原因となるアストロサイトの異常増殖の発症機序が明らかになっただけでなく、成人期に必発する認知症のメカニズムを知る大きな一歩になると考えられます。ヒトiPS細胞とゲノム編集技術を戦略的に組み合わせることで、アストロサイトを標的とした遺伝子治療法の開発に進むことが可能になると思われ、今後同症候群の臨床像が大きく変化すると期待されます。
特記事項
本研究成果は、2021年6月14日(月)18時(日本時間)〔6月14日(月)10時(英国夏時間)〕、英国の科学誌「Communications Biology」に掲載されました。
<論文タイトル>
A human isogenic iPSC-derived cell line panel identifies major regulators of aberrant astrocyte proliferation in Down syndrome
<著者>
川谷 圭司1、南原 利彦1、那波 伸敏1、吉松 秀隆1、日下部 春奈1、平田 克弥1,2、田邉 彰3、隅山 健太3、坂野 公彦1,4、谷口 英俊1、荒堀 仁美1、大薗 恵一1、北畠 康司1
<所属>
1. 大阪大学 大学院医学系研究科 小児科学
2. 大阪母子医療センター 新生児科
3. 理化学研究所 生命機能科学研究センター 高速ゲノム変異マウス作製研究チーム
4. 奈良県立医科大学 生理学第二講座
<研究支援>
本研究は、主に再生医療実現拠点ネットワークプログラム(疾患特異的iPS細胞の利活用促進・難病研究加速プログラム)採択課題「疾患特異的iPS細胞をもちいた小児難治性疾患の統合的理解と創薬開発」の支援により行われました。
用語説明
- ゲノム編集
さまざまな細胞・動物種における遺伝子改変を可能にする新しい技術です。これまでの技術ではできなかったような遺伝子操作を、高い効率で行うことが可能となりました。狙った遺伝子配列にDNA二本鎖切断を導入することで、任意の部位に変異導入・挿入・置換などを行うことができます。CRISPR/Cas9システムは代表的なゲノム編集技術で、その開発者2人は2020年のノーベル化学賞を受賞しています。
- アストロサイト
我々の脳は1000億個以上のニューロンと、その10倍以上ものグリア細胞から成り立っています。アストロサイトは中枢神経系で最も数の多いグリア細胞の1つで、神経細胞に栄養を与えたり、過剰なイオンや神経伝達物質を速やかに除去することにより、神経細胞の生存と働きを助けています。一方で中枢神経の外傷、感染、虚血、変性疾患などのさまざまな病態において重要な役割を果たすことが分かってきており、近年注目を集めています。
- 疾患モデルiPS細胞
ある病気の研究を行うには、まずその病態を再現することが重要です。原因となる遺伝子異常が分かっている場合は、同一の遺伝子異常をもつ細胞あるいは動物を作成し、その遺伝子変化がどのようにして病態を引き起こすのかを一つずつ調べる必要があります。この疾患を再現できる細胞を疾患モデル細胞と呼びます。
