全2工程で!あらゆるタンパク質のN末端に薬剤をつなぐ新技術
バイオ医薬品、検査試薬、タンパク質材料への応用に期待
研究成果のポイント
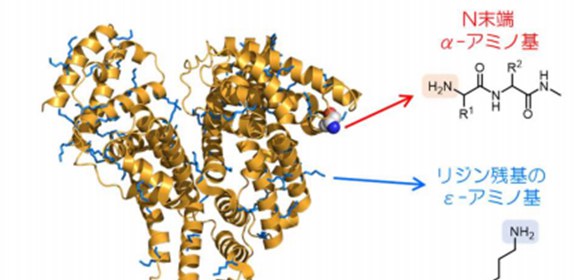
・タンパク質のN末端 に対して選択的に、薬剤などの分子をつなぐ新技術を開発
・タンパク質のN末端へ選択的に分子をつなぐ修飾剤は、これまでは多段階の製造工程が必要でしたが、今回の新技術によって、わずか1工程で修飾剤を製造可能に。
・次の1工程でN末端に選択的に目的の分子を繋ぐことができ、全2工程で可能に。
・バイオ医薬品、検査試薬、タンパク質材料などへの応用に期待
概要
大阪大学大学院工学研究科の小野田晃准教授、大学院生の井上望氏(博士後期課程)、住吉永伍氏(博士前期課程)、林高史教授らの研究グループは、タンパク質のN末端へ選択的かつ簡単に分子をつなぐことができる新技術を開発しました。巨大な分子であるタンパク質の特定部分へ、選択的に分子をつなぐ手法が、バイオ医薬品、検査試薬、タンパク質材料などの幅広い分野で求められています。タンパク質のN末端は、ひも状の構造をもつタンパク質の片方の末端であり、必ず存在する部分であることから、N末端へ選択的に、そして簡単に分子をつなぐ方法が研究されてきました。本技術では、薬剤などの目的の分子を原料に、1工程で修飾剤を製造できます。また、次の1工程でタンパク質のN末端に対して選択的に、目的の分子をつなぐことができます。N末端に分子をつなぐ技術の中で、この新技術は、現在世界で最も簡単、そして実用性の高いもので、タンパク質を利用する幅広いバイオ分野での応用が期待されます。
本研究成果は、Wiley誌「ChemBioChem」の2020年11号に正式公開予定であり、Early viewとして12月3日に先行してオンラインで閲覧可能になっています。
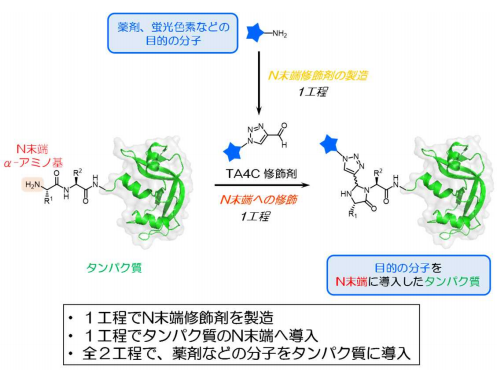
図1 タンパク質のN末端に分子をつなぐ今回の技術の概要
研究の背景
タンパク質は、20種類のアミノ酸 がペプチド結合 でつながったひも状の生体高分子で、折りたたまれた構造をもっており、すべての生物において様々な重要な役割を果たしています。例えば、私たちヒトの血中におよそ6割含まれるタンパク質に、血清アルブミンがあります。血清アルブミンは、585個のアミノ酸がつながったもので、分子量は66,438、化学式はC 2936 H 4590 N 786 O 889 S 41 と9242個の原子からなる巨大な分子です。このような巨大なタンパク質のある特定の一つの原子に対して選択的に、薬剤や材料などの目的の分子をつなぐ技術が近年、大変重要になっています。その一例として、タンパク質である抗体 に薬物をつないだ抗体-薬物複合体が挙げられます。抗体-薬物複合体は、抗体によってがん細胞を標的として認識し、抗体につないだ薬物をがん細胞内に送ることで、がん細胞を攻撃するがん治療薬の一つです。巨大なタンパク質の特定部位に対して、自在に、選択的に、数を厳密にコントロールして、さらに簡単に、目的の分子をつなぐ技術が、バイオ医薬品、検査試薬、タンパク質材料などの幅広い分野で求められています。
研究成果の内容
私たちは、今回の研究成果で、タンパク質のN末端へ選択的に分子をつなぐための修飾剤 1H-1,2,3-トリアゾール-4-カルボアルデヒド(TA4C)を新たに開発しました。TA4Cは、アジド化合物 とアルキン化合物 を原料として、環化付加反応 により高効率で簡単に製造できるため、目的の分子にTA4C部分を簡単につなぐことができます。また、ディムロス転位反応 を活用すれば、目的の分子に含まれるアミノ基を、類似の化合物である1-(4-ニトロフェニル)-1H-1,2,3-トリアゾール-4-カルボアルデヒドと反応することによって、1工程で、N末端修飾剤TA4Cへと変換する製造方法を確立しました。血清アルブミンには、アミノ基を持つリジンが59個含まれていますが、N末端修飾剤TA4Cは、血清アルブミンのN末端アミノ基へ選択的に分子をつなぐことができます。この他にも、リボヌクレアーゼと呼ばれる酵素に対しても、構造を保持したまま、また活性を損なうことなく、N末端へ分子をつなぐことができます。本技術は、全2工程で、あらゆるタンパク質のN末端へ選択的に、薬剤などの目的の分子や材料を導入することができる画期的な手法です。
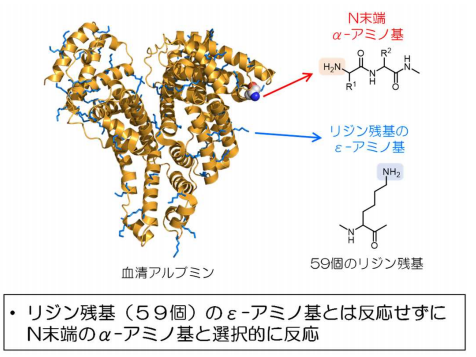
図2 アルブミンタンパク質のN末端に分子をつなぐ例
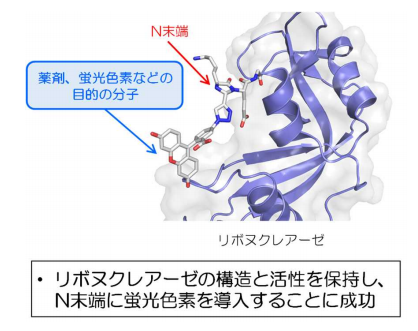
図3 N末端へ目的の分子を導入したリボヌクレアーゼ
本研究成果が社会に与える影響(本研究成果の意義)
これまでタンパク質N末端に選択的に分子をつなぐための修飾剤は、多段階の製造工程が必要でしたが、今回の新技術では、わずか1工程で製造可能になりました。この技術は、現在報告されているN末端選択的なタンパク質修飾法の中で、最も簡単で、高い選択性があります。抗体-薬物複合体やペプチド医薬などのバイオ医薬品、検査試薬、タンパク質材料などへの幅広い応用が期待されます。
研究者のコメント
タンパク質N末端へ分子をつなぐ今回の技術は、私たち自身がタンパク質を使った基礎研究を進める過程で、より簡単に、かつ有用な手法の必要性に気付いて開発しました。簡単さを追求した結果、有機合成を専門としない、医学、生物、材料の研究者はもちろん、一般の方も利用できる方法に至りました。この技術を、イノベーションジャパン2019で紹介後、製薬企業、化学企業、試薬・検査試薬企業から問い合わせを多数うけていますので、今後、医学、生物学の基礎応用の両面で幅広く波及効果が期待されます。
特記事項
本研究成果は、Wiley誌「ChemBioChem」の2020年11号に正式掲載の予定であり、Early viewとして12月3日に先行してオンラインで閲覧可能になっています。
タイトル:“Triazolecarbaldehyde Reagents for One-step N-Terminal Protein Modification”
著者名:Akira Onoda, Nozomu Inoue, Eigo Sumiyoshi, and Takashi Hayashi
なお、本研究は科学研究費補助金、基盤研究(JP17H05370、JP18H04651、JP15H05804)、JST SICORP および特別研究員奨励費のサポートを受けて実施されました。
参考URL
大阪大学 大学院工学研究科 応用科学専攻 物質機能化学講座 構造有機化学領域 林研究室
http://www.applied-bioinorganic.jp/jp/
用語説明
- N末端
(アミノ末端):
タンパク質を構成するペプチド鎖の端に位置するアミノ酸残基のうち、アミノ基を有するものです。もう一方の端でカルボキシル基を有するものをC末端(カルボキシル末端)と呼びます。
- アミノ酸
アミノ基(-NH 2 )とカルボキシル基(-COOH)の両方を同一分子内にもつ有機化合物で、タンパク質の主要成分です。
- ペプチド結合
タンパク質やペプチド(アミノ酸が2個以上つながったもの)中で、アミノ酸残基間を結合する酸アミド結合の一種で、-CONH-で表されます。一方のアミノ酸のα-カルボキシル基と、他方のアミノ酸のα-アミノ基が脱水縮合することによって生成する化学結合です。
- 抗体
抗原に特異的に結合するタンパク質で、抗原刺激の結果による免疫反応によって生体内に誘導されます。
- アジド化合物
-N 3 で示される化合物です。
- アルキン化合物
分子内に三重結合を1つ持つ脂肪族不飽和炭化水素の総称です。
- 環化付加反応
付加反応に伴って、非環状化合物が環状化合物になる反応で、アジド化合物とアルキン化合物を原料した場合は、ヒュスゲン双極子環化付加と呼ばれます。この反応は、ノーベル賞を受賞したSharpless博士により提唱されたクリックケミストリーを代表しており、クリック反応とも呼ばれます。
- ディムロス転位反応
環内または環外のヘテロ原子(炭素、水素以外の原子)、およびヘテロ原子を含んだ置換基が、開環と閉環を経て転位を起こすヘテロ環の異性化反応をディムロス転位と呼びます。
