
ポリリン酸が引き起こす蛋白質異常凝集体の形成機構を解明
高齢者に多いアミロイド病の予防・治療の進展に貢献
研究成果のポイント
・透析アミロイドーシスの原因となるβ2ミクログロブリンのアミロイド線維(蛋白質異常凝集体)の形成を、ポリリン酸が促進することを発見し、さらにその機構を解明しました。
・ポリリン酸はさまざまなアミロイド病に関わり、アミロイド線維形成を促進している可能性があります。
・ポリリン酸に焦点を当てた研究を展開することにより、様々なアミロイド病の予防や治療の進展が期待できます。
概要
大阪大学蛋白質研究所後藤祐児教授のグループは、新潟大学医学部、福井大学医学部、ハンガリーのエトヴァッシュ・ローランド大学と共同で、透析アミロイドーシス(アミロイド病) の原因蛋白質であるβ2ミクログロブリンのアミロイド線維形成 が、ポリリン酸によって促進されることを発見しました。ポリリン酸はリン酸が数珠状に結合した生命活動に必須の生体高分子です (図1) 。また、リン酸は緩衝液としてよく使われる塩ですが、蛋白質の凝集傾向を示すホフマイスター系列 によると、凝集を誘導する作用が強い塩の一つです (図1) 。これまでに、ポリリン酸がいくつかのアミロイド線維の形成を促進することが、報告されています[Cremers et al., Mol. Cell 63, 768–780 (2016)]。しかし、β2ミクログロブリンのアミロイド線維形成については不明であり、また、これらに共通する促進機構も不明でした。ポリリン酸が引き起こすアミロイド線維の一般的な促進機構が明らかになったことで、高齢化社会の深刻な病気であるアミロイド病の予防や治療の進展につながることが期待されます。
なお、本研究成果は米国科学アカデミー紀要(Proceedings of the National Academy of Sciences of the UnitedStates of America)に2019年6月10日(月)(米国時間EST)に掲載されました。
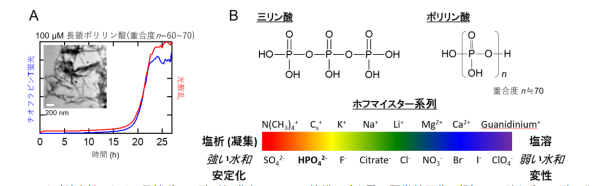
図1 (A)中性における長鎖ポリリン酸が促進するアミロイド線維形成と電子顕微鏡画像、(B)三リン酸とポリリン酸の化学構造(上)とホフマイスター系列(下)。
研究の背景
蛋白質はアミノ酸配列によって様々な天然構造を形成して機能を発現します。一方、蛋白質が変性して凝集すると、アミロイド線維と呼ばれる幅が10ナノメータ-で長さが数マイクロメーターの針状の凝集体を形成します (図2) 。また、アモルファス凝集体と呼ばれる不定形な凝集を形成することもあります。現在、35種類以上の蛋白質がアミロイド線維を形成して、アルツハイマー病、パーキンソン病、透析アミロイドーシスなどの様々な疾患の発症に至ることがわかっています。
透析アミロイドーシスは、長期の血液透析を行う患者に発症するアミロイド病であり、蛋白質β2ミクログロブリンのアミロイド線維によって引き起こされます。血液透析患者では、血中のβ2ミクログロブリンの濃度が上昇しますが、それだけではアミロイド線維の形成反応は引き起こされず、凝集体形成のトリガーとなる物質や機構は不明です。
ポリリン酸は、生体に必須の分子であり、大腸菌や酵母ではATP(アデノシン三リン酸)のリン酸のリザーバーとして機能していることが知られています。哺乳類ではポリリン酸は血小板に含まれていますが、その役割は未だ不明です。これまでに、ポリリン酸がいくつかのアミロイド線維の形成を促進することが報告されていますが、β2ミクログロブリンのアミロイド線維形成をはじめ一般的な促進機構については不明でした。一方、食品にポリリン酸は添加物として多く含まれており、ポリリン酸による強い水和作用により、食品を乾燥から保護するなどの役割があります。
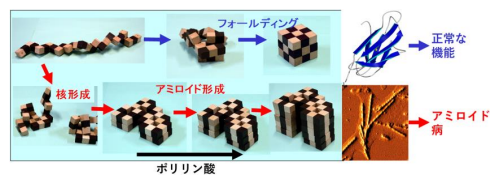
図2 蛋白質のフォールディングとアミロイド線維形成のイメージ。
本研究成果の内容
アミロイド線維形成反応
本研究グループでは、鎖長の異なる様々なポリリン酸を用いて、超音波 照射下で、β2ミクログロブリンの凝集体の形成反応を測定しました( 図1 , 3 )。その結果、β2ミクログロブリンが変性した酸性溶液中ではポリリン酸の鎖長に依存して、アミロイド線維とアモルファス凝集体の形成が促進されました (図3) 。中性溶液中ではβ2ミクログロブリンは天然構造を形成していますが、生体濃度に匹敵する極めて低い濃度の長鎖ポリリン酸存在下において、アミロイド線維形成が引き起こされることが分かりました (図1) 。
ポリリン酸によるアミロイド線維の形成の化学的機構
酸性溶液中では、ポリリン酸は負電荷をもち、蛋白質は等電点より低いため正電荷を帯びており、電荷-電荷相互作用によりアミロイド線維形成を促進します (図4) 。中性溶液中ではポリリン酸と蛋白質は、両者とも負電荷を帯びており、互いに反発します。水和したポリリン酸が蛋白質周りに集まる選択的水和により、アミロイド線維形成が促進されると考えられます (図4) 。
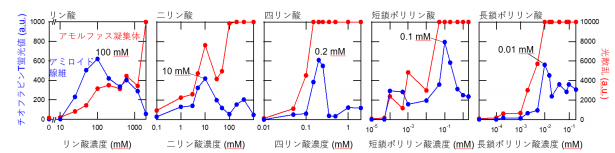
図3 酸性溶液中、様々な鎖長のポリリン酸存在下におけるアミロイド線維形成。
アミロイド線維形成はチオフラビンT蛍光測定により、アモルファス凝集体形成は光散乱により測定した。青い点が高いとアミロイドが多くできている。ポリリン酸の鎖長が長くなるほど、アミロイド線維形成が最大となるポリリン酸濃度は低下した。
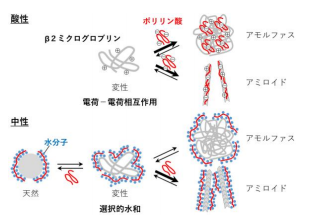
図4 酸性(上)と中性(下)におけるポリリン酸が促進するアミロイド線維の形成機構。
本研究成果が社会に与える影響(本研究成果の意義)
ポリリン酸は生体に必須な分子ですが、塩析作用が強く、水分子を強く引き付ける性質があります。中性では、ポリリン酸の選択的水和により、蛋白質はよりコンパクトな天然構造をとり、さらには、アミロイド線維を形成することがわかりました。血液透析治療を長期間続けると、β2ミクログロブリンのアミロイド線維形成が引き起こされますが、この過程においてもポリリン酸のような分子が関わっているものと推察されます。その他、アルツハイマー病やパーキンソン病、糖尿病をはじめ高齢化社会の深刻な病気のほとんどに蛋白質の異常凝集が関わります。ポリリン酸による異常凝集体形成は、蛋白質の種類によらない一般的な反応です。その機構が明らかになったことで、今後、生体のポリリン酸の濃度を正確に測定する技術を開発することができれば、アミロイド病の予防や治療の進展につながると期待されます。
特記事項
本研究成果は米国科学アカデミー紀要(Proceedings of the National Academy of Sciences of theUnited States of America)の電子版に2019年6月10日(月)(米国時間EST)に掲載されました。
タイトル:Possible mechanisms of polyphosphate-induced amyloid fibril formation of β2-microglobulin
(ポリリン酸が促進するβ2 ミクログロブリンのアミロイド線維形成の想定される機構)
著者名:Chun-ming Zhang, Keiichi Yamaguchi, Masatomo So, Kenji Sasahara, Toru Ito, Suguru Yamamoto, Ichiei Narita, József Kardos, Hironobu Naiki, and Yuji Goto
(張 春明、山口 圭一、宗 正智、笹原 健二、伊藤 徹、山本 卓、成田 一衛、József Kardos、内木 宏延、後藤 祐児)
なお、本研究は、大阪大学蛋白質研究所共同研究(CR-15-02)、同国際共同研究(ICR-16-02)、科学研究費補助金新学術領域研究(17H06352)、日本学術振興会・研究拠点形成事業(A型)、AMED先端計測分析技術・機器開発プログラムの一環として行われました。
参考URL
大阪大学 蛋白質研究所 蛋白質構造形成研究室
http://www.protein.osaka-u.ac.jp/physical/yoeki.html
用語説明
- アミロイド線維形成
変性蛋白質が凝集するとゆで卵の白身のように不定形の凝集だけを形成すると考えられていました。ところが図2にイメージするように規則正しく積み重なっていくタイプの凝集(アミロイド線維)も存在することがわかっています。アミロイド線維の形成は、水に溶けた物質が結晶として析出する場合と似た性質を示し、過飽和(あるいは過冷却)状態から、何かのきっかけで突然生じる他、シード(種)があると形成が促進されます。
- 透析アミロイドーシス(アミロイド病)
アミロイド病(あるいはアミロイドーシス)は変性蛋白質がアミロイド線維を沈着して発症する病気の総称であり、アルツハイマー病、パーキンソン病、透析アミロイドーシスをはじめとする数十種類の疾患が含まれます。アミロイド病には高齢化に伴い発症するもの(孤発性)、遺伝的な原因で若年で発症するもの(家族性)がありますが、透析アミロイドーシスは透析患者だけが発症するという特徴をもっています。現在は、透析技術の改良により透析アミロイドーシスの発症リスクは下がってきていますが、発症機構は依然、不明です。
- ホフマイスター系列
蛋白質の溶解度や安定性に及ぼす塩効果の順列であり、これに従って蛋白質の塩析や塩溶などの作用が起きます。
- 超音波
超音波照射によって生じるキャビテーション、または、かく拌により、蛋白質の凝集体形成が促進されます。本研究では、様々な鎖長のポリリン酸存在下において、超音波を周期的に照射して、アミロイド線維形成実験を行いました。
