ALS等の発症の鍵を握る蛋白質Ataxin-2の機能を特定
神経難病の解明への貢献に期待
本研究のポイント
・筋萎縮性側索硬化症(ALS) や遺伝性脊髄小脳変性症などの発症の鍵を握るAtaxin-2が、RNAの安定性を制御する蛋白質であることを発見。
・次世代シーケンサーを用いて、Ataxin-2の結合する標的 RNA(リボ核酸) やRNA中の結合部位を網羅的に決定。
・神経変性疾患で認められる遺伝子変異は、Ataxin-2によるRNA安定化機能を低下させることを発見。
・パーキンソン病など複数の神経変性疾患に共通する発症メカニズムの解明につながることが期待される。
リリース概要
大阪大学大学院医学系研究科ゲノム生物学講座(神経遺伝子学)の河原行郎教授らの研究グループは、筋萎縮性側索硬化症(ALS)、遺伝性脊髄小脳変性症2型(SCA2)、パーキンソン病などの複数の神経変性疾患の発症の鍵を握るAtaxin-2蛋白質の機能を明らかにしました。これまでAtaxin-2は神経変性疾患に関連することは知られていましたが、具体的にどのような機能を持っているのか不明でした。
本研究グループは、PAR-CLIP法と呼ばれる蛋白質に結合するRNAを高純度に精製する手法と、次世代シーケンサーを用いた解析を組み合わせ、Ataxin-2に結合するRNAとその結合部位を網羅的に決定することに成功しました。その結果、Ataxin-2が、RNAの安定化を促進する蛋白質であることを突き止めました。また、ALSやSCA2で認められている遺伝子変異が、Ataxin-2のRNA安定化機能を低下させることも発見したことから、神経変性疾患に共通した発症病態の解明や将来的に新たな治療法を確立することにつながることが期待されます。
なお、本研究成果は、米国科学誌Molecular Cellの電子版に6月19日(木曜日)12時(米国東部時間)に掲載されます。
研究の背景
ALSやパーキンソン病などに代表される神経変性疾患は、超高齢化社会の到来と共に、今後患者数が益々増加すると予測されています。しかし、一方で、病態解明と治療法確立が遅れており、根治可能な治療法は確立していないのが現状です。脊髄小脳変性症は、小脳や脳幹が主に障害される神経変性疾患の一種で、約30%が遺伝性です。その一型であるSCA2は、Ataxin-2蛋白質中にあるポリグルタミン鎖(グルタミンの繰り返し配列)の異常伸長が原因です。通常、健常人ではグルタミン数は26個以内ですが、SCA2では遺伝子変異によって34個以上に伸長しています (図1) 。また、Ataxin-2のポリグルタミン鎖が異常伸長した患者の中には、パーキンソン病と同様の症状を呈する方もいます。更に、最近では、Ataxin-2のポリグルタミン鎖の中等度伸長(27-33個)が、ALSの発症を高める危険因子となることが判明しています (図1) 。このように、遺伝子変異によるAtaxin-2のポリグルタミン鎖の異常伸長は、様々な神経変性疾患に共通した発症病態に関与することが明らかとなっています。しかしその一方で、Ataxin-2がそもそもどのような機能を持った蛋白質なのか長年に渡って不明であったことから、遺伝子変異が病気を引き起こすメカニズムについても謎でした。
一方、近年実用化された次世代シーケンサーと呼ばれる高速シーケンス機器を用いることによって、DNAやRNAの塩基配列を高速かつ網羅的に決定できるようになりました。これまで、ある蛋白質がDNAやRNAなどの核酸に結合することが知られていても、詳細に解析することは技術的に限界がありました。しかし、最近では、蛋白質に結合する核酸を精製できれば、次世代シーケンサーを使って、何種類くらいの核酸のどの部分に結合するのかを詳細に明らかにし、その性状から機能を予測することも可能となりました。
今回、本研究グループは、Ataxin-2がRNAに結合する蛋白質であることを発見し、これを突破口とし、次世代シーケンサーを使って、結合しているRNAを網羅的に決定することに成功しました。また、結合している部位などから機能を予測し、Ataxin-2がRNAの安定性を促進する蛋白質であることを突き止めました。更に、Ataxin-2の標的が分かったことから、遺伝子変異によるポリグルタミン鎖の異常伸長が、Ataxin-2の機能を減弱させることを明らかにすることに成功しました (図2) 。
本研究成果が社会に与える影響(本研究成果の意義)
これまで、Ataxin-2は、ALS、SCA2、パーキンソン病などの発症に関連していることが知られていましたが、具体的な機能は特定されていませんでした。今回、RNAの安定性を制御する蛋白質であることが明らかとなり、また疾患と関連する遺伝子変異が、この機能を低下させることが分かりました。これらの標的となるRNAの中には、神経細胞の生存に必要不可欠なものや、神経変性疾患の発症と強く関連するRNAなどが含まれていることが明らかとなりました。今後、これらの標的RNAを更に詳細に解析することによって、神経変性疾患の発症メカニズムを解明し、今後の神経変性疾患の新たな治療戦略の確立に大きく貢献することが期待されます。
特記事項
掲載誌:米国科学雑誌Molecular Cell(6月19日付け:米国東部時間12時・電子版)
論文タイトル:Direct Binding of Ataxin-2 to Distinct Elements in 3’UTRs Promotes mRNA Stability and Protein Expression
著者:Moe Yokoshi, Quan Li, Munetaka Yamamoto, Hitomi Okada, Yutaka Suzuki, Yukio Kawahara
なお、本研究は、鈴木穣教授 (東京大学大学院新領域創成科学研究科)との共同研究です。
参考図
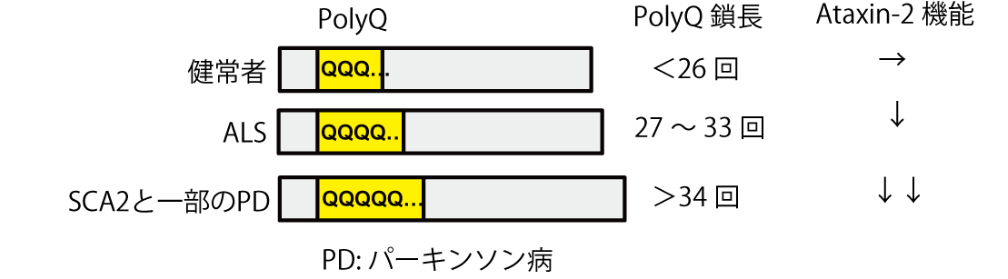
図1 Ataxin-2のポリグルタミン(PolyQ)鎖長と神経変性疾患の関係
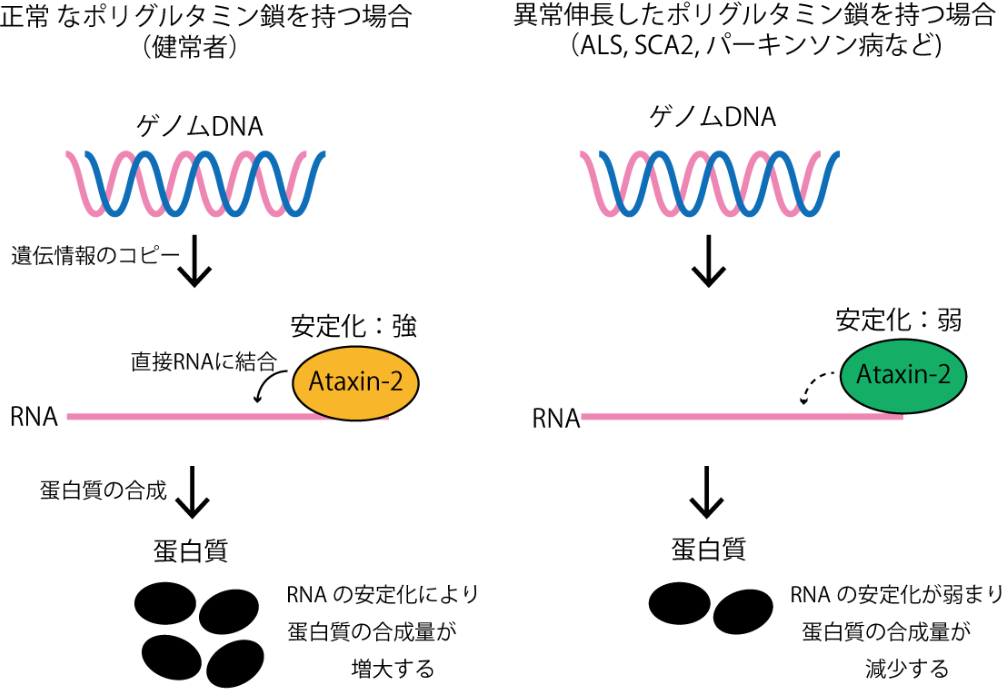
図2 ポリグルタミン鎖伸長によるAtaxin-2のRNA安定化機能の低下
参考URL
大阪大学大学院医学系研究科 医学専攻ゲノム生物学神経遺伝子学
http://www.med.osaka-u.ac.jp/jpn/activities/results/2014/002.html
用語説明
- 筋萎縮性側索硬化症(ALS)
脊髄(下位)および大脳皮質(上位)にある運動神経細胞が変性し、全身の筋力が低下していく神経変性疾患。90%以上に遺伝性がなく、遺伝性のないケースでは、発症原因が不明である。運動神経細胞だけが選択的に障害される一方で、感覚や知能が保たれる。急速に進行するケースが多く、発症してから数年以内に呼吸不全となり、人工呼吸器などのアシストが必要になる。治療方法は確立していない。基本的には、中年期以降に発症する。日本には約9000人弱の患者がいる。
- RNAの安定性
ゲノムDNAに載った遺伝情報は、RNAへとコピーされ、RNA上の情報をもとに蛋白質が合成される。このため、RNAは遺伝情報の中間産物的な位置づけにあり、DNAに比べて不安定であることから、蛋白質が合成される前に分解されてしまうものも一定量存在する。したがって、RNAの安定性は、蛋白質の合成量を左右する重要な因子である。RNA結合蛋白質の中には、RNAに結合し保護することによって、安定性を促進するものもあるが、一方で分解を促進するタイプのものもある。
- 次世代シーケンサー
核酸の塩基配列を、高速・多並列に読む(シーケンス)ことができる機器。従来は、Sanger法(第一世代)が使われてきたが、一回に処理できる量が限られていた。最新の次世代シーケンサーを用いれば、ヒトのゲノムDNA全長を一日でシーケンスすることも可能である。
- RNA(リボ核酸)
DNA(デオキシリボ核酸)と同じ核酸の一種。ゲノムDNAにコードされている遺伝情報は、RNAへとコピーされ、RNA上の情報をもとにして蛋白質が合成される。このように、RNAは情報伝達の介在役として機能を果たす。
- パーキンソン病
中脳の黒質にあるドーパミン産生細胞が減少することによって、手足の震え、固縮などの運動障害を呈する神経変性疾患。90%以上に遺伝性がなく、遺伝性のないケースでは、発症原因が不明である。日本だけでも、14万人近い患者がいる。現在の治療は、不足したドーパミンを補充する対症療法が主体であり、根治療法はない。基本的には、中年期以降に発症する。Ataxin-2の遺伝子変異は、稀にSCA2よりもパーキンソン病に近い症状となって発症する患者もおり、数自体は多くないが、パーキンソン病患者の中には、本遺伝子変異を保有する人がいる。
- 遺伝性脊髄小脳変性症2型(SCA2)
脊髄小脳変性症は、主に小脳、脳幹、脊髄などの様々な神経細胞が障害され、ふらつき、ろれつが回らない、むせるなどの症状を呈する神経変性疾患。このうちの約30%程度に遺伝性があり、現在40近い原因遺伝子が同定されている。SCA2は、この中の1つであり、Ataxin-2をコードしている遺伝子の変異によって生じる。患者数は非常に少ない。発症年齢は2歳から60歳ほどと幅広い。
- PAR-CLIP法
2010年にアメリカのロックフェラー大学のグループによって開発された手法。細胞に発現するRNA結合蛋白質に結合するRNAを、高純度に抽出することができる。しかし操作が煩雑であることから、世界的にも限られた研究室でしかできない。
- ポリグルタミン鎖
アミノ酸の一種であるグルタミンの繰り返し配列からなる部位。いくつかの蛋白質中に存在していることが知られており、ポリグルタミン鎖の異常伸長によって引き起こされる病気をポリグルタミン病と総称する。SCA2以外にも、ハンチントン病(ハンチンチンと呼ばれる蛋白質中にあるポリグルタミン鎖の異常伸長が原因)など9疾患が同定されている。
- RNAに結合する蛋白質
RNA結合蛋白質:
DNAに結合しうる蛋白質をDNA結合蛋白質、RNAに結合しうる蛋白質をRNA結合蛋白質と総称する。RNA結合蛋白質は、ヒトには約1000種類程度あると予測されており、RNAの合成や成熟過程などに関与しているが、具体的な標的RNAや機能が特定されているのは、全体のごく一部に過ぎない。
