制御性T細胞による免疫寛容 その発見と臨床への展望
Nobel Prize Lecture "Regulatory T Cells for Immune Tolerance: Discovery and Clinical Prospects"
坂口志文特別栄誉教授ノーベル賞受賞記念講演 ダイジェスト
スウェーデンの首都ストックホルムにあるカロリンスカ研究所の講堂「アウラ・メディカ」。2025年12月7日、坂口志文特別栄誉教授はここでNobel Prize Lecture(受賞記念講演)に臨み、研究成果の集大成を世界に向けて発信しました。制御性T細胞の発見から機能解明に至るひとつひとつの軌跡と、臨床応用につながる研究の意義を丁寧に語り終えると、満員の会場は、長く、大きな拍手に包まれました。約30分の講演内容をダイジェストでお送りします。

はじめに
ご来賓の皆さま、ご列席の皆さま。今年の生理学・医学部門のノーベル賞をメアリー・ブランコウ氏とフレッド・ラムズデル氏と共に受賞でき、非常に光栄で嬉しく思います。この賞に私たちを選んでくださったノーベル委員会とカロリンスカ研究所のノーベル会議に感謝します。本日は、免疫寛容における制御性T細胞の役割についてお話しします。
免疫寛容と制御性T 細胞
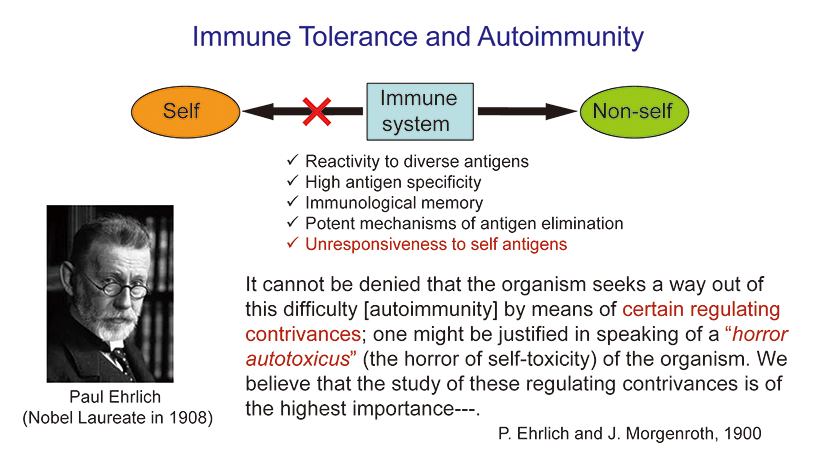
免疫系は侵入してくる病原菌から私たちの体を守るものです。T細胞とB細胞といった免疫系は多様な抗原※1に対する反応性、高い抗原特異性、免疫学的記憶、そして抗体やT細胞を介した強力な抗原除去メカニズムを持っています。通常、免疫系は自己を攻撃しません。
20世紀初めの学者パウル・エールリッヒは、免疫系は私たち自身の体と反応しないと考えていましたが、その一方で自己免疫から私たち自身を守るような一定の調節機構が必要とも述べました。
※1 抗原:抗原は、通常病原体の外側に存在しています。抗原は病原体ごとにバラエティに富んでいますが、免疫系の「抗原特異的な抗体」またはリンパ球表面の「抗原特異的な受容体」と結合します。抗体に結合された抗原を持つ病原体は失活して無毒化します(中和反応)。(「阪大微研のやわらかサイエンス 感染症と免疫のQ&A」より)
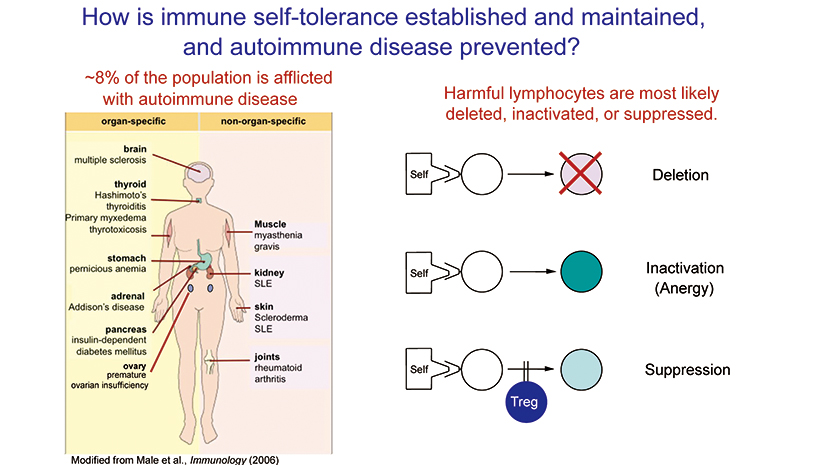
それ以来、適切でない免疫反応を調節する仕組みである免疫寛容について、いくつかのメカニズムが提案されました。1つ目は、自己免疫を起こすT細胞やB細胞が除去される「排除」。2つ目は、共刺激をなくすことによる免疫細胞の「不活性化」。そして3つ目が「抑制」です。「抑制」の考え方においては、通常の個体は、潜在的に危険な自己反応性の免疫細胞を持っているかもしれませんが、それらの活性化や増殖は別のT細胞集団によって制御されています。これが、私たちが発見した「制御性T細胞(Treg)」と呼ぶものです。
免疫学の重要な課題は、「これらのメカニズムのどれかが機能しなくなった場合に自己免疫疾患が発生するかどうか」です。自己免疫疾患は推定で人口の約8 %の人々が苦しんでいると言われています。
マウスによる実験で存在を確認
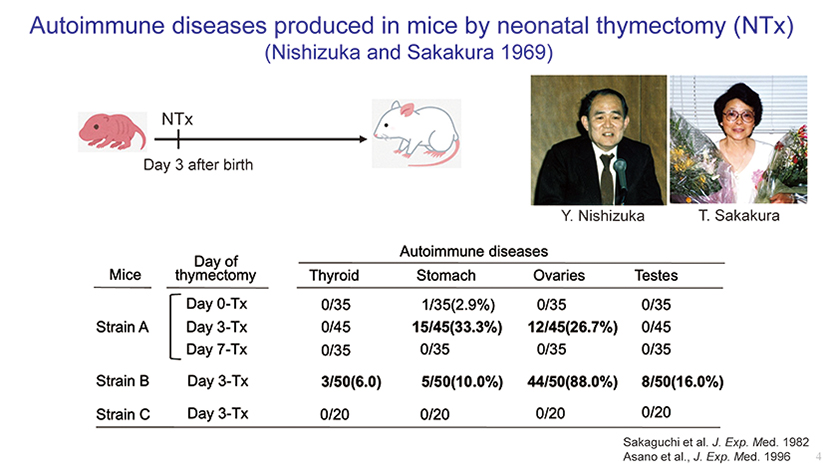
1969年に西塚泰章氏と坂倉照妤氏は、マウスの胸腺を生後3 日頃に除去するとさまざまな自己免疫疾患が起こることを発見しました。これをもとに私たちは、新生仔胸腺摘出がどのように自己免疫疾患を引き起こすのかについて実験し、結果を以下のように考察しました。
① 生後0 日目に胸腺を摘出すると、自己免疫疾患は発生しなかった⇒自己反応性T細胞も制御性T細胞も生成されないため
② 生後7 日目に胸腺を摘出すると、自己免疫疾患は発生しなかった⇒既に十分な数の制御性T細胞が末梢に存在しているため
このことを確かめるため、正常な大人のマウスにおいて、制御性T細胞と自己免疫性T細胞の分離を試み、また、制御性T細胞のみを直接除去することで自己免疫疾患を誘発するかを実験しました。
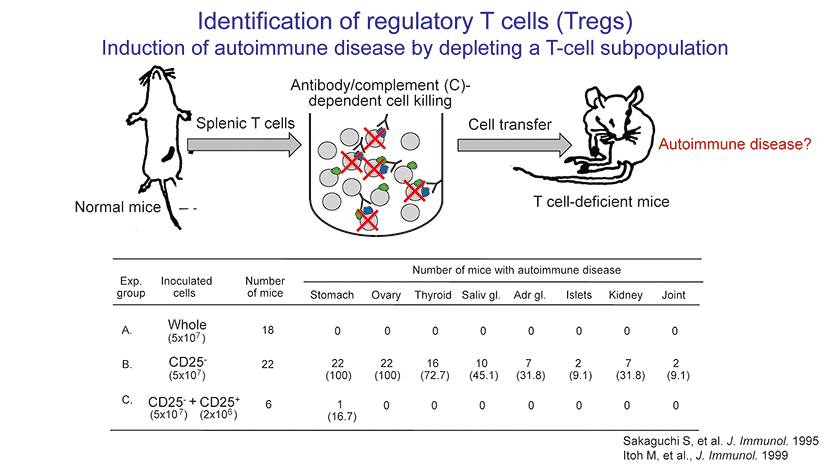
CD5、CD45RBといった細胞表面の分子マーカーを手がかりに研究を進め、最終的に特異的な分子マーカーとしてCD25に辿り着きました。
CD25を発現するT細胞を無くした状態のマウスには、様々な自己免疫疾患が発症しました。その後CD25陽性細胞群、つまり制御性T細胞を加え戻すと、疾患の発展を抑制できることも確認しました。
CD25を持つ制御性T細胞は胸腺で生成されますが、成熟に時間がかかります。そのため、新生仔の胸腺を生後3 日頃に摘出すると、この細胞だけが選択的に減少し、結果として自己免疫疾患が引き起こされることが示唆されました。
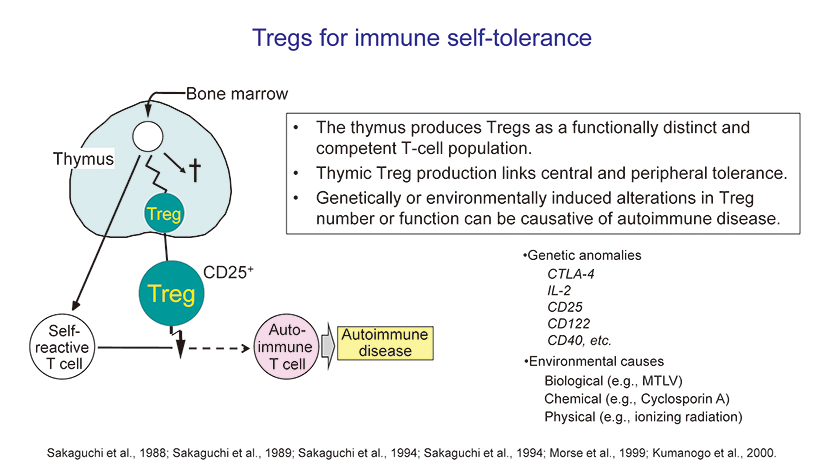
T細胞は、胸腺内で成熟した細胞集団に分化します。自己に強く反応するT細胞はここで除去され(中枢性免疫寛容)、自己に中程度親和性を有するものが制御性T細胞となります。自己に弱く反応するT細胞は胸腺で作られますが、普段は制御性T細胞によって反応を抑えられています(末梢性免疫寛容)。制御性T細胞が中枢と末梢の免疫寛容をつないでいるのです。そして私たちは、ウイルスや化学物質、放射線などの環境因子による制御性T細胞の減少が、自己免疫疾患を引き起こすことを明らかにしました。がんなどのような遺伝子そのものの変異ではなく、細胞集団の異常が自己免疫疾患の本質だったのです。
Foxp3遺伝子の発見
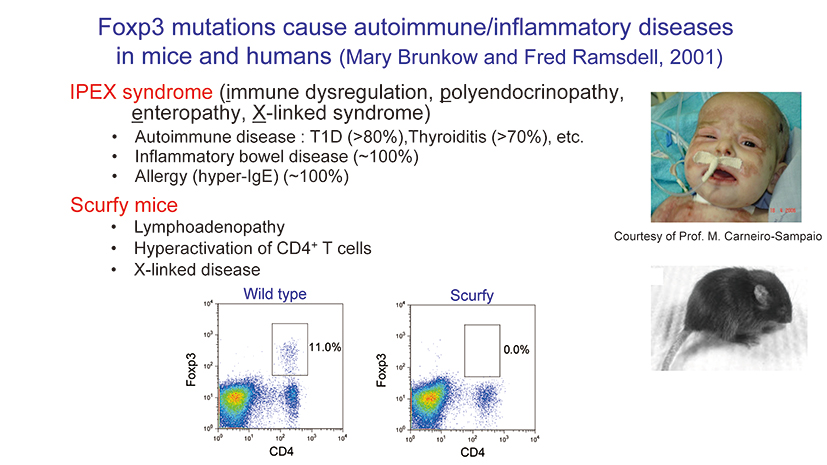
次の課題は、このようなメカニズムがヒトでも機能しているかどうかという点です。2001年にメアリー・ブランコウ氏とフレッド・ラムズデル氏は、重度の全身性自己免疫疾患を示すマウスの原因遺伝子を突き止め、「Foxp3」と命名し、これはヒトの稀な自己免疫疾患であるIPEX症候群の原因遺伝子であることを示しました。
私たちの研究グループも、IPEX症候群の症状が、制御性T細胞を除去したマウスの症状と酷似していたことから、その原因遺伝子であるFoxp3に注目しました。Foxp3を認識する抗体を作って解析した結果、Foxp3は制御性T細胞で特異的に発現する遺伝子であることを、私たちを含む3 グループが発表しました。マウスだけでなくヒトにおいても、Foxp3が欠損していると制御性T細胞が存在できず、重篤な自己免疫疾患が起こります。こうして、ヒトの免疫においても、制御性T細胞が働いていることが確かめられたのです。
自己と非自己の境界は動く
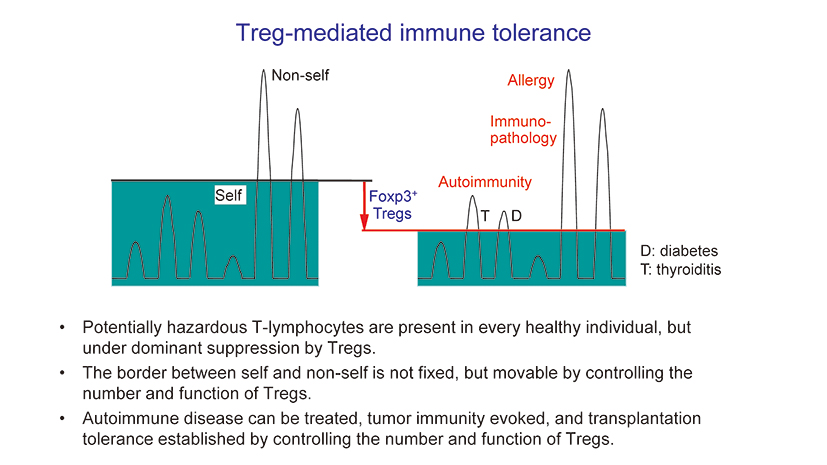
守られる「自己」と攻撃される「非自己」の境界は固定されたものではなく、制御性T細胞の数や機能をコントロールすることで移動可能なものなのです。免疫学者が好んで用いる「自己-非自己識別」という言葉、しかしその境界線は制御性T細胞を増加または減少させることで、移動させることができます。これは、自己免疫疾患の治療や、腫瘍(がん)への免疫の強化、臓器移植後の拒絶反応の抑制が、制御性T細胞のコントロールによって可能になることを意味します。
腫瘍に関しては、制御性T細胞が存在するマウスに腫瘍細胞を接種すると、腫瘍は大きくなります。しかし制御性T細胞を除去すると、腫瘍に対する免疫応答が活性化し、腫瘍を拒絶できるようになります。
移植の場合は、制御性T細胞を増やすことで、他のマウスからの皮膚移植に対する拒絶反応が抑制され、生着する割合が増加します。免疫抑制薬なしで移植寛容を誘導できるのです。
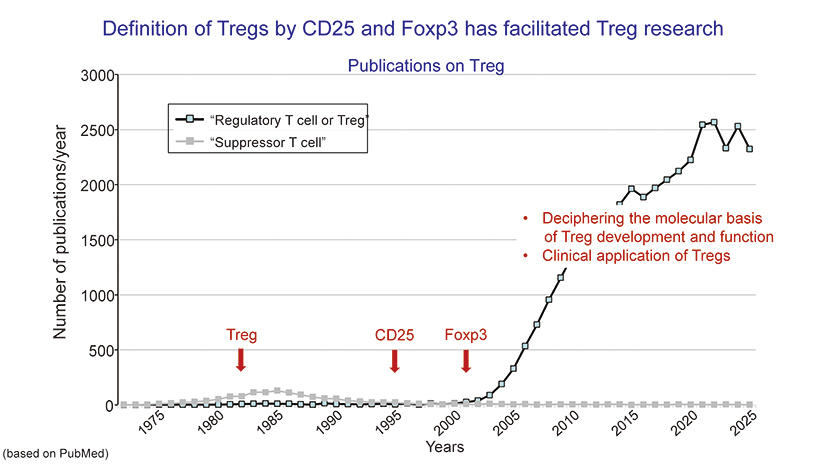
制御性T細胞は、CD25を細胞表面の分子マーカーとして、Foxp3を核内の特異的マーカーとして特定されたことで、明確な細胞集団として定義されました。これにより世界中で制御性T細胞に関する論文数も急速に増加し、特にその発生と機能における分子の動きが解明されてきました。
制御性T細胞の分子メカニズム
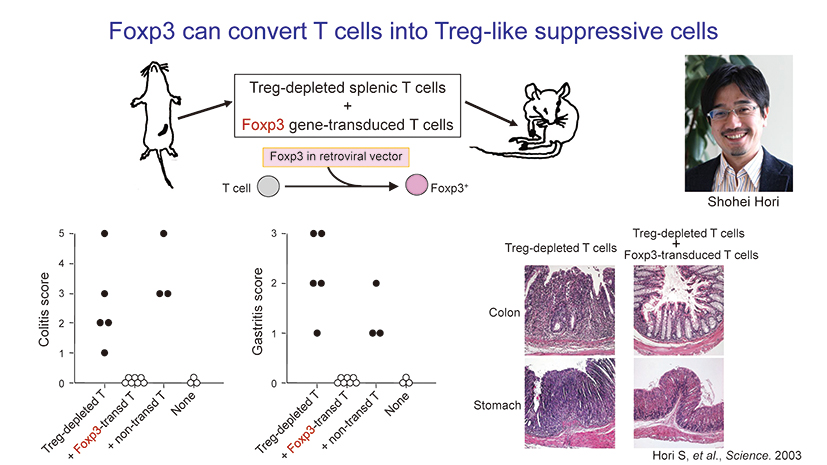
私の研究室に所属していた堀昌平氏の研究から、Foxp3遺伝子が通常のT細胞に自己免疫疾患を抑制する能力を与えることが示され、その後Foxp3が制御する数百種類の遺伝子の中でも、IL-2(インターロイキン2※2)とその受容体が重要であることがわかりました。制御性T細胞はIL-2がないと生存できませんが、自らIL-2を産生することはできません。実際に、体内のIL-2を除去すると制御性T細胞が減少し、重度の自己免疫疾患が起こります。
※2 IL-2(インターロイキン2):免疫細胞から分泌されるサイトカイン(タンパク質によるメッセージ)の一群。T細胞を活性化する。
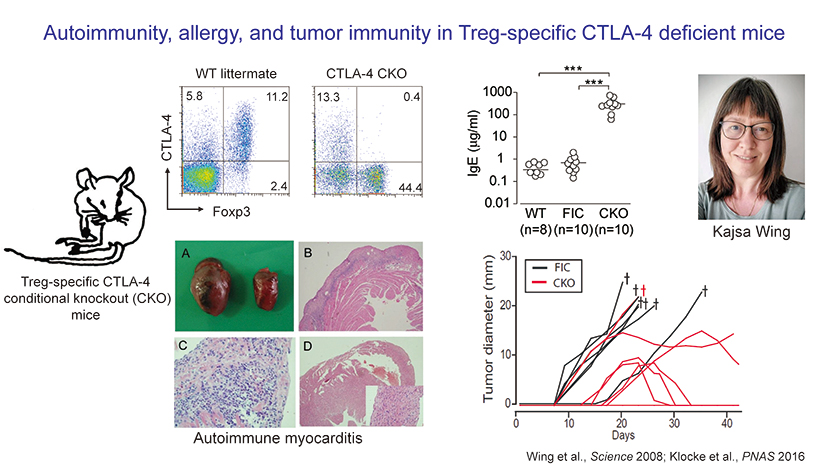
CTLA-4は、T細胞の表面にあり、免疫応答の過剰な活性化を抑制する分子です。私の研究室の研究員であったスウェーデン出身のカイサ・ウイング氏は制御性T細胞だけでCTLA-4を欠損させたマウスが自己免疫疾患を発症し、腫瘍免疫も強くなることを示しました。これは制御性T細胞を除去した場合とよく似ており、CTLA-4が制御性T細胞の機能に不可欠であることを裏付けています。
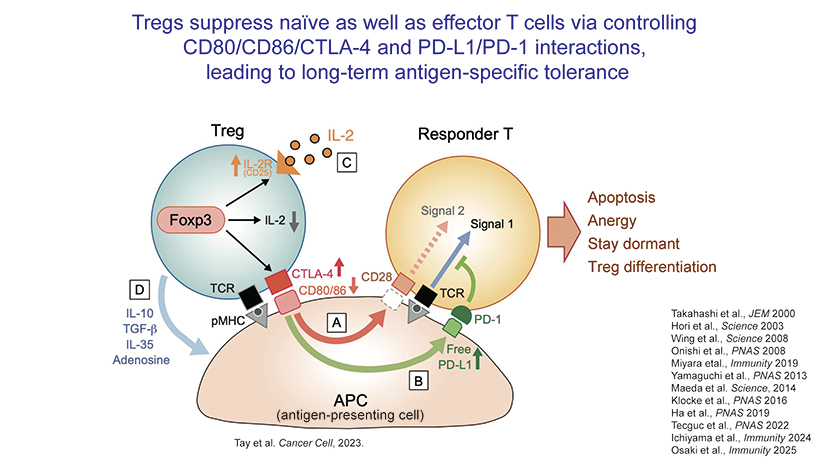
人口の約8 %に影響していると言われる一般的な多遺伝子性自己免疫疾患についてはどうでしょうか。私たちの解析では、制御性T細胞機能に関する主要遺伝子の変異が制御性T細胞の発達や機能を弱めていることがその本質的な主因であることが分かりました。
この他にも多段階的な仕組みで、制御性T細胞が免疫応答抑制を実現していることが明らかになりました。特に、主要分子( Foxp3、CD25、CTLA-4 )の異常は重度の自己免疫疾患(Tregopathy)を引き起こします。
治療への応用
制御性T細胞を標的とする疾患治療法について述べます。まず、制御性T細胞の増加です。低用量のIL-2を使用することで、制御性T細胞のみを増やすことができます。これによって免疫寛容を強化することができます。
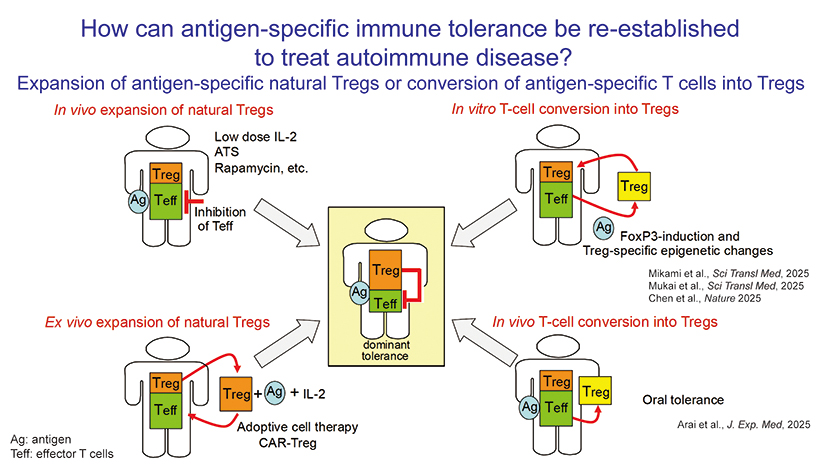
また、体内の血液中に存在する制御性T細胞を採取して培養によって増やし、それを患者に再移植する方法もあります。
さらに別の方法として、私たちは、通常のT細胞をin vivo(生体内)またはin vitro(試験管内)で制御性T細胞に変換する方法に取り組んでいます。これにより、非常に安定した制御性T細胞を生成でき、患者に移入することで疾患の進行を抑えることができます。
このように、制御性T細胞は、間もなく臨床応用が可能になります。制御性T細胞を増やし、その機能を強化することで、自己免疫疾患、アレルギー、炎症性腸疾患(IBD)などの様々な免疫疾患を治療することができます。また、臓器移植の成功や、流産の防止にも活用できる可能性があります。
一方で、制御性T細胞の機能を減少させることで免疫応答を強化することもできます。これは、腫瘍(がん)の治療に有効です。
おわりに

これまでの研究に関して、多くの方々のご支援に御礼を申し上げます。まず妻の教子に感謝しています。彼女は私の人生のパートナーであり、共同研究者でもあります。そして、西塚泰章氏と坂倉照妤氏にも感謝しています。お二人は、新生仔胸腺摘出によって自己免疫疾患を引き起こす方法を教えてくださいました。また、高橋利忠先生には抗体を用いてT細胞集団を分離する方法を教えていただきました。
これまで多くの同僚、学生、共同研究者と協力して研究を進めてきました。ここで言及した方々以外にも、多くの方が制御性T細胞の研究に貢献してくださいました。また、日本およびアメリカの資金提供機関にも心から感謝申し上げます。
ご清聴ありがとうございました。

■動画で見る
2025年ノーベル生理学・医学賞受賞記念講演(Nobel Prize公式)
◆ 坂口 志文(さかぐち しもん) プロフィール
1951年滋賀県生まれ。76年京都大学医学部卒業。77年愛知県がんセンター研究所研修生、83年京都大学大学院医学研究科で博士(医学)。米国にてジョンズホプキンズ大学卒後研究員、スタンフォード大学客員研究員、スクリプス研究所助教授などを務めた後、99年京都大学再生医科学研究所教授、2007年同所長。11年より大阪大学免疫学フロンティア研究センター教授となり、16年大阪大学名誉教授、京都大学名誉教授。同年から大阪大学免疫学フロンティア研究センター特任教授(常勤)。19年に文化勲章を受章。25年大阪大学特別栄誉教授。
過剰な免疫反応を抑える制御性T細胞を発見し、免疫疾患における意義を解明。25年に「末梢性免疫寛容に関する発見」により、メアリー・ブランコウ氏、フレッド・ラムズデル氏と共にノーベル生理学・医学賞を受賞。
(本記事は、2026年2月27日発行の大阪大学NewsLetter 94号に掲載されたものです。)
