定説を覆す発見!分裂酵母が独特の核膜孔複合体アウターリング構造を持つことを解明
真核生物の進化の解明につながる発見
研究成果のポイント
・真核生物の細胞内では核と細胞質の間を分子が行き来するとき、「核膜孔複合体 」という構造を通るが、これまでその構造はどの生物でも同じだと考えられていた
・分裂酵母の核膜孔複合体を構成するタンパク質が核膜孔の中でどの位置にあるのかを初めて明らかにし、核膜孔複合体の土台となるアウターリング構造 において他の生物と全く異なる配置をとっていることを発見
・核膜孔複合体の構造の多様性に注目することにより、核膜孔の進化的成り立ちだけでなく、細胞核の構造や機能の進化について理解する手がかりとなる発見
・核膜孔の異常によって起こる疾病の理解につながる成果として期待
概要
大阪大学大学院生命機能研究科の淺川東彦准教授、平岡泰教授の研究グループは、情報通信研究機構未来ICT研究所の原口徳子主任研究員の研究グループおよび大阪大学大学院理学研究科の小布施力史教授の研究グループとの共同研究で、分裂酵母の核膜孔複合体 (図1) のアウターリング構造 (図2) が、他の生き物で従来知られている構造とは全く異なっていることを世界で初めて明らかにしました。
真核生物において、細胞内の分子は核と細胞質の間を行き来する際に「核膜孔複合体」と呼ばれる核膜に空いた穴のような構造体を通過します。これまで、核膜孔複合体の構造および、その土台となるアウターリング構造は、どの生物でも基本的に同じ構造を取っていると考えられてきました。近年では、このアウターリング構造を形成するタンパク質の変異が、ヒトの腎疾患であるネフローゼ症候群の原因になることから、この構造のもつ特性と機能および、疾病との関連が注目されています。
共同研究チームは、免疫電子顕微鏡法 および、蛍光顕微鏡による高精度測定法によって、核膜孔複合体アウターリングの構造は、全真核生物で必ずしも共通ではなく、生物種によって多様な構造をとるということを示しました。
本研究成果は、核膜孔複合体因子の変異による病気の理解に貢献するものと期待されます。また、真核細胞は、進化の過程において、核と細胞質を核膜によって区画化すると同時に、両者の間で分子輸送をおこなうために核膜孔という分子の通り道を作り出しました。本研究で見いだされた核膜孔アウターリング構造の違いは、真核生物の起源の解明にも繋がる重要な発見と言えます。
本研究成果は、米国科学誌「PLOS Genetics」に、6月7日(金)午前3時(日本時間)に公開されました。
図1 核膜孔複合体とアウターリングの模式図
核膜孔複合体は核膜を貫通した八回回転対称の筒状の構造体である。筒状構造の内部を分子が通過することによって核と細胞質の間の分子輸送が行われる。アウターリング構造(青色)は、ヒトや出芽酵母では核膜孔複合体の核内側と細胞質側の両方に見られるリング状の構造体である。
図2 アウターリングの模式図
1つのアウターリングはY字型の構造をもった複合体(Nup107-160サブ複合体)が8つ連なってできる。出芽酵母とヒトでは、それぞれ7または10種類の異なるタンパク質が集まってひとつのサブ複合体を形成する。
研究の背景
真核生物の細胞内では核と細胞質を隔てる核膜と呼ばれる膜構造が存在します。核膜孔複合体は、核と細胞質との間で細胞内分子を輸送するための通過孔として核膜上に存在しています。1個の核膜孔複合体は、約千個のタンパク質で出来ています。しかし、その種類は約30種類程度と少なく、かつ構成タンパク質は真核生物の間でほぼ共通していることから、核膜孔複合体の構造は全ての真核生物で共通と考えられてきました。アウターリング(Outer ring)は、核膜孔の核内側および細胞質側に対称的に配置することによって、核膜孔複合体を支える土台となる最重要構造と考えられています。アウターリングの構造は、ヒトと出芽酵母という進化的に離れた生物でも極めて類似していることが分かっており、それ故に「すべての」真核生物の間で共通であると考えられていました。しかし、分裂酵母のアウターリング構造を構成するタンパク質は、これらの代表的なモデル生物のアウターリング構成タンパク質とは発現パターンが異なっていること、また、他の生物にはない構成タンパク質を含んでいることから、分裂酵母の核膜孔複合体アウターリングは、従来知られているものとは異なる構造である可能性が考えられました。
本研究の成果
研究グループは、免疫電子顕微鏡法による解析および蛍光顕微鏡画像の分析をおこない、分裂酵母の核膜孔複合体を構成するおよそ30種類のタンパク質が核膜孔の中のどの位置にあるのかを決定しました。その結果、ヒトや出芽酵母では、アウターリングタンパク質は、それぞれ核膜孔の核内側と細胞質側の両側に配置しているのに対して、分裂酵母では、一部のタンパク質は核内側に、その他は細胞質側にと、分かれて配置していることがわかりました (図3) 。一方で、アウターリング構造以外の核膜孔複合体タンパク質は、ヒトや出芽酵母と同じように配置していました。ヒトや出芽酵母では、アウターリングタンパク質は、それぞれが核内側(図3では下側)と細胞質側(図3では上側)の両方に同じ量ずつ存在しており、上下で対称な構造であることが分かっています。今回の成果は、分裂酵母では、アウターリングが2つの部分に分割され、それぞれが核膜孔複合体の中で核内側と細胞質側に分かれて配置していることを示しています。アウターリング構造は、核内側と細胞質側の両方に同量ずつ存在することが定説となっていることから、分裂酵母で発見された構造は、ヒトや出芽酵母といった今までのモデルとは全く異なるものです (図4) 。
また、アウターリング構造のうち核内側のタンパク質が細胞質側に配置されるように遺伝子改変した分裂酵母を作製したところ、細胞の分裂が異常になることを発見しました。このことは今回発見された特殊な非対称配置が分裂酵母にとって必要なものであることを示すものです。
本研究は、核膜孔複合体アウターリング構造が、それぞれの種に都合の良いように、多様に進化してきた構造体であることを示す重要な発見であると言えます。
図3 分裂酵母の核膜孔複合体タンパク質の局在解析
アウターリングを構成するタンパク質の位置を免疫電子顕微鏡画像から解析し、核膜孔複合体の核内側(緑)、内部(赤)、細胞質側(青)にわけて集計した結果を示す。アウターリングを構成するタンパク質は、核内側と細胞質側にはっきりと分かれた局在を示すことがわかった。
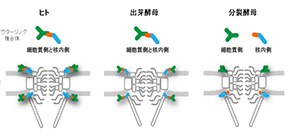
図4 ヒト、出芽酵母、分裂酵母の核膜孔複合体のモデル図
本研究成果から考えられるアウターリングの構造および核膜孔複合体の構造の違いを示す模式図。
本研究成果が社会に与える影響(本研究成果の意義)
核膜孔複合体のアウターリング構造は核膜孔の中で極めて重要な構造と考えられてきたため、どの生物でも、基本的に同じ構造を取っていると考えられてきましたが、本研究成果により、極めて自由度の高い構造として進化してきた可能性が見えてきました。このことはこれまでの定説を覆す全く新しい概念であり、今後の核膜孔複合体の構造や役割に関する研究を大きく進展させる重要な発見です。
また、最近、アウターリング構造の変異が、腎疾患であるネフローゼ症候群の原因になるという研究成果が報告されています。病気との関連を知る上でも、本研究成果は重要な知見を与えるものとなります。今後は、各構成パーツや各構成タンパク質の機能を調べることにより、核膜孔複合体因子の変異による病気の理解に貢献することができるものと期待されます。
特記事項
本研究成果は、2019年6月6日(木)14時(米国東部時間)〔6月7日(金)3時(日本時間)〕に米国科学誌「PLOS Genetics」(オンライン)に掲載されました。
タイトル:“Asymmetrical localization of Nup107-160 subcomplex components within the nuclear pore complex in fission yeast”
著者名:Asakawa H (1), Kojidani T (2,3), Yang HJ (1), Ohtsuki C (1), Osakada H (2), Matsuda A (2), Iwamoto M (2), Chikashige Y (2), Nagao K (4,5), Obuse C (4,5), Hiraoka Y (1,2), Haraguchi T (1,2)
(1)大阪大学大学院生命機能研究科
(2)情報通信研究機構未来ICT研究所
(3)日本女子大理学部
(4)北海道大学生命科学院
(5)大阪大学大学院理学研究科
なお、本研究は、上原記念生命科学財団(原口徳子)、中華民国科技部(楊惠如)、日本学術振興会科学研究費補助金新学術領域研究(研究領域提案型)「クロマチン機能を保証する核膜の構造と分子基盤(研究代表者:原口徳子)」、同新学術領域研究(研究領域提案型)「再構成とエピゲノム編集による初期胚核の機能性獲得機序の理解(研究代表者:山縣一夫)」、同新学術領域研究(研究領域提案型)「ヘテロクロマチンの構造と機能の理解(研究代表者:小布施力史)」、同新学術領域研究(研究領域提案型)「ヘテロクロマチンの凝縮構造を作り出すノンコーディングRNA群の解明(研究代表者:長尾恒治)」、同新学術領域研究(研究領域提案型)「染色体上の非コードRNAが動的クロマチン構造を制御する仕組み(研究代表者:平岡泰)」、同新学術領域研究(研究領域提案型)「減数分裂における細胞核・クロマチン構造の変換メカニズム(研究代表者:平岡泰)」、日本学術振興会科学研究費補助金基盤研究A(平岡泰)、同基盤研究B(原口徳子、小布施力史)、同基盤研究C(淺川東彦、岩本政明、近重裕次、長尾恒治)、同挑戦的研究(萌芽)(原口徳子)の一環として行われました。
研究者のコメント
淺川東彦(あさかわはるひこ)(=米国科学雑誌「PLOS Genetics」誌掲載論文の第一著者)
「分裂酵母が、定説とは全く異なるアウターリング構造を持つことがわかった時は大変驚いた。今回の発見は、細胞核の構造と特性を解明する上で重要であるだけでなく、生命の多様性や進化の理解にも繋がる大きな発見であると考えている。」
参考URL
大阪大学大学院生命機能研究科 細胞ネットワーク講座 細胞核ダイナミクス研究室
http://www.fbs.osaka-u.ac.jp/labs/hiraoka/preface.html
用語説明
- 核膜孔
(核膜孔複合体):
核膜を貫通するチャンネル状の構造。この構造を通じて、核と細胞質の間で物質が輸送される。核膜孔を構成するタンパク質複合体のことを核膜孔複合体といい、進化的に保存されたおよそ30種類の特異的なタンパク質が複数コピーずつ集まって構成されている (図1参照) 。酵母の細胞の核膜には100個から200個、動物の細胞の核膜には1000個から5000個の核膜孔複合体があると言われている。
- アウターリング構造
核膜孔複合体の中で、核内側と細胞質側に見られるリング状の構造体。ヒトや出芽酵母では、7個から10個のタンパク質がひとつのY字型複合体を形成しており、それがさらに8個連なることによってリングを形成している (図2参照) 。このようなリング構造がヒトでは核内側に2つ、細胞質側に2つあるとされ、出芽酵母では核内側に1つ、細胞質側に1つあるとされている。
- 免疫電子顕微鏡法
化学架橋剤で固定した細胞を使って、目的のタンパク質を抗体で染色し樹脂で固めたものを、極めて薄く切った切片にして観察する方法。切片に含まれる細胞内の構造を同時に染色することにより、目的のタンパク質が細胞の微細構造のどの部分に局在するのかがわかる。
