有機合成反応で乳がん手術を改革
迅速・簡易・安価な手術中がん診断技術を世界基準へ
研究の概要
理化学研究所(理研)開拓研究本部田中生体機能合成化学研究室の田中克典主任研究員、アンバラ・プラディプタ基礎科学特別研究員、盛本浩二客員研究員、大阪大学大学院医学系研究科の多根井智紀助教、野口眞三郎教授、カザン大学のアルミラ・クルバンガリエバ准教授らの国際共同研究グループ は、乳がんの手術中に摘出した組織で有機合成反応を行うことにより、乳がん細胞の有無だけでなく、がんのさまざまな種類(形態)を従来よりもはるかに短い時間で、簡易に識別できる診断技術を開発しました。
本研究成果は、従来の手術中における病理学的診断法に代わって、今後、乳がん切除範囲を迅速・簡易・安価に判断する世界基準の診断技術として活用されると期待できます。
田中主任研究員らは以前、酸化ストレス 条件下で、細胞で発生する「アクロレイン 」が蛍光基を持つ「アジドプローブ 」と有機合成反応し、細胞を蛍光標識できることを見いだしていました。今回、国際共同研究グループは、この有機合成反応を用いて、さまざまなヒトがん細胞でアクロレインが多量に発生していることを突き止めました。さらに、乳がん手術で摘出した“生”の組織にこの手法を適用したところ、わずか数分で97%の高感度でがん細胞の有無を判別し、かつさまざまな種類の乳がんを識別することに成功しました。
本研究は、ドイツの科学雑誌『Advanced Science』のオンライン版(11 月 27日付け)に掲載されました。

図 手術中に切除する乳がん部位を迅速に見極める新しい診断技術
※国際共同研究グループ
理化学研究所
開拓研究本部 田中生体機能合成化学研究室
主任研究員 田中 克典 (たなか かつのり)
基礎科学特別研究員 アンバラ・プラディプタ(Ambara Pradipta)
テクニカルスタッフⅡ 藤井 素子 (ふじい もとこ)
客員研究員 盛本 浩二 (もりもと こうじ)
国際プログラム・アソシエイト(研究当時) エレナ・サイジトバタロバ(Elena Saigitbatalova)
環境資源科学研究センター ケミカルゲノミクス研究グループ
専任研究員(研究当時) 伊藤 昭博 (いとう あきひろ)
グループディレクター 吉田 稔 (よしだ みのる)
大阪大学 大学院医学系研究科乳腺・内分泌外科学
助教 多根井 智紀 (たねい とものり)
教授 野口 眞三郎 (のぐち しんざぶろう)
病態病理学
准教授(研究当時) 池田 純一郎 (いけだ じゅんいちろう)
教授 森井 英一 (もりい えいいち)
カザン大学 生体機能化学研究室(理研-カザン連携研究室)
准教授 アルミラ・クルバンガリエバ(Almira Kurbangalieva)
※研究支援
本研究は、科学技術振興機構(JST)戦略的創造研究推進事業個人型研究(さきがけ)の研究領域「分子技術と新機能創出」(研究総括:加藤隆史)研究課題名「生体内合成化学治療:動物内での生理活性分子合成」(研究者:田中克典)の一環として行われました。
背景
乳がんは、日本人女性で最も患者数の多いがんであり、12人に1人の割合で罹患することが知られています 注1) 。現在、乳がん切除手術では、乳房の膨らみを残して乳腺を部分のみ切除する「乳房温存手術」が多く実施されています。この「乳房温存手術」では、手術中に端の乳腺組織(断端)での顕微鏡による診断(術中迅速組織診断)を行い、がんが残っていないかどうかを確認し、断端にがんが残っていた場合には、さらに乳腺組織を追加して切除することで、できるだけ乳がんを取り残さないように多くの病院で努力しています (図1) 。また、退院後に最終的な顕微鏡検査(病理組織診断)で切除断端にがんが残っていた場合には、再度切除手術を行うことになり、乳がん手術の断端検査を厳密に行うことは患者にとっても大変重要です。
現在、手術中における断端検査には、ヘマトキシン・エオジン染色法(HE染色法)と呼ばれる病理学的診断が利用されています。HE染色法では、摘出した断端を凍結して切片にし、HE試薬を用いて染色した後、顕微鏡でがん細胞を検出しますが、1回の検査に40分程度を要します。この間、全身麻酔の状況の患者と執刀医は結果を待つ必要があります。一方で、検査をする病理医の数が非常に少ないことも問題でした (図1) 。そこで、乳がん患者の手術中の負担を減らし、都市の大病院から地方の病院に至るまで、多くの患者の手術を短時間で簡便に実施できる新しい迅速術中診断技術を開発することが求められていました。
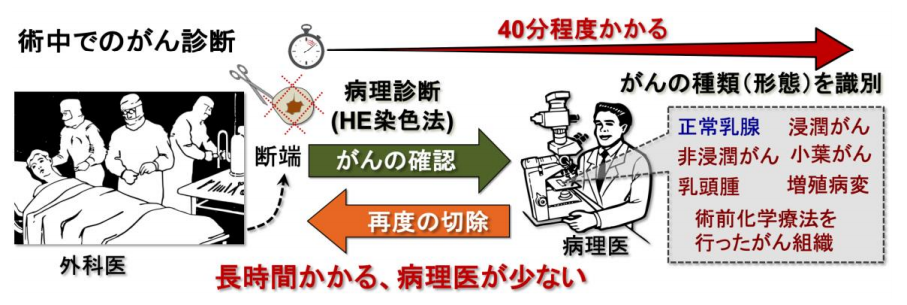
図1 乳がんの術中診断に用いられている病理学的診断(HE染色法)
乳がんの手術でがん細胞が残っているか否かを調べるため、摘出したがん断端を凍結切片にして、HE染色を行う。HE染色は、さまざまな乳がんの種類(浸潤がん、非浸潤がん、小葉がん、乳頭がん、増殖病変など)を的確に判別できる反面、時間がかかり、画像の識別には、病理医の経験が必要とされる。
2016年に田中主任研究員らは、酸化ストレス条件下で細胞内に発生する毒性の「アクロレイン」とテトラメチルローダミン(TAMRA)蛍光基を持つ「アジドプローブ」が選択的に反応し、1,2,3-トリアジン化合物が速やかに生成されることを見いだしました 注2) 。この1,2,3-トリアジン化合物がさらに細胞内で複数の有機合成反応を経ることにより、細胞中に蛍光基がとどまります。この蛍光基を利用してアクロレインを生成している細胞を1細胞レベルで蛍光標識できます (図2) 。

図2 アジドプローブを用いたアクロレインを発生する細胞の蛍光標識
酸化ストレスの条件下で発生する毒性のアクロレインは、細胞内でアジドプローブと選択的に[2,3]-双極子環化反応を起こして、1,2,3-トリアジン化合物が速やかに生成する。細胞内における低pH環境下で、1,2,3-トリアジン化合物はジアゾ化合物へと変換される。ジアゾ化合物が細胞内のさまざまなタンパク質と反応した結果、蛍光基が細胞中にとどまり、1細胞レベルで蛍光標識される。なお、図の赤丸の「蛍」はTAMRA蛍光基を示す。
一方で、がん細胞は酸化ストレス細胞であることが知られています。そこで、国際共同研究グループは、アクロレインとアジドプローブを用いることで、がん細胞だけを蛍光標識できる可能性があると考えました。
注1)Hori M, Matsuda T, Shibata A, Katanoda K, Sobue T, Nishimoto H, et al. Cancer incidence and incidence rates in Japan in2009: a study of 32 population-based cancer registries for the Monitoring of Cancer Incidence in Japan (MCIJ) project.Japanese journal of clinical oncology. 2015;45(9):884-91.
注2)2016年4月12日プレスリリース「アクロレインの可視化に成功」
http://www.riken.jp/pr/press/2016/20160412_2/
研究手法と成果
国際共同研究グループはまず、がん細胞でアクロレインが多量に発生しているか否かを調べました。3種類の正常細胞および乳がん細胞を含む8種類のがん細胞のそれぞれの培養液に対してアジドプローブを作用させた後、顕微鏡で蛍光観察を行ったところ、正常細胞に比べて、がん細胞で蛍光強度が著しく増大しており、それぞれの細胞が示す蛍光強度は、細胞が生産するアクロレインの量と比例することから、アクロレインががん細胞で選択的に多量発生していることが分かりました (図3) 。
この方法で蛍光標識されたがん細胞をより詳しく調べたところ、がん細胞の中で選択的に複数の有機合成反応が進行したことが分かりました。これにより、さまざまながん細胞でアクロレインが多量に発生していることが初めて実験で示されました。
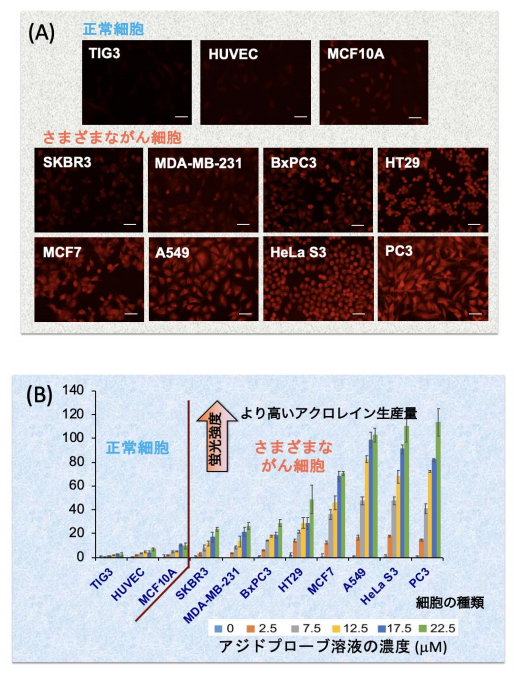
図3 正常細胞とがん細胞から発生するアクロレインの検出
(A)3種類の正常細胞と8種類のがん細胞の培養液にアジドプローブを作用させた後、蛍光顕微鏡により観察した画像。正常細胞は、左からヒト肺線維芽細胞(TIG3)、ヒト臍帯静脈内皮細胞(HUVEC)、ヒト乳腺上皮細胞(MCF10A)を用いた。がん細胞は、左上からヒト乳がん細胞(SKBR3)、ヒト乳がん細胞(MDA-MB-231)、ヒト膵がん細胞(BxPC3)、ヒト結腸細胞(HT29)、ヒト乳がん細胞(MCF7)、ヒト肺がん細胞(A549)、ヒト子宮頚部がん細胞(HeLaS3)、ヒト前立腺がん細胞(PC3)を用いた。スケールは10μm(1μmは1,000分の1mm)。
(B)細胞に異なる濃度のアジドプローブを作用させて蛍光を測定した結果。アクロレインががん細胞選択的に多量発生していることが分かる。
次に、手術中に摘出した“生”の乳がん組織にアジドプローブとアクロレインを反応させることにより、がん細胞を選択的に蛍光標識できるかを、乳がん組織とその周辺の正常組織を用いて調べました(合わせて60例)。その結果、手術中に患者から摘出した乳がんの断端をアジドプローブ溶液に5分間浸すだけで、97%の高い確率でがん細胞を判別できることが分かりました (図4) 。
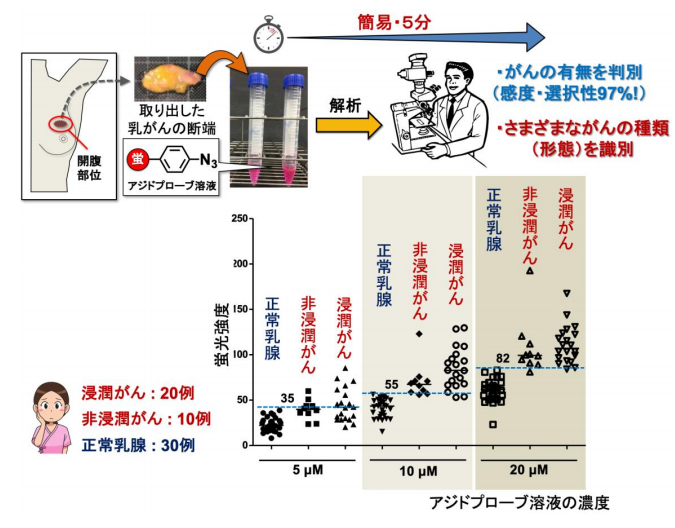
図4 アジドプローブを用いた乳がん患者から摘出したがん細胞の判別結果
乳がん患者の手術で摘出したがん(20例の浸潤がんと10例の非浸潤がん)と正常乳腺(30例)の断端をそれぞれアジドプローブ溶液に5分間浸した後、顕微鏡で観察し蛍光強度を測定した。20μM(1μMは100万分の1M)のアジドプローブ溶液を使用することで、がんの有無を感度・選択性ともに97%の高い確率で判別できた。
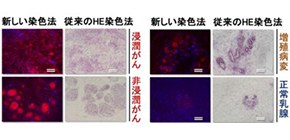
個々のがん細胞はさまざまな方式で集まり、さまざまな種類(形態)のがんを形成します。 図2 で示すように、アジドプローブを用いるとがん細胞を1細胞レベルで蛍光標識できるので、さまざまな“がんの形”の可視化が期待できます。そこで、7種類の乳がん(浸潤がん、非浸潤がん、増殖病変、小葉がん、乳頭腫[良性の腫瘍]、微小浸潤がん、微小非浸潤がん)を、それぞれアジドプローブ溶液に5分間浸した後、顕微鏡で観察したところ、さまざまな“がんの種類(形態)”を確認できることが分かりました。この結果はHE染色法で得られた画像とほぼ同じ結果であり、アジドプローブ染色法を用いると従来のHE染色法で得られた画像と同じ画像を5分で得ることが可能になりました (図5) 。

図5 アジドプローブ染色とHE染色による乳がんの種類の比較結果
左側のアジドプローブによる染色画像では、赤がアジドプローブで染まったがん、青がHoechst試薬により染まった細胞核を示している。アジドプローブによる染色法とHE染色法の画像がほぼ同じ形態を示している。
今後の期待
今回、アクロレインという毒性化学物質に着目し、“アクロレインが多量に発生するがん細胞内で選択的に有機合成反応を行う”という画期的な視点で研究を進めることで、これまで長年使用されてきた手術中の病理学的診断法に代わる新しい診断技術の開発に成功しました。今後、乳がん診断検査の臨床研究を経て、多くの乳がん手術現場で本技術が活用されると期待できます。さらに、本技術と人工知能(AI)の画像診断技術との併用によって、乳がんの切除手術の効率化がいっそう進むことも期待できます。また、今後の臨床研究で、本技術が世界基準となり、専門的な技術や病理医の主観を必要としない技術が開発されれば、乳がんだけではなく、他のあらゆるがん手術の現場を改革すると考えられます。
論文情報
タイトル:Cascade Reaction in Human Live Tissue Allows Clinically Applicable Diagnosis ofBreast Cancer Morphology
著者名:Tomonori Tanei, Ambara R. Pradipta, Koji Morimoto, Motoko Fujii, Mayumi Arata,Akihiro Ito, Minoru Yoshida, Elena Saigitbatalova, Almira Kurbangalieva, Jun-ichiroIkeda, Eiichi Morii, Shinzaburo Noguchi and Katsunori Tanak
雑誌:Advanced Science
DOI:10.1002/advs.201801479
参考URL
大阪大学大学院 医学研究科 乳腺内分泌外科
http://www.onsurg.med.osaka-u.ac.jp/index.html
用語説明
- 酸化ストレス
生体内で酸化還元状態の均衡が崩れたとき、過酸化水素やヒドロキシラジカルを代表とする活性酸素が生産される。これらが生体内のタンパク質や脂質、あるいは核酸と反応し、生体にダメージを与える。この状態を酸化ストレスと呼び、がんや動脈硬化、アルツハイマー病や慢性疾患などの原因とされている。
- アクロレイン
アルデヒド基が二重結合(または三重結合)と炭素—炭素結合を介してつながった構造を持つ化合物を不飽和アルデヒドといい、アルデヒド基につながる二重結合が、全て水素で置換されている分子がアクロレインである。不飽和アルデヒドは、アルデヒド基や二重結合の多数の部位で反応でき、反応性が高い分子で、特にアクロレインは不飽和アルデヒドの中で最も小さく反応性が高いため、生体内のさまざまな分子と反応する。また、毒性が非常に強い。
- アジドプローブ
窒素原子が直線上に3つ並んだ化学構造がアジド基である。この発表では、アジド基がTAMRA蛍光基に結合した分子をアジドプローブと呼ぶ。
