
波長が変化するレーザーを用いた新しい顕微鏡を開発
染色せずに生体の三次元構造などの観察が可能に
リリース概要
大阪大学大学院工学研究科 小関泰之助教、伊東一良教授、福井希一教授、元大学院生 梅村航氏、住村和彦特任助教、科学技術振興機構、キヤノン株式会社 橋本浩行室長、大塚洋一博士、佐藤秀哉博士、名古屋大学 西澤典彦教授らの研究チームは、波長の高速切替が可能なレーザーを用いて生体組織を高速かつ無染色で観察する顕微鏡を開発しました。この装置と独自に開発した解析アルゴリズムを用いることで、生体組織の3次元構造や構成物質の組成差を、あたかも各種の染色剤を使って染色したかのように可視化することができます。
この成果は2012年11月11日(英国時間)に英国の論文誌Nature Photonicsのオンライン速報版に掲載される予定です。
研究の背景と内容
基礎医学、臨床医学や生物学において、生体組織を観察することは、病変部位の診断や組織形成の研究のための重要な技術です。しかし、多くの生体組織は透明であるため、観察する際は組織の加工や染色が必要です。これには多くの工程と数十分程度の時間を要し、熟練も必要です。このため、生体組織を迅速かつ鮮明に観察できる技術が求められています。また、生体組織の構造を3次元的に可視化するためには、組織を薄片化し、多数の2次元画像を重ねる必要があるなど、大変コストと手間がかかります。近年、染色が不要でかつ3次元分解能をもつ観察手法として、2色のパルスレーザーを用いた誘導ラマン(Stimulated Raman scattering, SRS)顕微鏡が注目されています。これは、生体分子の分子振動に由来するラマン効果を高感度に捉え、生体をリアルタイムに可視化することができる技術です。しかし、従来のSRS顕微鏡では、レーザーの波長で決まる特定の周波数の分子振動しか検出できないという課題がありました。このため、生体組織を構成する異なる分子が持つ振動スペクトルのわずかな違いを捉えることは困難でした。
研究グループは、波長を高速に切り替えられるパルスレーザーを開発するとともに、このレーザーを用いたビデオレートSRS顕微鏡を実現しました。この顕微鏡は500 x 480ピクセルの画像を1秒間あたり30.8フレーム取得可能です。そして、フレーム毎、すなわち1秒間に30.8回レーザーの波長を変化させることで、様々な周波数の分子振動を短時間に検出することができます(図1)。さらに、わずかな振動スペクトルの違いを画像化するための解析手法も開発しました。これらを用いてラットの肝臓(厚さ0.1 mm)を観察し、データを解析したところ、脂肪滴、細胞質、細胞核、線維、及び類洞などの2次元分布(図2)や、血管壁の線維の3次元分布(図3)を可視化することに成功しました。また、マウスの小腸の絨毛を構成する細胞の3次元的な配置をとらえ、細胞の種類を形態的に識別することにも成功しました(図4)。さらに、観察性能の高速性を活用し、息をして動いているマウスの皮膚内部の構造を可視化することにも成功しました。
本研究成果が社会に与える影響(本研究成果の意義)
今回開発した顕微鏡は、基礎医学・分子生物学における研究ツールとして、また、医療分野においては組織の異常を調べるための高感度で再現性のある検査技術として応用され、患者および医師の負担を軽減することが期待されます。今後、レーザー光源の実用性を更に高めることで、本技術は数年以内の実用化が可能です。
特記事項
本研究の主たる成果は科学技術振興機構 戦略的創造研究推進事業 個人研究(さきがけ)「光の利用と物質材料・生命機能」研究領域(研究総括:増原宏 奈良先端科学技術大学院大学 物質創成科学研究科 特任教授/台湾国立交通大学 講座教授)」における研究課題「誘導ラマンによる高感度光学活性検出及び高分解能イメージング(研究者名:小関泰之)」の一環として行われました。また一部は科学研究費補助金の助成によります。
論文名および著者名
“High-speed molecular spectral imaging of tissue with stimulated Raman scattering”
(誘導ラマン散乱 による組織の高速分子分光イメージング)
小関泰之、梅村航、大塚洋一、佐藤秀哉、橋本浩行、住村和彦、西澤典彦、福井希一、伊東一良
参考図
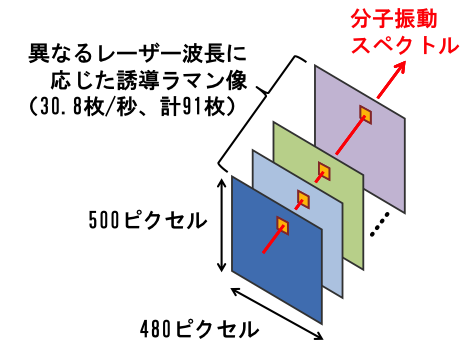
図1 波長可変レーザーを用いたSRS分光顕微鏡の動作の模式図。
500 x 480ピクセルの誘導ラマン像を1秒間に30.8フレーム取得しつつ、フレーム毎にレーザー波長を変化させる。その結果、各ピクセルにおいて生体試料の分子振動スペクトルの情報を得ることができる。

図2 ラットの肝臓組織の無染色観察例。
A: 脂肪滴。
B: 細胞質。
C: 線維。
D: 細胞核。
E: 類洞(毛細血管)。
F: 白血球(好酸球)。
【スケールバー:20 µm。】

図3 ラットの肝臓の血管周辺の線維構造の3次元無染色観察例。
【観察領域:130 x 125 x 80 µm。】
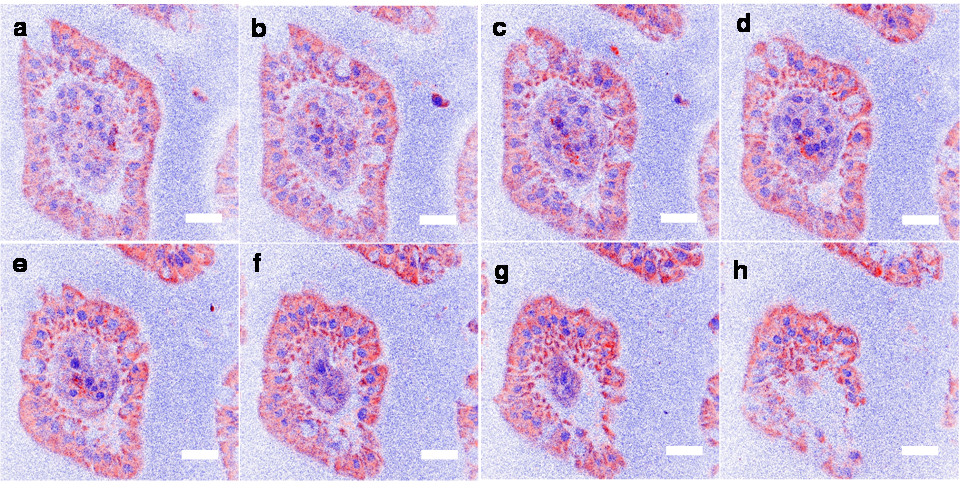
図4 マウスの小腸の絨毛の無染色観察例。
厚さ100 µmの組織切片内部において、5.6 µmずつ深さを変えながら観察した。青:細胞核。赤:細胞質。【スケールバー:20 µm。】
参考URL
用語説明
- 誘導ラマン散乱
(SRS):
2色の光と分子の相互作用の一つ。2色の光の光周波数の差が、分子振動の共鳴周波数と一致したとき、短波長の光から長波長の光にエネルギーが移動する現象。
