
トキソプラズマ症の発病を防ぐ最重要宿主防御因子GBPを同定
インターフェロン誘導性タンパクGBPは寄生虫「トキソプラズマ」を破壊する
<リリース概要>
大阪大学医学系研究科の竹田潔教授(免疫学フロンティア研究センター兼任)と同微生物病研究所の山本雅裕准教授(免疫学フロンティア研究センター兼任)らの研究グループは、インターフェロンにより誘導されるタンパク質であるGBP(p65 GTP分解酵素)が寄生虫「トキソプラズマ」を破壊することでトキソプラズマ症の発病を抑制している宿主防御因子であることを明らかにしました。

<研究の背景>
寄生虫「トキソプラズマ」はエイズや抗癌剤投与下にある免疫不全患者に致死性のトキソプラズマ症や妊婦に流産と新生児に水頭症を引き起こす先天性疾患の原因病原体です。我々ヒトを含む宿主はインターフェロンと呼ばれる分子を出すことでトキソプラズマ症の発病を抑えていることが四半世紀前から分かっていましたが、インターフェロンが具体的にどのようにしてトキソプラズマを破壊するのか、そのメカニズムは不明でした。
<本研究成果が社会に与える影響>
本研究で、トキソプラズマが感染細胞内で増殖する際に必須の生活の場である「寄生胞」を、インターフェロンにより誘導されるタンパク質であるGBPが破壊することが、トキソプラズマが感染細胞内で増殖不可能にするために不可欠であり、その結果トキソプラズマ症の発病を抑制していることを、GBP欠損マウスの作製と生体レベルでのイメージング解析により、世界に先駆けて証明しました。
本研究成果は、近年我が国においても症例報告が急増しているトキソプラズマ症に対して、GBPの機能を高めるなどの人為的な制御を加えることでの新たな分子標的治療戦略を提供できるものとして大いに期待できます。
<特記事項>
本研究成果は、米国の科学雑誌『Immunity』(7月12日付け:日本時間7月13日午前1時)にオンライン掲載されます。本研究は、大阪大学免疫学フロンティア研究センターの山本雅裕准教授、竹田潔教授らとスイス・ジュネーブ大学医学部微生物学教室(ドミニク ソルダーティ=ファーブル博士)の共同研究グループが、独立行政法人科学技術振興機構(JST)の戦略的国際科学技術協力推進事業「日本-スイス(ETHZ)研究交流」研究領域における研究課題「胞子虫類原虫における宿主内作動性エフェクター因子の機能的解析」(研究代表者:山本雅裕・ドミニク ソルダーティ=ファーブル)の一環として行いました。
<1 背景>
トキソプラズマはネコを終宿主とする病原性寄生虫です(図1A)。中間宿主はヒトを含むほぼ全ての恒温動物であり、ヒトに限っていえば全世界人口のうちの約3分の1(数十億人)が感染し、我が国だけでも数千万人に感染していることが試算されています。健常人では一過性の発熱などを除いてほとんど症状がないことからトキソプラズマは日和見病原体として扱われていますが、エイズ患者・抗癌剤投与された患者などの免疫不全者においてはトキソプラズマ脳症を引き起こします。近年我が国において、ガーデニングの流行や非加熱の生肉食の増加などのライフスタイルの欧米化に伴い、とりわけ妊婦がトキソプラズマに感染し、その結果胎児にトキソプラズマが母体の胎盤を介して感染し流産したり、あるいは新生児が水頭症に罹患した状態で生まれてくるなど非常に予後不良な疾患を引き起こす症例が急増しており、マスコミなどにも取り上げられています(2012年5月10日放映 NHK・朝イチ「妊婦さんご注意!意外なモノで赤ちゃんに危険」も参考にして下さい。 http://www.nhk.or.jp/asaichi/2012/05/10/01.html)。 また、最近は統合失調症の発病にもトキソプラズマの感染の有無が関連しているとの報告もされています。
トキソプラズマはマラリア症の原因病原体であるマラリア原虫などと同じ胞子虫類原虫に分類され、宿主の細胞の中でのみ増殖可能な偏性細胞内寄生生物です。感染可能な細胞の種類はすべての有核の細胞であり、赤血球あるいは肝臓細胞のみにしか感染できないマラリア原虫とは比較にならないぐらいの多種多様の細胞がトキソプラズマの標的細胞となることが、非常に多くの感染者がいる原因の一つであると考えられます。トキソプラズマは細胞に感染した時に、「寄生胞」と呼ばれる細胞内小器官を形成し、その中で宿主から栄養分を摂取することで効率的に増殖することがわかっています(図1B)。それに対して、我々宿主はインターフェロン(IFNγ)というT細胞やナチュラルキラー細胞などの免疫細胞から主に分泌されるタンパク質を使って寄生胞内のトキソプラズマを破壊することがトキソプラズマ症の発病を防ぐのに重要であるということが約30年前から示唆されていました。しかし、IFNγ自身には病原体を直接破壊するような構造はなく、従ってどのようにしてIFNγがトキソプラズマを破壊しているのかについてのメカニズムは長い間不明のままでした。
<2 研究の手法と成果>
研究グループはIFNγがマクロファージや線維芽細胞などの自然免疫担当細胞に作用して、約2000種類のエフェクター分子群の遺伝子発現を誘導することに着目しました。中にはトキソプラズマの寄生胞の周辺に集まってくるGBP(p65 GTP分解酵素)と呼ばれる13個のファミリー分子群から形成されるエフェクター分子群があり、宿主の抗トキソプラズマ免疫応答に何らかの役割を果たしていることが考えられました。通常、ある特定の遺伝子の役割を調べたいという場合には一つの遺伝子を欠損させたマウスを作成して検討しますが、GBPの場合はそれぞれの遺伝子の相同性が非常に高く(つまり、よく似ているため)、一つの遺伝子を欠損させても非常に良く似た別のGBPファミリー分子がその機能を補う(相補する)ことが予想されました。そこで当研究グループではGBPファミリー分子が6個と7個に分かれて異なる染色体上の非常に狭い領域に隣り合って存在することを利用して、染色体工学的手法を用いて3番染色体上に存在する全てのGBP(6個)のGBPファミリー分子を欠損するマウス(GBPchr3欠損マウス)の作製し解析しました。
GBPchr3欠損マウスと野生型マウスにトキソプラズマを感染させ生存率を測定した所、GBPchr3欠損マウスはトキソプラズマ感染に対して非常に弱くなっていることが分かりました(図2A)。また感染マウス内でのトキソプラズマの感染拡大を、トキソプラズマから出る発光を指標に生体イメージング装置を使って検討したところ、GBPchr3欠損マウス内では野生型マウスと比べて劇的にトキソプラズマが増殖していることが分かりました(図2B)。次にトキソプラズマが生体内で感染している細胞であるマクロファージと呼ばれる自然免疫細胞を単離して、トキソプラズマを感染させその増殖を検討しました。IFNγで野生型マクロファージを処理すると濃度依存的にトキソプラズマの増殖が抑制されますが、GBPchr3欠損マクロファージではIFNγによるトキソプラズマの増殖を野生型細胞と比較して抑制できないことを見出しました(図2C)。このことから、IFNγによって誘導されるGBPchr3は自然免疫細胞マクロファージ内でトキソプラズマ増殖を妨げることが、生体レベルでのトキソプラズマに対する感染防御反応に重要であることが分かりました。
では、GBPを欠損したマクロファージでは何故トキソプラズマの増殖を抑制できないのでしょうか?その問題を解決するために研究グループは電子顕微鏡を使って、感染細胞内でのトキソプラズマの状態を検討しました。その結果、IFNγで刺激した野生型マクロファージ内ではトキソプラズマの寄生胞の膜が激しく波打ち、その構造が著しく破壊されていました(図3A)。一方、GBPchr3欠損マクロファージ内ではIFNγ処理をしてもそのような寄生胞膜の構造変化は認められませんでした(図3B)。このことから、GBPはマクロファージ内でトキソプラズマの寄生胞の膜構造を破壊する機能があることが分かりました。
ではどのようにしてGBPはトキソプラズマの寄生胞膜を破壊することができるのでしょうか?以前から寄生胞膜の破壊についての機能が示唆されていたGBPとは別のファミリー分子群であるp47 GTP分解酵素(IRG)の動態について、野生型及びGBPchr3欠損マクロファージで比較しました。すると、野生型細胞ではIRGがトキソプラズマに蓄積するのに対して、GBPchr3欠損マクロファージではIRGの蓄積が著しく減少していることが分かりました(図4A)。またGBPとIRGの局在について野生型マクロファージ内で検討したところどちらもトキソプラズマに蓄積し、さらにGBPはIRGに結合していることも分かりました(図4B)。これらのことから、GBPはIRGをトキソプラズマに蓄積させることでその寄生胞膜を破壊し増殖を阻害していることが示唆されました(図5)。
<3 今後の期待>
今回の研究により、IFNγによって誘導される抗トキソプラズマ感染防御機構にGBPが重要な役割を果たしていることを明らかにしました。このことから、人為的にGBPの機能を高めることにより、我が国で症例報告が急増しているトキソプラズマ症に対する新たな治療戦略を提供できることが期待できます。
寄生胞はトキソプラズマに限らずマラリア原虫においても形成されることを考えると、GBPがマラリア原虫感染防御に関与する可能性は非常に高く、マラリア症の発病におけるGBPの役割の解明は最も重要な今後の研究課題です。またGBPは様々な癌において高い発現が認められることが多数報告されており、感染下ではない異常な状態でのGBPの存在が引き起こす疾患の病理機構の解明に、研究グループが染色体工学により作り出したGBP欠損マウスが非常に有用であると考えられます。
<参考図>
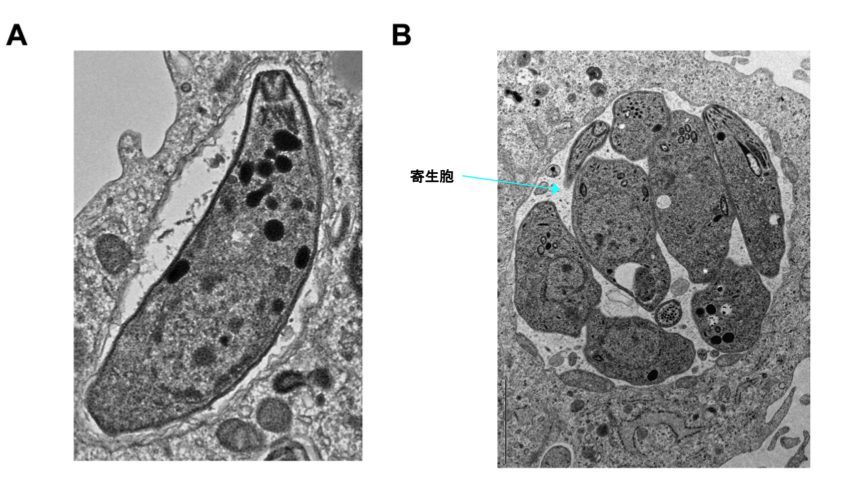
図1:トキソプラズマは「寄生胞」の中で増殖する
(A)トキソプラズマの電子顕微鏡写真。
(B)寄生胞の中で増殖しているトキソプラズマの電子顕微鏡写真。寄生胞膜を介して感染細胞から増殖に必要な栄養分を摂取する。

図2:GBPchr3を欠損したマウス及び細胞はトキソプラズマ感染に弱くなる
(A)野生型及びGBPchr3欠損マウスにトキソプラズマを感染させ生存率を測定した結果、GBPchr3欠損マウスはトキソプラズマ感染に非常に感受性が高まることが明らかとなった。
(B)発光するトキソプラズマをマウスに感染させ、生体イメージング装置でトキソプラズマの動態を観察した所、GBPchr3欠損マウス内でトキソプラズマがより多く増殖した。
(C)野生型マクロファージをIFNγで刺激すると濃度依存的にトキソプラズマの数が減少するが、GBPchr3欠損マクロファージでは野生型に比べて原虫数の数が多かったことから、GBPchr3の欠損によりIFNγ依存的な増殖抑制に障害が出ることが示唆された。
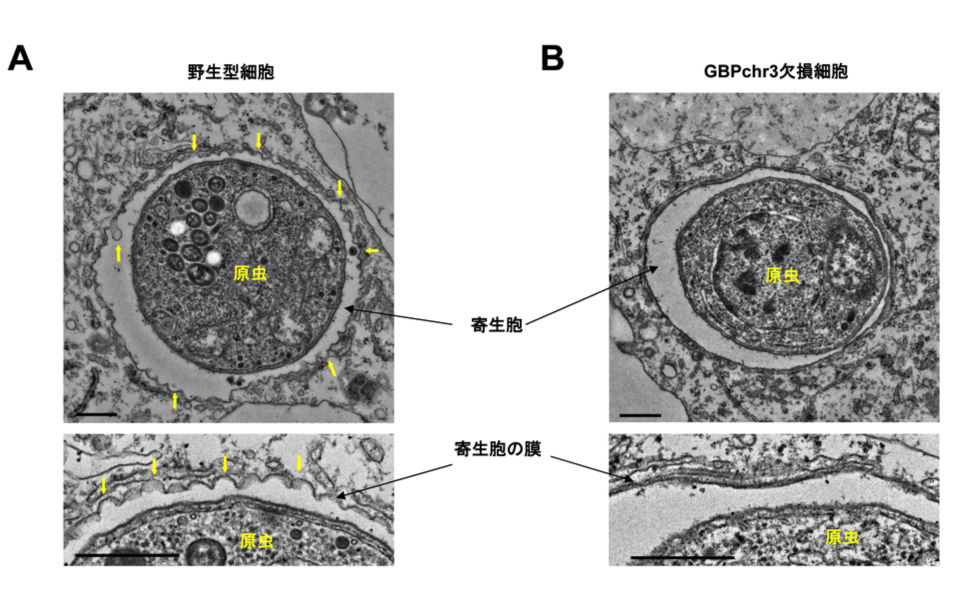
図3:GBPchr3を欠損した細胞では寄生胞膜の構造変化が認められない
(A)野生型
(B)GBPchr3欠損マクロファージにおける寄生胞内のトキソプラズマの電子顕微鏡像。野生型細胞では寄生胞の膜が激しく波打っているのに対し、GBPchr3欠損細胞ではそのような変化は認められない。

図4:GBPchr3を欠損した細胞ではIRGのトキソプラズマへの蓄積が低下している
(A)IRGのトキソプラズマへの蓄積を比較した所、野生型細胞に比べてGBPchr3欠損細胞ではIRGとトキソプラズマが共局在している像が認められない。
(B)野生型細胞においてGBP、IRGとトキソプラズマは共局在をすることからGBPとIRGは非常に近い所に存在することが示唆された。
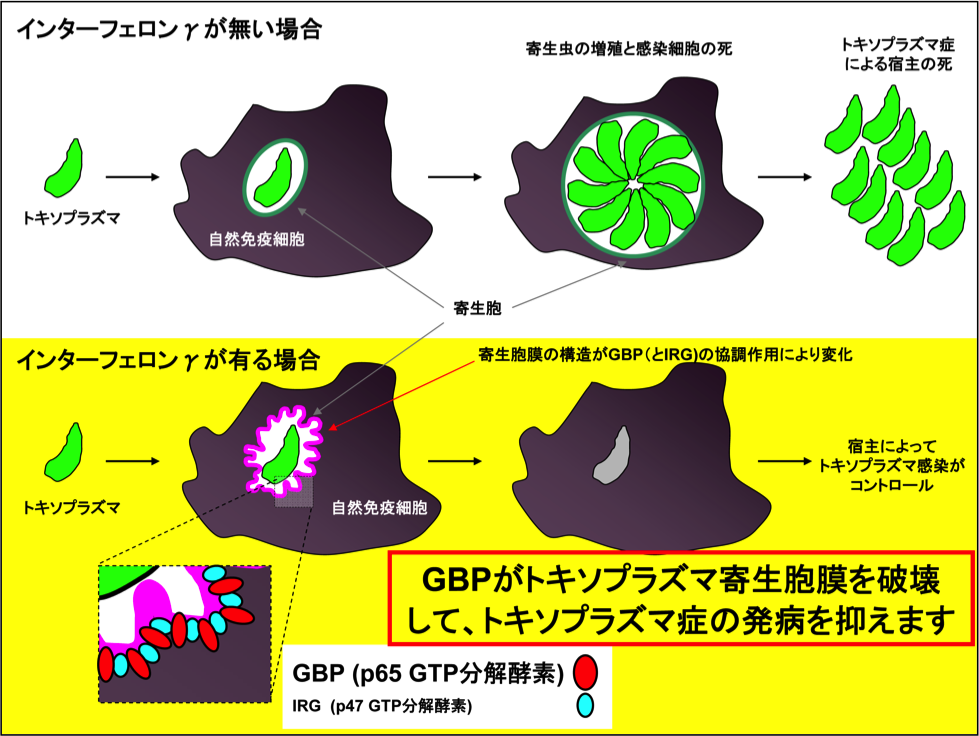
図5:今回明らかとなったインターフェロン誘導性タンパクGBPを介する抗トキソプラズマ感染防御機構
IFNγが無い場合、トキソプラズマは感染細胞内の寄生胞内で増殖し、その結果感染細胞はトキソプラズマによって殺され、最終的には宿主がトキソプラズマ症により死亡する。一方、IFNγ存在下ではGBPが誘導され寄生胞膜にIRGと共に蓄積することで寄生胞膜構造を破壊し、トキソプラズマは増殖することができなくなる。
