脂質の挙動をありのままに再現する蛍光プローブでラフトの形成機構を解明
概要
九州大学大学院理学研究院の松森信明教授、木下祥尚助教、京都大学物質-細胞統合システム拠点(iCeMS=アイセムス)の楠見明弘教授、鈴木健一特定拠点准教授、大阪大学の村田道雄教授(科学技術振興機構(JST)ERATO「村田脂質活性構造プロジェクト」研究総括を兼任)」らの共同研究グループは、脂質の動きを「ありのまま」に再現する蛍光性の脂質アナログ分子 を合成することで、細胞膜上においてラフトが形成される様子を観察することに成功しました。
細胞膜にはスフィンゴミエリンなどの特定の脂質が集まったラフト領域と呼ばれる数ナノから数十ナノメートルの特殊領域が多数点在しており、細胞膜の重要な働きである信号伝達機能のかなりの部分を担っていると、この25年来仮定されてきました。しかし、これまでラフトの実態はよく分かっていませんでした。本研究グループでは、スフィンゴミエリン脂質に蛍光を発する分子を目印として結合させ、ラフトへの出入りを解明することに成功しました。今までの同様の試みでは、目印の結合により脂質の性質が変わってしまったのですが、蛍光の目印を水になじみやすいように工夫して脂質に結合させることで、この問題の解決を試みました (図1) 。新たに合成した蛍光スフィンゴミエリンをラフト様領域を含む人工膜に取り込ませたところ、天然のスフィンゴミエリンと同様の割合で、ラフト様領域に局在することがわかりました (図2) 。さらに、細胞膜上での1分子観察によって、蛍光目印のついたスフィンゴミエリンはラフト結合型受容体分子とラフト内で結合と解離を繰り返していること、しかも、結合時間は10ミリ秒程度であること、さらに受容体が活性化されると、結合時間は5 倍も延びることなど、従来の教科書の記述を書き換えるような発見がなされました (図3) 。今後、このスフィンゴミエリンの蛍光アナログ分子は、ラフトの研究に大きく貢献すること、さらに、ラフトが関わるシグナル伝達の異常や感染症の解明に大きく寄与することが期待されます。
本研究成果は、米国学術誌「Journal of Cell Biology(Tools)」のオンライン版で3月22日に公開されました。
図1 (上)新たに合成したスフィンゴミエリン蛍光アナログ分子。(下)従来の蛍光アナログ脂質との違い。親水性の蛍光分子とリンカーを用いることで、天然の脂質と同じ振る舞いができる。
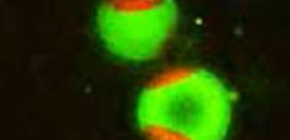
図2 緑色の蛍光スフィンゴミエリン分子は、人工膜のラフト様領域に局在する。赤色の領域は、ラフトでない膜領域。
図3 本研究で解明された、スフィンゴミエリンの様々な様態のCD59 への過渡的結合の模式図。
参考URL
大学院理学研究科 化学専攻 生体分子化学研究室
http://www.chem.sci.osaka-u.ac.jp/lab/murata/
用語説明
- 蛍光性の脂質アナログ分子
脂質分子の細胞膜内での挙動を調べたいとき、脂質分子を見るのは難しい。そこで蛍光を発する化合物を脂質分子に結合させ、その蛍光を目印として動きや局在を追跡することが可能になる。( 図1 参照)。このとき、目印が、元の脂質分子の性質を変えないように、うまい目印を、上手に結合させることが必要である。このような蛍光性化合物を目印に結合させた脂質分子の類似体を蛍光性の脂質アナログ分子と呼ぶ。
