生体防御に必須の免疫記憶成立のメカニズムを解明
記憶B細胞の誕生には低代謝と生存シグナルが重要
研究成果のポイント
・胚中心 におけるB細胞の分化運命決定のメカニズムは不明であったが、記憶B細胞 の前駆細胞の同定に成功。
・胚中心B細胞から記憶B細胞への分化には、低代謝状態とB細胞受容体からの生存シグナルが必要。
・転写因子Bach2 は、胚中心B細胞の代謝制御に重要な役割を担っており、記憶B細胞誕生に必須。
概要
大阪大学免疫学フロンティア研究センターの井上毅特任准教授(常勤)、黒﨑知博特任教授(常勤)(理化学研究所生命医科学研究センター兼任)らの研究グループは、ワクチン療法の基本原理である免疫記憶の中心を担う記憶B細胞が、胚中心B細胞より効率的に分化誘導されるメカニズムを明らかにすることに成功しました。
B細胞、T細胞といったリンパ球は、細菌・ウイルスなどの微生物感染において、生体防御反応の中心的役割を担います。特に、細菌・ウイルスなどの2度目の侵入時には、1度目の感染時にできた記憶B細胞が素早く抗体産生細胞(プラズマ細胞)に分化し、効果的に抗原をブロック・除去します。この免疫記憶の仕組みを利用して、感染前に免疫記憶を人為的に誘導するのがワクチン療法です。
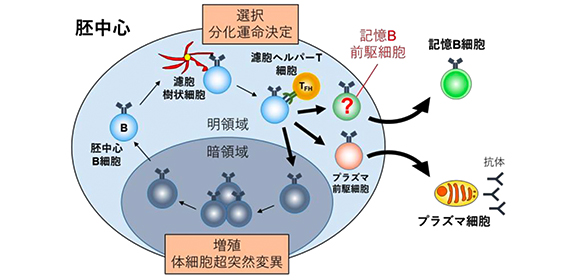
ウイルス、ワクチンなどの抗原が人の体内に入ると2次リンパ組織の中で胚中心が形成されます。胚中心では、B細胞がプラズマ細胞に分化するか、記憶B細胞に分化するか、胚中心に留まるかの運命選択がなされますが、そのメカニズムは分かっていませんでした。本研究では、胚中心において記憶B細胞への運命決定がなされてすぐの記憶B細胞の前駆細胞を同定することに成功し、その性質・機能を解析しました (図1) 。その結果、より代謝活性の低く、かつB細胞受容体からの生存シグナルをより多く獲得した胚中心B細胞が記憶B細胞に効率的に分化しやすいことが分かりました。また、本研究グループはこれまでの研究で転写因子Bach2が記憶B細胞産生に必要であることを報告していましたが(Shinnakasu et al., Nat Immunol , 2016)、この研究でBach2は胚中心B細胞を低代謝状態に抑えるために重要な役割を果たしていることも分かりました。
本研究成果は、科学誌「 Journal of Experimental Medicine 」に、10月12日(月)午後11時(日本時間)に公開されました。
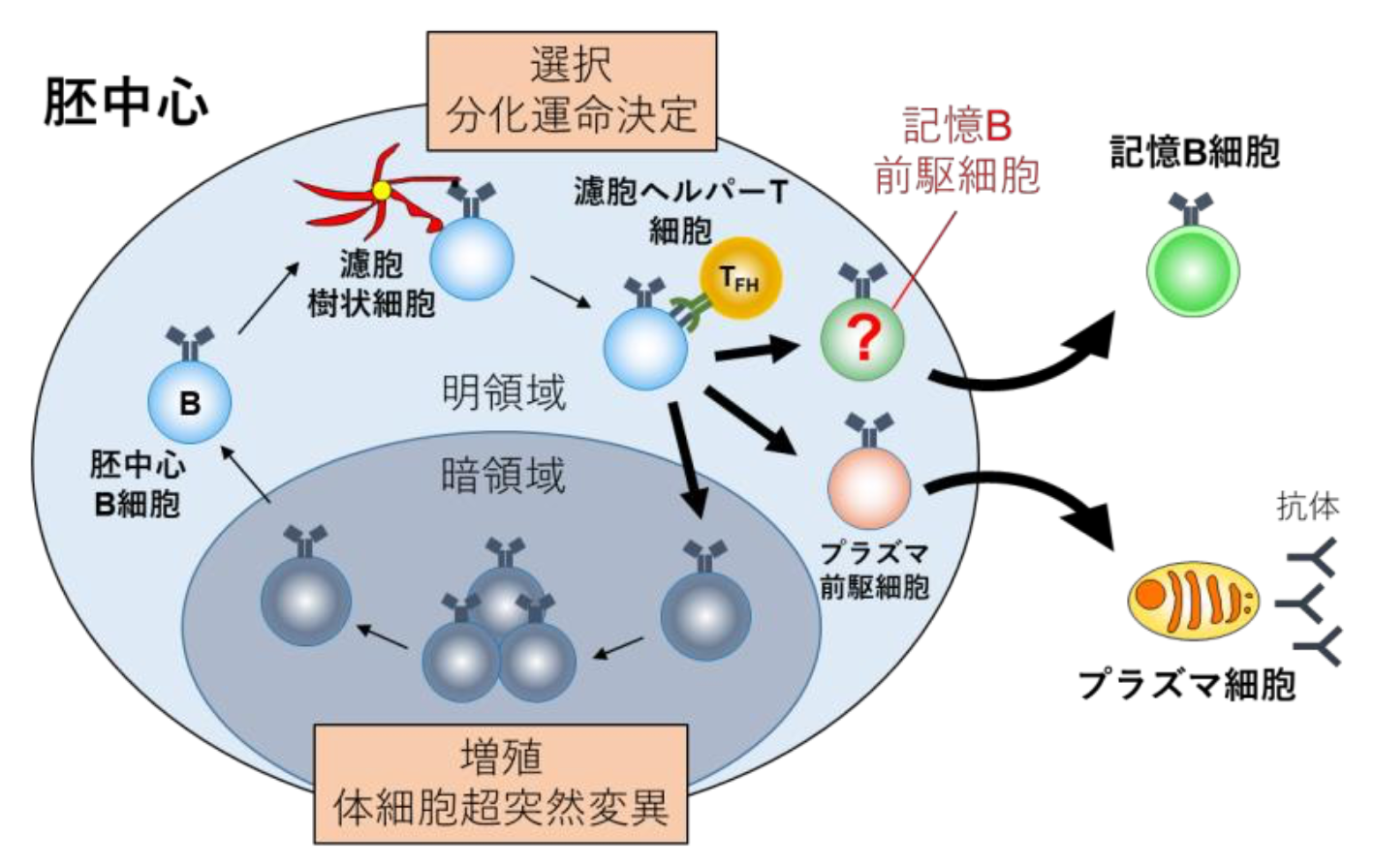
図1 胚中心におけるB細胞分化
研究の背景
新型コロナウイルスやインフルエンザウイルス感染に対する生体防御メカニズムの解明は社会的にも重要かつ喫緊の課題です。B細胞、T細胞といったリンパ球は、このような細菌・ウイルスなどの微生物感染において、生体防御反応の中心的役割を担います。特に、細菌・ウイルスなどの2度目の侵入時に迅速に反応して抗原を除去する仕組みを「免疫記憶」と言い、1度目の感染時に作られた記憶B細胞が記憶T細胞の助けをかりて素早くプラズマ細胞に分化し、効果的に抗原をブロック・除去します。記憶B細胞は主に2次リンパ組織の中で胚中心から産生されますが、胚中心B細胞はそのほかにも、プラズマ細胞に分化するもの、あるいは胚中心に留まってB細胞受容体遺伝子に変異を蓄積させるものも共存しており、これらにどのように分化の運命選択がなされているのか、そのメカニズムは分かっていませんでした。
本研究の成果
研究グループは、胚中心には記憶B細胞へ分化することが決定された記憶B細胞の前駆細胞が存在すると考え、胚中心B細胞の特徴を保ちつつも記憶B細胞の性質を獲得しはじめている細胞の同定を試みました。その結果、胚中心B細胞の機能に必須の転写因子Bcl6と、記憶B細胞のマーカーであるCD38の両方を発現する稀少細胞集団を発見し、遺伝子発現の解析や細胞機能の解析などからこれが胚中心B細胞と記憶B細胞の中間状態の細胞(=記憶B前駆細胞)であることを示しました。
この細胞の性質を詳細に解析したところ、プラズマ細胞に分化する細胞や胚中心に留まる細胞と比較して、細胞の代謝制御を司るmTORC1タンパク質の活性が低いことを見出しました。そこで、免疫応答時にB細胞のみでmTORC1活性を阻害することのできる実験系を開発し、胚中心B細胞の分化を解析したところ、mTORC1活性を低減させたB細胞は記憶B細胞への分化が亢進することが分かりました。また、本研究グループはこれまでの研究で、転写因子Bach2欠損マウスは記憶B細胞産生が低下することを報告していましたが(Shinnakasu et al., Nat Immunol , 2016)、この研究でBach2欠損B細胞はmTORC1活性が上昇しており、このことが記憶B細胞分化が阻害されている原因の一つであることも分かりました。
さらに研究グループは、記憶B前駆細胞は胚中心B細胞と比較して細胞表面のB細胞受容体 の発現量が高く、その結果細胞の生存因子の一つであるBcl2の発現が上昇していることも見出しました。これまでの研究から、胚中心においてB細胞受容体の抗原親和性の高い細胞はプラズマ細胞に分化しやすく、親和性の低い細胞は記憶B細胞に分化しやすいことが分かっていましたが、本研究の結果から、低親和性B細胞はT細胞ヘルプを少ししか受け取れないためmTORC1活性は低く保たれるいっぽう、B細胞受容体の発現が高くなることでより細胞の生存に有利にはたらいていることが分かり、この2つのメカニズムが、休止状態で長寿命である記憶B細胞へ分化するために重要な役割を果たしていることが明らかになりました。
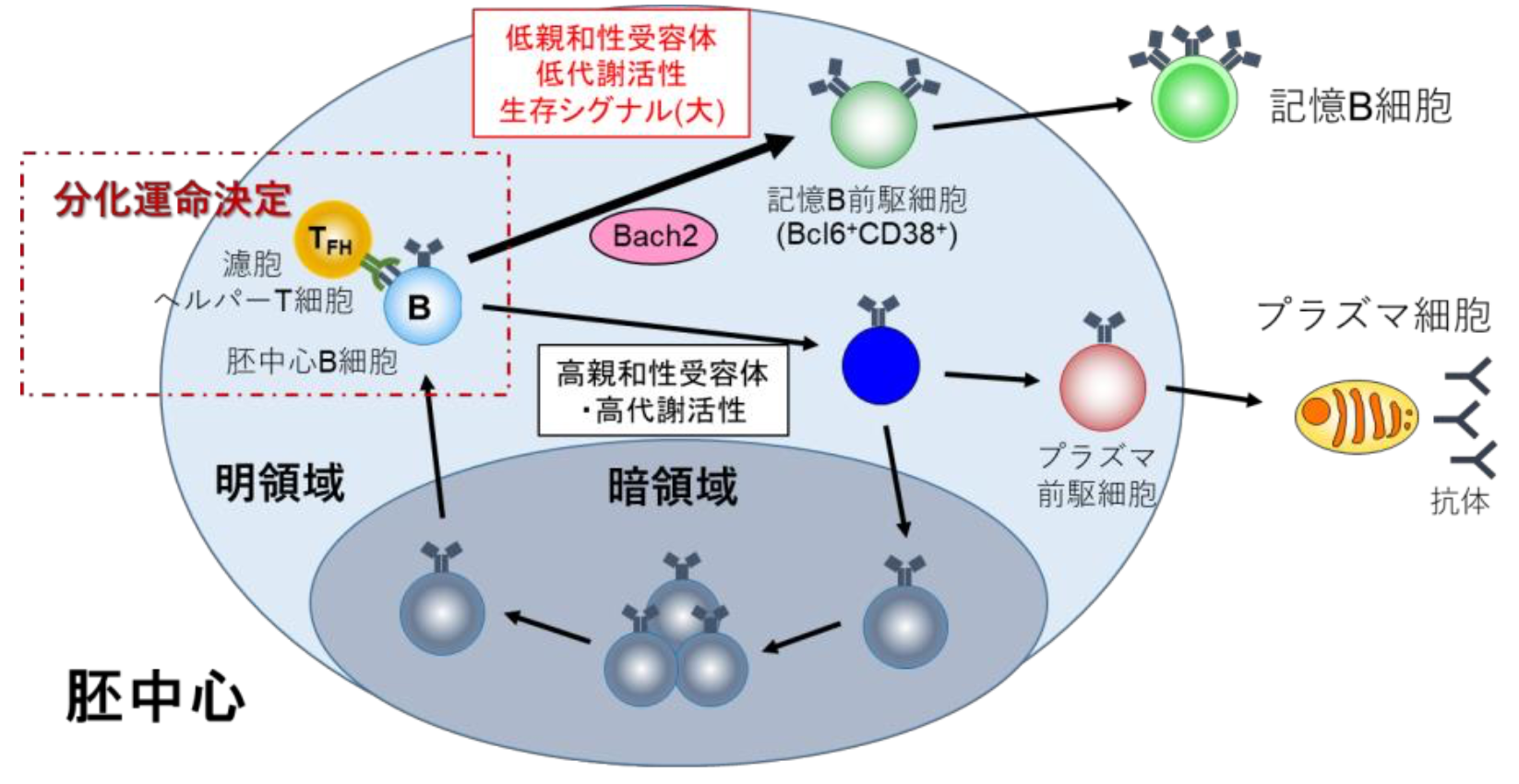
図2 代謝制御とB細胞受容体からの生存シグナルが記憶B細胞分化に影響
本研究成果が社会に与える影響(本研究成果の意義)
HIVやインフルエンザウイルス感染においては、胚中心B細胞が抗体遺伝子に再度変異を獲得し、適切な抗原親和性を持つ抗体を発現する能力を記憶B細胞として保持していくことで変異ウイルスに対する生体防御能が発揮されると考えられています。本研究による記憶B細胞分化メカニズムの解明は、例えば現行のインフルエンザワクチンではなぜ変異ウイルスに対する有効な記憶B細胞を誘導できず、毎年のワクチン接種が強いられるのか、といった問いに答えるための基盤的データを提供するものであり、将来的に革新的なワクチン開発につながる可能性があります。
特記事項
【掲載誌】 Journal of Experimental Medicine (オンライン)2020年10月12日に掲載
【タイトル】“Exit from germinal center to become quiescent memory B cells depends on metabolicreprograming and provision of a survival signal”
【著者名】 Takeshi Inoue 1 , Ryo Shinnakasu 1 , Chie Kawai 1 , Wataru Ise 1 , Eiryo Kawakami 2 ,3, Nicolas Sax 4 , Toshihiko Oki 5 , Toshio Kitamura 5 , Kazuo Yamashita 4 , Hidehiro Fukuyama 6 , and Tomohiro Kurosaki 1,6
【所属】
1 大阪大学 免疫学フロンティア研究センター 分化制御研究室
2 理化学研究所 医科学イノベーションハブ推進プログラム
3 千葉大学 大学院医学研究院 人工知能(AI)医学
4 KOTAIバイオテクノロジーズ株式会社
5 東京大学医科学研究所 先端医療研究センター 細胞療法分野、幹細胞治療センター 幹細胞シグナル制御分野
6 理化学研究所 生命医科学研究センター 分化制御研究チーム
参考URL
免疫学フロンティア研究センター分化制御研究室-IFReC-
http://lymph.ifrec.osaka-u.ac.jp/index_j.html
用語説明
- 胚中心
免疫応答時にリンパ節や脾臓などの免疫組織につくられる微小構造。暗領域(dark zone)では、B細胞が増殖するとともに抗体遺伝子に変異を入れてより良い抗体を産生できるようにする。明領域(light zone)では、B細胞は濾胞樹状細胞や濾胞ヘルパーT細胞と相互作用して分化の運命選択がなされる。
- 記憶B細胞
抗原に1度目に感作されたときにつくられるB細胞。記憶していた抗原の再刺激を受けると、迅速にプラズマ細胞に分化して、多量の抗体をつくる。
- B細胞受容体
B細胞表面に抗原に発現する膜型の免疫グロブリンタンパク質で、抗原に結合するとB細胞の活性化・分化を引き起こす。それぞれのB細胞は異なる配列のB細胞受容体を発現しており、異なる抗原を認識することができる。胚中心の暗領域ではB細胞受容体遺伝子に変異が入り、抗原親和性が変化する。
- 転写因子Bach2
特定のDNA配列に結合して、遺伝子発現を調節するタンパク質の一つ。B細胞では、Blimp1という遺伝子を抑制することでプラズマ細胞分化を抑制している。また、Bach2欠損マウスでは記憶B細胞分化が障害される。
