アルツハイマー病の原因物質を「毒性」に変貌させる 新しいメカニズムを発見
溶けているはずの塩がナノレベルでは析出と溶解を繰り返すことが原因
研究成果のポイント
・溶解度の50分の1という低濃度の塩水においても、ナノレベルでは塩の析出 と溶解が繰り返されていることを発見
・この局所的・短時間に起こる塩の析出と溶解が、アルツハイマー病の原因タンパク質を毒性物質へと変貌させることを発見
・液体からのタンパク質の析出という現象に対して新たなメカニズムが明らかとなり、同時に、アルツハイマー病の発症メカニズムの解明にも寄与することが期待される
概要
大阪大学国際医工情報センターの中島吉太郎特任研究員(常勤)、工学研究科の荻博次教授らの研究グループは、北海道大学低温科学研究所の木村勇気准教授らとの共同研究により、溶液に溶けているはずの塩が局所的に析出と溶解を繰り返す現象を特殊な電子顕微鏡により直接観測することに成功し、この現象がアルツハイマー病の原因と考えられるタンパク質凝集体の生成を加速する様子を世界で初めて直接観察することに成功しました。
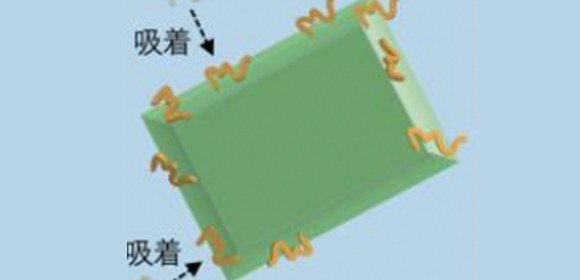
今回の発見は、溶質が溶媒に「溶けている」という現象が、析出と溶解の動的平衡により成り立っていることを直接立証した成果であると同時に、タンパク質が溶けている溶液に塩を加えるとタンパク質が析出する「塩析」という現象の理解に新たな概念が加わることになります。アルツハイマー病の原因タンパク質が塩とともに溶解しているとき、塩が一時的に析出し成長すると、その表面に多くのタンパク質分子が吸着し、その後、その塩が再び溶ける時、吸着したタンパク質分子が塩の消滅点に集められ、局所濃縮され、通常では起こり得ない反応が起き、結果、タンパク質の凝集核を形成することがわかりました (図1) 。この凝集核こそがアルツハイマー病の原因物質の起点となるものであり、こうした塩のナノレベルでの析出と溶解によって、タンパク質の凝集を加速することが明らかとなりました。これはタンパク質の凝集現象における全く新しいメカニズムであり、このメカニズムこそが、凝集反応を支配する可能性もあります。
本研究成果は、米国科学誌「The Journal of Physical Chemistry Letters」に、7月20日(月)に公開されました。
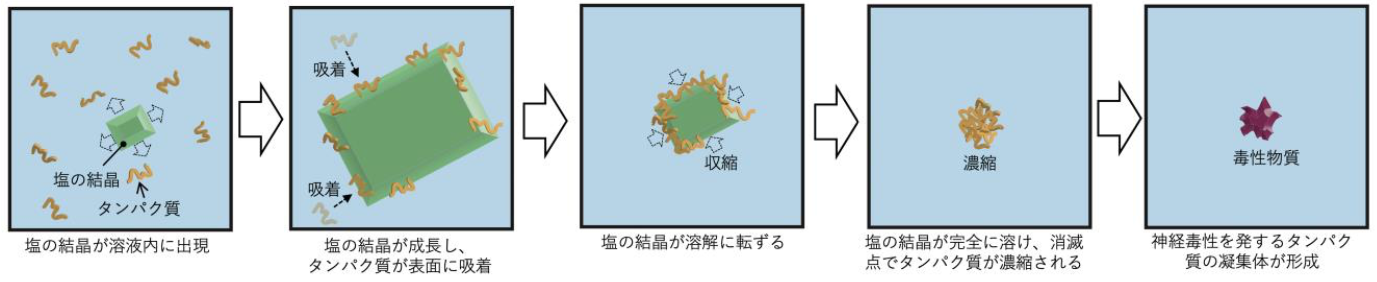
図1 塩の結晶が析出し、成長し、溶解する過程で、タンパク質が局所的に濃縮され、毒性の凝集体が出現する
研究の背景
水に少量の塩を加えてよくかき混ぜると塩は溶けます。温度を一定にしてどんどん塩を加えて溶かすと、溶液の塩の濃度がある値以上には溶けることができず、塩は析出します。この濃度が溶解度です。溶解度よりも低い濃度のとき、塩は溶けた状態を維持し、析出することはありません。血液や脳脊髄液といった体液には溶解度以下の塩分が含まれており、タンパク質の性質を研究する際には、塩を少量混ぜて実験を行うことが一般的です。今回の私たちの実験では、溶解度の50分の1程度の濃度の塩の溶液を使用しています。溶かす塩の量は少量ですから、見た目の溶液から塩は析出することがなく、溶けた状態が保たれており、何も起きていません。ところが、液体を直接観察することができる特殊な透過型電子顕微鏡(溶液TEM )を用いて、溶液内のナノサイズの領域を観察すると、時折、溶けているはずの塩が析出して成長し、そして、収縮し、再び溶解する現象が観察されました。溶解度よりも低い濃度であっても、非常に小さい領域では、塩の析出と溶解が繰り返されていたのです。溶液内の塩分濃度は至るところ一定ではなく、つねに揺らいでいます。この「ゆらぎ」により、たまたま、濃度の高い箇所が出現すると、塩の結晶が生まれるのです。しかし、その寿命は短く、一定程度のサイズ(約100nm)までは成長するものの、成長により周りの塩濃度が急激に低下するため、再び収縮して消滅します(つまり溶けます) (図2) 。
「ゆらぎ」により、局所的・短時間に塩の析出・溶解が繰り返されるのです。こういった現象を動画で直接撮影に成功したのは世界初です。
さらに重要な発見がありました。それは、この現象が、タンパク質の凝集を加速することです。アルツハイマー病の原因タンパク質は、アミロイドβ であることが良く知られています。アミロイドβは本来水に溶けますが、ある程度濃度が高くなったり、温度が上がったり、溶液のpHが変化したり、力学的刺激が加わったり、そして、塩濃度が上がったりすると、凝集して析出します。このアミロイドβの凝集体こそがアルツハイマー病の原因となります。最後に記した「塩によるタンパク質の析出」は、いわゆる「塩析」という現象として巨視的に理解されてきました。例えば、イオン化した塩分が電気的な接着剤のようにタンパク質どうしを結合させて析出させるとか、タンパク質を溶かすのに必要な水を塩が奪うために、タンパク質が析出するなど、巨視的に理解されてきました。ところが、今回の発見により、少なくともアミロイドβというタンパク質は、一時的に析出した塩の結晶の表面に吸着し、その後の、塩の溶解により塩の消滅点に集められ、過度の局所濃縮が起こることにより、凝集体を形成するという、これまで全く知られていなかった現象が起こっていることが明らかになりました。疎水性(液体が苦手な)部位を有するアミロイドβは、固体である塩の結晶が出現すると、好んでその表面に吸着します。塩の成長とともに表面積は増え、吸着するアミロイドβの量も増えます。その後、溶解により、これらのタンパク質が1カ所に集められ、濃縮され、毒性の凝集体が出現するのです (図1) 。
実は、私たちは、以前、超音波を照射することにより、アミロイドβの凝集が加速される現象を発見し、そのメカニズムを解明しました。超音波は圧縮・引張りの繰り返しの力を溶液に与えます。超音波の「引張り」により、溶液の圧力は低下して、小さな気泡が発生し、成長します(つまり局所的に沸騰します)。気泡は気体ですから、水が苦手なアミロイドβは好んで気泡の表面に吸着します。ところが、超音波の作用が「圧縮」に切り替わると、気泡は急激に押し縮められて圧壊します。このとき、表面に吸着したアミロイドβが気泡の運動に追随して、圧壊点に集められて、過度に濃縮されるために、毒性の凝集体が生み出されるのです (図3) 。
超音波は外部から我々が与える刺激ですが、実は、塩の一時的な析出と溶解という現象が、超音波と同じ作用を自然に起こしていたことになるのです。

図2 塩の一時的な析出・溶解現象を電子顕微鏡により直接観察した例
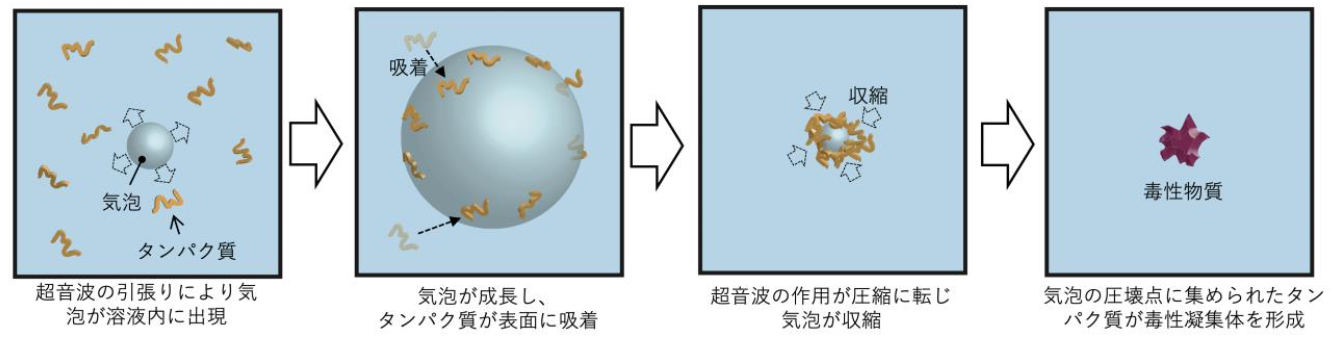
図3 超音波が作る気泡の成長と圧壊によるタンパク質の凝集加速現象
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、神経変性疾患にかかわるタンパク質には、同様に疎水性の部位が存在しますから、この新たに明らかとなった凝集メカニズムは、神経変性疾患の発症に共通した現象であるとも考えられます。こういった現象をより深く探究することにより、神経変性疾患の予防・治療に貢献すると考えられます。
特記事項
本研究成果は、2020年7月20日(月)に米国科学誌「The Journal of Physical Chemistry Letters」(オンライン)に掲載されました。
タイトル:"Time-Resolved Observation of Evolution of Amyloid-β Oligomer with Temporary Salt Crystals"
著者名:Kichitaro Nakajima, Tomoya Yamazaki, Yuki Kimura, Masatomo So, Yuji Goto, and Hirotsugu Ogi
参考URL
工学研究科 量子計測領域 荻研究室HP
http://www-qm.prec.eng.osaka-u.ac.jp/pmwiki/pmwiki.php
用語説明
- 析出
溶解している溶質が固体として現れる現象。
- 溶液TEM
通常の透過型電子顕微鏡は、試料を高真空環境内に設置して電子線を照射し、試料を透過した電子線を利用することにより、試料を観察する。Transmission Electron Microscopeという英語名から、TEMと呼ばれている。液中TEMでは、溶液状態の試料を、上下に窒化ケイ素の微小窓を有する200nm程度の薄さの微小容器に閉じ込めてシールし、この微小容器ごと高真空環境に設置して、微小窓に電子線を透過させることにより、溶液状態のまま透過画像を得ることができる電子顕微鏡である。
- アミロイドβ
分子量が約4500のタンパク質。疎水性の強いアミノ酸配列を含むため、それらの相互作用により凝集し、様々な凝集体を形成することがある。これらの凝集体が神経細胞内外に沈着し、神経毒性を発し、アルツハイマー病を発症させると考えられている。
