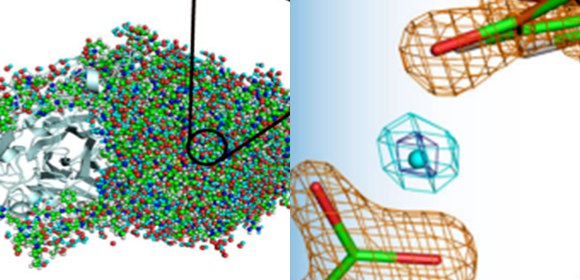
宙に浮く水素イオン?!
大型タンパク質の中性子結晶構造解析で見えた特異な世界
研究成果のポイント
・分子量の大きなタンパク質は結晶調製が難しく、高品質な大型結晶の作製は極めて困難とされてきた。
・様々な検討の結果、高分子量タンパク質の大型結晶の作製とこれを用いた中性子結晶構造解析 に成功した。
・酵素反応のしくみの解明に欠かせない“水素イオンの正確な位置”が明らかになった。
概要
大阪医科大学、大阪大学、量子科学技術研究開発機構、茨城大学、筑波大学らの研究グループは、大強度陽子加速器施設(J-PARC) 、物質・生命科学実験施設(MLF)の茨城県生命物質構造解析装置(iBIX) を用いた実験により、銅アミン酸化酵素 の高分解能中性子結晶構造解析に成功しました。本酵素は、これまでに中性子結晶構造解析が行われた中で最も大きなタンパク質(分子量:70,600)であり、小型タンパク質を主なターゲットとしてきた中性子結晶構造解析の適用範囲を大きく広げました。得られた構造からは、三方向からの酸素原子との相互作用により宙に浮いているかのようにみえる水素イオン(非局在化したプロトン)や、特異な補酵素構造など、水素原子核の位置が精密に決定されることにより初めて解明された重要な知見が得られました (図1) 。
本研究成果は、米国科学誌「Proceedings of the National Academy of Sciences of the United States of America」に公開されます。
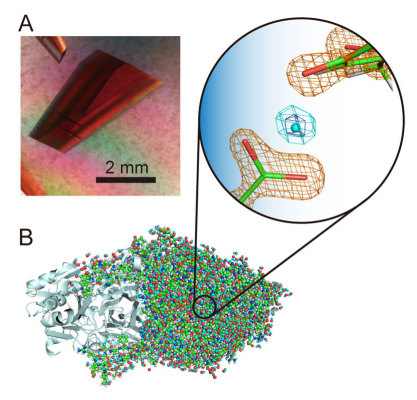
図1 (A)大型タンパク質、銅アミン酸化酵素の巨大な結晶。(B)同酵素の水素原子を含んだ立体構造とそこから見つかった“宙に浮いた”プロトン(拡大図中央)。
発表者
村川武志:大阪医科大学 医学部 助教
栗原和男:量子科学技術研究開発機構 量子生命科学領域 上席研究員
庄司光男:筑波大学 計算科学研究センター 助教
柴崎千枝:量子科学技術研究開発機構 量子生命科学領域
角南智子:量子科学技術研究開発機構 量子生命科学領域 主幹研究員
玉田太郎:量子科学技術研究開発機構 量子生命科学領域 グループリーダー
矢野直峰:茨城大学 フロンティア応用原子科学研究センター 助教
山田太郎:茨城大学 フロンティア応用原子科学研究センター 准教授
日下勝弘:茨城大学 フロンティア応用原子科学研究センター 教授
鈴木守:大阪大学 蛋白質研究所 准教授
重田育照:筑波大学 計算科学研究センター 教授
黒木良太:元日本原子力研究開発機構
林秀行:大阪医科大学 医学部 教授
矢野貴人:大阪医科大学 医学部 教授
谷澤克行:大阪大学 産業科学研究所 名誉教授
安達基泰:量子科学技術研究開発機構 量子生命科学領域 グループリーダー
岡島俊英:大阪大学 産業科学研究所 准教授
研究の背景
タンパク質などの立体構造を決定し、その機能とメカニズムを解明する構造生物学において、中性子結晶構造解析は、水素原子を含む構成全原子の位置を正確に決定することができる強力な研究手法です。しかし、極めて大きなタンパク質結晶が必要であり、一般に分子量の大きなタンパク質ほど結晶の大型化が難しいため、中性子結晶構造解析は、主に小型タンパク質を対象として行われてきました。我々の研究グループは様々な条件を検討した結果、これまでに例のない大きな分子量を持つ銅アミン酸化酵素(分子量 70,600)において、高品質の大型結晶 (約7mm 、図1A) の作製に成功しました。JPARCMLFのiBIXを用いて、得られた結晶の中性子回折実験を行った結果、大型タンパク質としては極めて高分解能 ※5 (分解能:1.72Å)の中性子結晶構造解析に成功しました。
特筆すべき成果として、活性中心において“宙に浮いた”プロトン (図1B拡大図) を観測したほか、補酵素トパキノンの六員環が湾曲し、補酵素はエノラート型とケト型の平衡状態として存在していることがわかりました (図2) 。さらに、銅イオンに配位したヒスチジン残基のプロトンが解離し、銅イオンとの結合が安定する (図3) ことなど、酵素反応の働きに中心的役割を果たす水素原子やプロトンの正確な位置が明らかとなりました。同時に、実験的に決定された水素原子核の位置に基づく量子化学計算によって、解離基のプロトン化状態やエネルギーレベルを理論検証することが可能となりました。これらの知見は、水素原子核の位置が精密に決定される中性子結晶構造解析によって初めて解明されたことであり、銅アミン酸化酵素の反応機構を理解するため極めて重要な成果となりました。
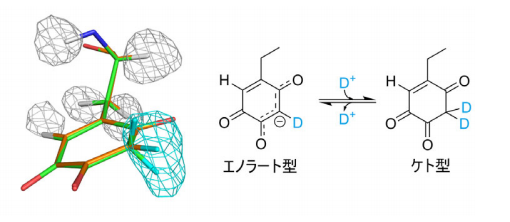
図2 補酵素トパキノンの構造と平衡状態。軽水素を灰色、重水素を水色の網目で示す。
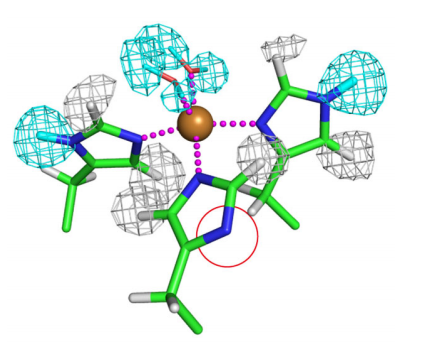
図3 銅イオンと結合したヒスチジン残基の構造。手前のヒスチジン残基には重水素が結合しておらず(赤丸で囲んだ部分)、特異なイミダゾレートアニオンが形成されていた。軽水素を灰色、重水素を水色の網目で示す。
本研究成果が社会に与える影響(本研究成果の意義)
今回の研究成果は、中性子結晶構造解析の適用範囲を大きく広げるものであり、高分子量の有用タンパク質や薬剤開発の標的タンパク質において、水素原子を含んだ立体構造決定につながるものと期待されます。また、本研究は、水素原子核の位置を実験的に決定することによって、これまで予想されなかった構造の存在や作用機構を明らかにできることを実証しており、中性子結晶構造解析の大きな可能性を示すものと考えられます。例えば、本研究で明らかになった“宙に浮いた”プロトンの存在は、極めて軽い質量を持つプロトンの量子的な性質を観察したものであり、近年提案されている、酵素の量子論的振る舞いを理解するうえで重要なデータとなるものと考えられます。
特記事項
本研究成果は、米国科学誌「Proceedings of the National Academy of Sciences of the United States of America」にオンライン公開されました。
タイトル:Neutron crystallography of copper amine oxidase reveals keto/enolate interconversion of the quinone cofactor and unusual proton sharing
著者名:Takeshi Murakawa, Kazuo Kurihara, Mitsuo Shoji, Chie Shibazaki, Tomoko Sunami, Taro Tamada, Naomine Yano, Taro Yamada, Katsuhiro Kusaka, Mamoru Suzuki, Yasuteru Shigeta, Ryota Kuroki, Hideyuki Hayashi, Takato Yano, Katsuyuki Tanizawa, Motoyasu Adachi, Toshihide Okajima
なお、本研究は、日本学術振興会科学研究費助成事業、および物質・デバイス領域共同研究拠点事業の支援を得て行われました。
研究者のコメント (岡島俊英准教授)
高品質の大型結晶を作ることは非常に困難でしたが、苦労のかいがあって想像以上に多くの知見が得られました。タンパク質を構成する原子のほぼ半数は水素原子であり、今後、中性子結晶構造解析が発展し、水素原子の検出が容易になれば、今まで予想すらしていなかったタンパク質分子のもつ機能が、次々と明らかにされていくのではないかと期待しています。
参考URL
大阪大学 産業科学研究所 第3研究部門 生体分子反応科学研究分野HP
https://www.sanken.osaka-u.ac.jp/organization/thi/thi_05/
用語説明
- 中性子結晶構造解析
結晶へ中性子を照射し、原子核との相互作用による散乱強度を調べることにより、結晶内に存在する分子の立体構造を得る分析法。同様の手法にX線結晶構造解析があるが、こちらは電子との相互作用を検出するものであり、電子を1つしか持たない水素原子の位置を決定することは極めて難しい。さらに、電子をもたないプロトンについては位置情報を得ることが不可能である。中性子結晶構造解析では水素原子(あるいはプロトン)の詳細な観察が可能であり、これが特に生命科学分野で中性子結晶構造解析を行う最大の目的である。中性子照射を行う際には、データのノイズを防ぐため、あらかじめ、結晶を重水に浸すことが多く、水素(軽水素)の一部は重水素に置き換わる。
- 大強度陽子加速器施設(J-PARC)
茨城県東海村にある大強度陽子加速器施設であり、J-PARCの名称は(Japan Proton Accelerator Research Complex)に由来する。素粒子物理、原子核物理、物質科学、生命科学、原子力など幅広い分野の最先端研究を行うための陽子加速器群と実験施設群より構成される。陽子を加速し、様々な粒子を発生することが可能であり、本研究では、物質・生命科学実験施設(MLF)において加速した陽子が水銀に衝突して発生する中性子を用いた。
- 茨城県生命物質構造解析装置(iBIX)
茨城県がJ-PARC MLFに設置した2本の中性子ビームラインのうちの一つであり、J-PARC MLFの強力なパルス中性子源を生かした世界最高峰の生体高分子用パルス中性子単結晶中性子回折装置である。
- 銅アミン酸化酵素
様々な生物種に幅広く存在する酵素タンパク質であり、一級アミン類をアルデヒドとアンモニアに分解する活性を持っている。その活性中心には、銅イオンと補酵素トパキノンを含んでおり、ヒトの血清中の本酵素は、糖尿病の発症にも関与している。
- 分解能
対象を識別できる能力の指標。一般的には“解像度”と同じような意味で用いられ、数値が小さいほど、細かい構造が正確に見分けられることを意味する。結晶構造解析の分野では、単位としてÅ(オングストローム、1Å=10 -10 m)を用いられることが多い。中性子結晶構造解析では、分解能2.5Å以上で重水素原子核を検出できるが、水素(軽水素)原子核の検出には2.0Å以上の高分解能が必要である。
