
世界初!1分子量子シークエンサーによりDNAに取り込まれた抗がん剤の直接観察に成功
抗がん剤のメカニズムを調べる技術
研究成果のポイント
・DNAに取り込まれた抗がん剤の直接観察に成功
・これまでDNAに取り込まれた抗がん剤を調べることができなかったが、1分子を識別する1分子量子シークエンサーを使うことで可能に
・抗がん剤の新たなメカニズムの解明により新薬の開発に期待
概要
大阪大学産業科学研究所の谷口正輝教授らの研究グループと大阪大学大学院医学系研究科の石井秀始特任教授(常勤)らの研究グループは、治療によってがん細胞のDNAに取り込まれた抗がん剤の挙動を直接観察することに世界で初めて成功しました。
これまでDNA中のチミンと抗がん剤が入れ替わることで、がん細胞の増殖が阻害されて抗腫瘍効果が発揮されるメカニズムが想定されてきましたが、DNAに取り込まれた抗がん剤を直接観察することはできませんでした。
今回、谷口教授・石井特任教授らの研究グループは、DNAの塩基分子を1分子ずつ識別できる1分子量子シークエンサー を用いることで、DNA中の核酸アナログ型の抗がん剤を直接観察するとともに、塩基配列を同時に決定することに成功しました。これにより、DNAの中に抗がん剤が取り込まれてDNAの機能が変化するメカニズムを解明するとともに、新たな抗がん剤の開発が期待されます。
本研究成果は、英国科学誌「Scientific Reports」に、3月7日(木)午後7時(日本時間)に公開されました。
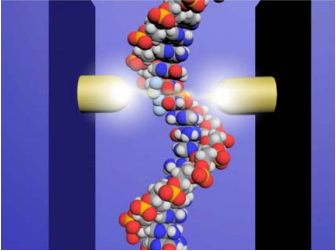
図1 1分子量子シークエンサーの原理図
研究の背景
フルオロチミン は、転移性大腸がん等の難治性消化器がんに効く抗がん剤として広く用いられています。フルオロチミンがDNA中のチミンと入れ替わることで、がん細胞の増殖を阻害すると考えられてきました。しかし、DNA中のどの位置にフルオロチミンが取り込まれているかを調べる方法がなく、抗がん剤のメカニズムとしては未知な部分が残されています。特にフルオロチミンのメカニズムの解明は、新たな抗がん剤を生み出すもととなるため、DNA中のフルオロチミンの挙動を直接観察する方法の開発が大きな課題でした。
谷口教授・石井特任教授らの研究グループでは、量子的な電流であるトンネル電流 により1分子を識別できる1分子量子シークエンサーの方法により、DNAの塩基配列とともに、DNA中の塩基配列のどの位置にフルオロチミンが存在するかを決定することに成功しました。これは、抗がん剤のメカニズムの解明を可能にすると期待されます。
さらに、この抗がん剤で処理されたがん細胞内のDNA中の塩基配列のどの位置にフルオロチミンが取り込まれて遺伝子の機能が変化しているのかを高い精度で明らかにすることで薬が効くメカニズムを明らかにし、新薬の開発へとつなげていきます。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、抗がん剤のメカニズムの解明と、新たな抗がん剤の開発が期待されます。この解析手法は、抗がん剤が効くかどうかを個人のゲノムレベルで調べる新たな手法となる可能性があります。さらにこの結果を機械学習と融合させることにより、発見されていない修飾塩基分子等の遺伝子異常を高精度に診断することができるゲノム情報に基づく精密医療(Precision Medicine)への応用が期待されます。
特記事項
本研究成果は、2019年3月7日(木)午後7時(日本時間)に英国科学誌「Scientific Reports」(オンライン)に掲載されした。
タイトル:“Direct Analysis of Incorporation of an Anticancer Drug into DNA at Single-Molecule Resolution”
著者名:Takahito Ohshiro, Yuuki Komoto, Masamitsu Konno, Jun Koseki, Ayumu Asai, Hideshi Ishii, and Masateru Taniguchi
なお、本研究は、科学研究費補助金・基盤研究(S)、科学技術振興機構(JST)戦略的創造研究推進事業(CREST)の鷲尾チームの研究の一環として行われました。
参考URL
大阪大学 産業科学研究所 バイオナノテクノロジー研究分野
http://www.bionano.sanken.osaka-u.ac.jp/
用語説明
- 1分子量子シークエンサー
量子的な電流であるトンネル電流により、DNAやRNAの塩基配列やペプチドのアミノ酸配列を決定する第4世代のシークエンサー
- フルオロチミン
チミンのアミノ基の水素原子が、全てフッ素に置換された分子
- トンネル電流
1分子のわずかな電子状態の違いを読み出す電流
