細菌のIII型分泌装置の機能を試験管中で再現!
食中毒菌の病原性のみを奪う薬剤スクリーニングに期待
研究成果のポイント
・III型分泌装置 を試験管内で再構成し、タンパク質輸送とべん毛 構造形成を再現。
・III型分泌装置は、ATP加水分解エネルギー とプロトン駆動力 のどちらのエネルギーでも作動する「ハイブリットエンジン型」の器官であることを実証。
・この実験系を使うことで、III型分泌装置を標的とした病原性のみを奪う新規薬剤の迅速なスクリーニングに期待。
概要
大阪大学大学院理学研究科の今田勝巳教授、寺島浩行特任助教(常勤)(現:名古屋大学大学院理学研究科助教)、大学院生命機能研究科の川本晃大特任助教(常勤)(現:蛋白質研究所特任助教(常勤))、南野徹准教授、難波啓一特任教授の共同研究グループは、細菌のべん毛III型分泌装置を試験管内で再構成し、タンパク質の輸送と細菌べん毛の構築を再現することに世界で初めて成功しました。
III型分泌装置は数百のタンパク質分子が集合してできた器官で、細菌の運動器官であるべん毛の形成や細菌のヒトや動物への感染装置として働きます。本研究グループは、開発した試験管内再構成実験系を用いて、III型分泌装置がATP加水分解エネルギーとプロトン駆動力という異なるエネルギーのどちらでも作動する、いわば「ハイブリットエンジン型」の装置であることを明らかにしました。また、今回成功した実験系は、III型分泌装置をターゲットとした感染症薬剤のハイスループット探索 を可能にするもので、サルモネラ菌や病原性大腸菌O-157といった病原性細菌の病原性を奪う新規抗菌薬の開発にもつながると期待されます。
本研究成果は、2018年6月26日(米国東部時間)に米国科学誌「mBio」にオンライン公開されました。
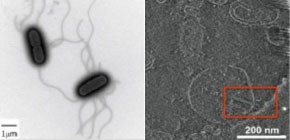
図1 サルモネラ属菌の電子顕微鏡写真。楕円形の菌体の周囲から複数のべん毛繊維が伸びている。
研究の背景
多くの細菌は、べん毛とよばれるタンパク質でできた繊維状の器官をスクリューのように使って水中や腸内を移動します (図1) 。べん毛は細胞の外に形成されるので、べん毛をつくるためには、べん毛タンパク質を細胞外へ輸送する必要があります。このとき働くのが、III型分泌装置です (図2) 。III型分泌装置はべん毛だけでなく、インジェクチソーム (”毒針”とも呼ばれる)とよばれる細菌の病原タンパク質の輸送器官にも存在します。
サルモネラ属菌や病原性大腸菌O-157、腸炎ビブリオなどの病原細菌は、べん毛を使って感染のターゲットとなる宿主細胞 まで移動し、インジェクチソームから病原タンパク質を宿主細胞に直接注入し、宿主細胞を乗っ取って感染が成立します (図3) 。したがって、病原性細菌の移動手段や感染手段を奪うことができれば、病原細菌を害のない普通の細菌にすることができます。このことから、III型分泌装置をターゲットにした病原性のみを壊す新規薬剤の開発が期待され、III型分泌装置のしくみを探る様々な研究が行われています。しかし、細菌を解析する従来の方法では、実験条件のコントロールが難しく、輸送を正確に計測することができません。そこで輸送装置を取り出して輸送を試験管内で再現して調べようとする試みが世界中で行われていました。しかし、III型分泌装置は数百のタンパク質分子で構成される複雑な構造体であるため、誰も成功していませんでした。
図2 細菌べん毛(左)とインジェクチソーム(右)の模式図。菌体表層上に緑色で示した基部構造が存在し、その内側に橙色のIII型分泌装置が存在している。
図3 病原細菌の生活環
研究の内容
本研究グループは、試験管内でIII型分泌装置のタンパク質輸送を再現するために、反転膜小胞に着目しました (図4) 。反転膜小胞は、細胞の内と外をひっくり返して作った小胞で、細胞の内側になる膜面が外を向いています。そのため、反転膜小胞に外から物質やエネルギーを加えるだけで、タンパク質輸送に必要な物質や量、エネルギーを調べることができるようになり、実験のコントロールも容易になります。また、輸送されたタンパク質は小胞内に蓄まるので定量的な計測も可能になります。
本研究グループは、III型分泌装置を壊さずに反転膜小胞を作製し精製する方法を見出し、実際に小胞内へのタンパク質輸送を行わせることに成功しました。また、外からべん毛を構成するタンパク質を加えることで、小胞内にべん毛構造ができることを確認し (図5) 、反転膜小胞中のべん毛III型分泌装置が生きた細菌が持つ機能を完全に保持していることを実証しました。そこで、この実験系を用いて輸送に必要なエネルギーを調べました。すると、これまでの知見と異なり、輸送に必要とされるATP加水分解エネルギーとプロトン駆動力のどちらか片方のエネルギーさえあれば輸送が起こることがわかりました。この結果から、III型分泌装置がそれぞれのエネルギーを独立して使うことのできる「ハイブリッドエンジン型」の装置であることが明らかになりました。
図4 (A)反転膜小胞の作製方法。(B)反転膜小胞のクライオ電子顕微鏡像
図5 反転膜小胞内にできたべん毛構造
本研究成果が社会に与える影響(本研究成果の意義)
現在、先進国では細菌感染症は抗生物質で治ると思われています。しかし、現実には安易な抗生物質の処方により多剤耐性菌が数多く出現し、問題になっています。そのため、抗生物質ではない、新しいコンセプトの細菌感染症薬の開発が望まれています。そのターゲットの一つがIII型分泌装置です。III型分泌装置を不活化できれば病原性細菌の病原性のみを奪うことができます。菌を殺さないため耐性菌ができにくく、善玉菌などの腸内細菌叢も破壊されない利点があります。また、III型分泌装置は細菌特有の器官であるため、副作用が出にくいことが期待されます。反転膜小胞を用いたIII型分泌装置阻害剤のハイスループットスクリーニングを行うことで、今後そのような化合物を見出せる可能性は高いと考えられます。将来的には細菌感染症を制御するための新技術として社会貢献することが期待されます。
特記事項
本研究成果は、2018年6月26日(火)(米国東部時間)に米国科学誌「mBio」(オンライン)に掲載されました。
タイトル:“In vitro reconstitution of functional type III protein export and insights into flagellar assembly (III型タンパク質輸送の機能的な試験管内再構成とべん毛形成メカニズムに関する知見)”
著者名:Hiroyuki Terashima 1 , Akihiro Kawamoto 2 , Chinatsu Tatsumi 1 , Keiichi Namba 2,3 , Tohru Minamino 2 and Katsumi Imada 1 (寺島浩行、川本晃大、巽千夏、難波啓一、南野徹、今田勝巳)
所属: 1 大阪大学大学院理学研究科、 2 大阪大学大学院生命機能研究科、 3 理化学研究所生命システム研究センター
なお、本研究は、科学研究費補助金基盤研究(S,A,B)、特別推進研究および新学術領域研究「少数性生物学」、「動的構造生命」による支援のもとに行われました。
参考URL
大阪大学 大学院理学研究科 高分子科学専攻 高分子構造科学研究室
http://www.chem.sci.osaka-u.ac.jp/lab/okuyama/
用語説明
- III型分泌装置
細菌べん毛やインジェクチソームに存在するタンパク質輸送装置。べん毛では構成タンパク質がIII型分泌装置を通って細胞外へ輸送され、べん毛が形成される。また、インジェクチソームでは、細菌感染に重要なエフェクターと呼ばれる病原性タンパク質の宿主細胞への送り込みを行う。
- べん毛
細菌の持つ運動器官の一つ。数万分子のタンパク質が集まり出来た、らせん繊維状の構造体で、スクリューのように回転させて推進力を生み出す。
- ATP加水分解エネルギー
生物のエネルギーの通貨とも呼ばれるATP(アデノシン三リン酸)が加水分解され、ADP(アデノシン二リン酸)とリン酸が生じるときに生まれる化学エネルギー。
- プロトン駆動力
細胞膜に生じる膜電位と膜内外のイオン濃度勾配(プロトン駆動力の場合イオン濃度はpHを示す)によって定義されるエネルギー。通常、細胞膜の内と外ではイオンの数が異なり、細胞内外でのpHも異なるため、絶縁体として働く細胞膜の内外に電気的なエネルギー差が生じる。
- ハイスループット探索
高速で高効率な探索のこと。数多くの化合物の効果を調べる(スクリーニングする)とき、高速に効果を評価できる実験系があれば、新規の化合物を見出す可能性が高くなる。
- インジェクチソーム
細菌の持つ病原性タンパク質輸送体。腸内病原性細菌の多くは、注射針の形をしたインジェクチソームを宿主細胞に刺して病原性タンパク質を直接送り込む。送り込まれた病原性タンパク質は、宿主細胞のアクチン繊維の再構成やシグナル伝達経路を撹乱して細菌に都合のよい状態に宿主細胞を改変し、感染が成立する。
- 宿主細胞
細菌等の感染相手となる細胞。
