神経ガイダンス因子が、免疫と代謝をつなぐ
免疫・炎症疾患における栄養・代謝の重要性が明らかに
研究成果のポイント
・神経・免疫・代謝が分子レベルで相互に連携していることを発見した。
・神経ガイダンス因子が代謝を調節することで炎症をコントロールしている。
・慢性の免疫疾患、炎症疾患の治療への応用が期待される。
概要
大阪大学大学院医学系研究科の熊ノ郷淳教授(呼吸器・免疫内科学)、免疫学フロンティア研究センターの姜秀辰寄附研究部門助教(免疫機能統御学/感染病態)らの研究グループは、神経に関わるとされてきたセマフォリン 6Dが栄養・代謝シグナルを調節することで、組織の恒常性に大切なM2マクロファージ の生成に関わっていることを明らかにしました (図1) 。栄養や代謝を調節することで、慢性の免疫・炎症疾患(炎症性腸疾患など)の治療に繋がることが期待されます。
代謝のシグナルが免疫に重要な役割を果たしていることが注目され始めていますが、これらがどのように連携しているのか、詳しい分子メカニズムは分かっていません。
今回、熊ノ郷教授らの研究グループは、神経発生に関わる神経ガイダンス因子とされてきたセマフォリン6Dにより代謝調節の鍵分子PPARγ の発現が調節され、組織の恒常性の維持や抗炎症作用のあるM2マクロファージの誘導に関わっていること、さらに、この仕組みが破綻すると炎症性腸疾患症状を発症し易くなることを明らかにしました。これにより、将来的に栄養・代謝調節による慢性の免疫・炎症疾患の治療に繋がると期待されます。
本研究成果は、米国科学誌「Nature Immunology」に5月19日(土)午前0時(日本時間)公開されました。
研究の背景
昔から、「病は気から」「栄養をつけないと抵抗力が落ちる」と言われてきましたが、代謝と免疫の関係や、どのような仕組みで起こるのかということについては解明されていません。臨床医学研究では、1980年代以降の分子生物学的手法の導入により、免疫調節に関わるシグナル分子を標的にした薬剤が臨床応用されおり、病態解析において、代謝学的な視点は免疫調節や免疫疾患の研究の中でなおざりにされた経緯がありました。しかし、代謝センサーmTOR(エムトール) とその関連分子の発見等を契機に、代謝シグナルが免疫・炎症細胞の活性化・分化に重要な役割を果たしていることが明らかになり「免疫代謝(Immunometabolism)」という研究分野が大きな注目を集めています。
熊ノ郷教授らの研究グループは、これまでに、免疫と代謝に関する研究において、細胞内で生成されたアミノ酸によりmTORを介してM2マクロファージが活性化されることを見出しています。その後、栄養・代謝センサーであるmTORシグナルの下流に何があるのかをマイクロアレイ解析で調べたところ、神経ガイダンス因子と言われているセマフォリン6Dが見つかり、今回、この分子と代謝、免疫の関係を詳しく調べました。
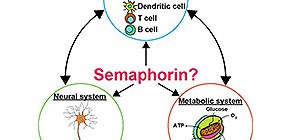
図1 セマフォリンの役割
セマフォリンを介して代謝と免疫が繋がれていることが分かった。
本研究の成果
研究グループは、マクロファージではmTORシグナルにより、セマフォリン6Dの発現が誘導されることに着目し、セマフォリン6Dの遺伝子を持たない(欠損)マウスを作製しました。セマフォリン6D欠損下では、マクロファージで脂質代謝の鍵分子であるPPARγ(ピーパーガンマ)の発現が低下しており、組織の恒常性の維持や抗炎症に関わるM2マクロファージが産生されませんでした。
次に、体内でのM2マクロファージによる抗炎症作用の獲得にセマフォリン6Dが関わっているかを調べました。通常のマウスで、体内のマクロファージをセマフォリン6D欠損型に置き換えた後に、DSSという化学物質で腸炎を誘導すると、腸炎を発症しました。それに対して、セマフォリン6D欠損マウスのマクロファージを通常のマウスのマクロファージに置き換えて、DSS誘導を行っても腸炎は発生しませんでした。よって、腸の恒常性における抗炎症作用に、セマフォリン6Dが重要な役割を果たしていることが分かりました。
これらの結果より、mTORのシグナルを受けた神経ガイダンス因子セマフォリン6Dは、M2マクロファージを誘導し炎症を抑えますが、その間にはセマフォリン6Dの細胞内の領域から伝達されるPPARγを介して代謝を制御していることが分かりました (図2) 。これは、神経と代謝、代謝と免疫、免疫と神経が相互に連関していることを直接分子レベルで証明したことになります。
さらに、炎症疾患の治療において、従来の免疫調節薬だけでなく、代謝調節の重要性が示されることになります。
図2 セマフォリン6Dを介したM2マクロファージの誘導
サイトカインの刺激からM2型マクロファージが誘導されるまでには、mTORの下流にあるセマフォリン6DのシグナルによりPPARγを通じてマクロファージの脂質代謝が変わる。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、慢性の炎症性疾患の治療において、単に免疫調節薬で病勢をコントロールするだけでなく、日常の栄養、代謝状態を維持・管理することが有用な可能性があり、今後治療治療薬選定・開発の手掛かりになることも期待されます。
特記事項
本研究成果は、米国科学誌「Nature Immunology」に5月19日(土)午前0時(日本時間)に公開されました。
【タイトル】“Semaphorin 6D reverse signaling controls macrophage lipid metabolism and anti-inflammatory polarization”
【著者名】Sujin Kang , Yoshimitsu Nakanishi , Yoshiyuki Kioi 1,2 , Daisuke Okuzaki 3 , Tetsuya Kimura 1 , Hyota Takamatsu 1,2 , Shohei Koyama 1,2 , Satoshi Nojima 1,7 , Masayuki Nishide 1,2 , Yoshitomo Hayama 1,2 , Yuhei Kinehara 1,2 , Yasuhiro Kato 1,2 , Takeshi Nakatani 1,2 , Tomomi Shimogori 8 , Junichi Takagi 4 , Toshihiko Toyofuku 1,6 , Atsushi Kumanogoh 1,2※ (※責任著者)
【所属】
1. 大阪大学 免疫学フロンティア研究センター 感染病態
2. 大阪大学 大学院医学系研究科 呼吸器・免疫内科学
3. 大阪大学 微生物病研究所 遺伝情報実験センター
4. 大阪大学 蛋白質研究所 分子創製学
5. 大阪大学 免疫学フロンティア研究センター 免疫機能統御学
6. 大阪大学 大学院医学系研究科 免疫再生制御学
7. 大阪大学 大学院医学系研究科 病態病理学
8. 理化学研究所 脳科学総合研究センター 視床発生研究チーム
本研究課題は、国立研究開発法人日本医療研究開発機構(AMED)、革新的先端研究開発支援事業(AMEDCREST)の研究開発領域「炎症の慢性化機構の解明と制御に向けた基盤技術の創出」における研究開発課題「慢性炎症におけるガイダンス因子の病的意義の解明とその制御」(研究開発代表者:熊ノ郷淳)の一環として行われました。なお、AMED-CREST研究開発領域は、平成27年4月の日本医療研究開発機構の発足に伴い、国立研究開発法人科学技術振興機構(JST)より移管されたものです。
参考URL
大阪大学 大学院医学系研究科 呼吸器・免疫内科学
http://www.imed3.med.osaka-u.ac.jp/
用語説明
- セマフォリン
1990年代初頭に発生の過程で神経の伸長に関わるガイダンス因子とされてきたタンパク質群で、20種類ほどのメンバーがある。熊ノ郷教授らの研究が端緒になり、免疫の制御に関わることが明らかにされている。セマフォリン6Dは免疫や骨に重要な因子として同定されたが、2017年には神経にも重要な役割を果たしていることが示されている。
- M2マクロファージ
炎症細胞であるマクロファージは、サイトカインや細菌の刺激成分等によるシグナルに応じてM1型とM2型など異なる機能を持つタイプに分かれる。M2マクロファージは、抗炎症、組織の恒常性の維持に関与するタイプのマクロファージである。
- PPARγ
(ピーパーガンマ;Peroxisome Proliferator-Activated Receptor γ):
脂質代謝の鍵分子とされている転写因子。
- mTOR
(エムトール、エムトア;Mammalian target of rapamycin):
栄養や代謝物を感知する代謝センターと考えられていて、糖、アミノ酸、インスリンなどのシグナルを感知して代謝制御に関わっているリン酸化酵素。
