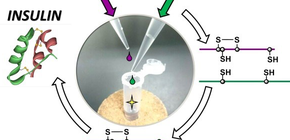
東海大学、大阪大学、東北大学、福岡大学の共同研究グループ インスリンの簡便な化学合成法を開発
糖尿病患者が増加する中、新しいインスリン製剤技術としての応用に期待
本研究成果のポイント
・化学修飾などを施していないインスリンの構成ポリペプチド鎖(A鎖とB鎖)が自己組織化してインスリン分子の構造になるメカニズムの全容を解明した。
・メカニズムをもとに、自己組織化の条件を最適化したところ、インスリンが約40%の収率で得られた。
・複雑な実験技法を必要とせず、A鎖とB鎖を1:1で混ぜるだけで目的のインスリンが得られる。
・遺伝子工学的な手法を一切用いないために大掛かりな製造設備を必要としない。
概要
東海大学(所在地:神奈川県平塚市北金目4-1-1、学長:山田清志〔やまだきよし〕)理学部化学科講師の荒井堅太および同学科教授の岩岡道夫、ならびに大阪大学(所在地:大阪府吹田市山田丘1-1、総長:西尾章治郎〔にしおしょうじろう〕)蛋白質研究所教授の北條裕信、東北大学(所在地:宮城県仙台市青葉区片平2-1-1、総長:大野英男〔おおのひでお〕)多元物質科学研究所教授の稲葉謙次および同大学学際科学フロンティア研究所助教の奥村正樹、福岡大学(所在地:福岡県福岡市城南区七隈8-19-1、学長:山口政俊〔やまぐちまさとし〕)理学部化学科の安東勢津子(開発当時:講師、現在:非常勤講師)らの研究グループは、インスリンを構成する2本の異なるポリペプチド鎖(A鎖およびB鎖)が水溶液中で自己組織化してインスリンの構造を獲得するメカニズムの全容を解明しました。さらに、その知見をもとにA鎖およびB鎖を水溶液中で混合するだけで、目的のインスリンを得る簡便なインスリン合成法も開発。化学合成技術を基盤とした新しいインスリン製剤技術としての応用が期待されます。
本研究グループは、インスリンの簡便な化学合成法の開発に成功しました。血糖値降下作用をもつ「インスリン」は糖尿病患者が使用する静脈注射製剤として広く知られています。しかし、インスリンは2本の異なるポリペプチド鎖(A鎖とB鎖)が2対のジスルフィド結合とよばれる化学結合でリンクした特徴的な分子構造をもっており、その化学合成は容易ではありません。インスリンの化学合成では、世界中の研究グループが様々な手法を試みてきましたが、手法の煩雑さなどの理由からインスリン製剤の製造応用へ展開された例はありません。今回の研究成果で、本研究グループは化学修飾などを施していない天然のA鎖とB鎖が溶液中で自己組織化し、インスリンの構造になるメカニズムの全容を明らかにしました。そのメカニズムに基づいて反応条件を最適化したところ、インスリンを約40%の収率で得ることに成功しました。
今回の合成法の利点は、遺伝子工学的な手法を一切用いないため、大掛かりな製造設備を必要としない点やA鎖とB鎖を混ぜ合わせるというごく単純な操作で目的のインスリンが得られる点です。
本研究成果は、東海大学理学部化学科、大阪大学蛋白質研究所、東北大学多元物質科学研究所および同大学学際科学フロンティア研究所、福岡大学理学部化学科が共同で実施した研究の成果です。また、研究を実施するにあたり、文部科学省科学研究費助成事業(東海大学)、公益財団法人武田科学振興財団(東北大学)、公益財団法人上原記念生命科学財団(東北大学)、国立研究開発法人科学技術振興機構CREST(東北大学)、物質・デバイス領域共同研究拠点(東北大学)から資金援助をいただいております。
なお、本研究成果は、5月3日(木)付でイギリスの国際化学誌「CommunicationsChemistry」電子版に掲載されました。
https://www.nature.com/articles/s42004-018-0024-0 DOI:10.1038/s42004-018-0024-0
研究の背景
世界保健機関(WHO)の発表によると、世界の成人の糖尿病患者数は2014年までに4億人を超えており、先進国、発展途上国を問わず、現在も増加傾向にあります。それに伴ってインスリン製剤の需要は今後もますます高まるものと予想されます。食後の血糖値をコントロールする薬剤として、一般的によく知られている「インスリン」ですが、その調製は容易ではありません。これは、インスリンが、2本の異なるポリペプチド鎖(A鎖とB鎖)が硫黄(S)原子同士のジスルフィド(SS)結合によってリンクした特徴的な構造をもっていることに起因します (図1) 。つまり、普通にA鎖とB鎖を混合しただけでは、各ポリペプチド鎖内のSS結合の架橋が優先してしまうため、目的のインスリンはほとんど得られません。そのようなインスリン調製法は、実際に、インスリンの化学合成の歴史のごく初期(約60年前)において、複数の海外のグループによって報告されていますが、最終的なインスリン収率は1~5%程度と非常に低く、製造技術としては不適切であると結論付けられました。その後、化学技術の進歩に伴い、A鎖とB鎖のS原子上に化学修飾を施し、それらを段階的に外しながら選択的にSS結合を架橋する技法や( 図1 -a)、生合成機構を模倣して、リンカーペプチドによってA鎖とB鎖がつながった一本鎖のインスリンを合成し、SS結合の架橋後にリンカー部位を切除する技法( 図1 -b)など、さまざまな技法が提案されてきました。しかしながら、いずれも多段階な操作を経由する上に、熟練された実験技法を要するため、効率よくインスリンを得られるものではありませんでした。
本研究グループは昨年、システインの代わりにセレノシステイン(システインの硫黄原子をセレン原子に置換したアミノ酸)をA鎖とB鎖に組み込むことで、A鎖とB鎖が自発的にジセレニド結合(SeSe結合)で架橋して天然型のインスリン(セレノインスリン)が効率的に得られることを報告しました(2017年4月11日プレスリリース)。このことは、自己組織化してインスリンとなる性質をA鎖とB鎖が潜在的に持っていることを示すものでありました。そこで今回、同研究グループは、あえて原点回帰し、単純かつ最も合理的な天然のA鎖とB鎖の自己組織化(Native Chain Assembly; NCA)を利用する技法( 図1 -c)を再考することにしました。
インスリンを効率よく得るために、まず本研究グループはインスリンのA鎖とB鎖が水溶液中でインスリンの構造を獲得(フォールディング)するメカニズムの全容解明に取り組みました。A鎖とB鎖を水溶液中で混合すると、各ポリペプチド鎖内でSS結合が架橋されたものやSS結合を掛け違えたもの、SS結合が欠損したものなど多くの中間体が観測されます。それらを一つずつ構造と反応性などの観点から緻密に分析を行ったところ、 (図2) に示すような主経路を通ってインスリンが生成することがわかりました。特に重要なことは、インスリンのSS結合が1対欠損した安定な前駆体(2SS * )を経由する点であり、いかにこの2SS * を安定化させ、生成量を多くするかが、本手法の効率化の鍵であると考えられます。
こうして明らかになったメカニズムをもとに、インスリンが最も効率よく生成する条件を探索する中で、温度やpHを綿密に検討したところ、–10°C、pH10.0の条件下でインスリンが良好な収率で得られることが明らかになりました。さらに、生体内のタンパク質中のSS結合架橋を促す生体酵素(プロテインジスルフィド異性化酵素;PDI)をごく少量添加することで、反応時間の短縮と収率向上が確認されました。反応溶液の高速液体クロマトグラフィー(HPLC)分析の結果から、出発物質であるA鎖とB鎖のピークが、反応後ではインスリンのピークに収束している様子が確認でき (図3) 、ウシ膵臓インススリンの場合、最適条件下において最高収率は39%。同様にヒトインスリンでは49%、インスリンと同様の構造をもつ類似ペプチドホルモンであるヒト2型リラキシンでは47%の収率で得られました。
このように、本手法では、遺伝子工学的な手法を一切用いないために大掛かりな製造設備を必要とせず、A鎖とB鎖を約1:1で混ぜ合わせるというごく単純な操作で目的のインスリンを得ることができます。将来的には、化学合成技術を基盤とした新しいインスリン製剤技術としての応用が期待されます。
図1 インスリンの化学合成。(a)複数の保護基とその脱保護を利用した段階的なSS結合架橋法による合成法。(b)人工のリンカーペプチドを利用した生合成機構の模倣による合成法。(c)本研究で開発した天然のインスリンA鎖およびB鎖の自己組織化を利用した合成法。
図2 Native Chain Assemblyによるインスリン分子構築の主経路(1)→(2)→(3)。
図3 NCAによって得られたサンプル溶液のHPLC分析の結果。(a)反応前。(b)反応から80時間後。
参考URL
大阪大学 蛋白質研究所 蛋白質有機化科学研究室
http://www.protein.osaka-u.ac.jp/organic/index.html
用語説明
- ポリペプチド鎖
構成単位であるアミノ酸がペプチド結合と呼ばれる結合で多数連なった生体高分子の総称。体内で、ある生理機能を果たしているポリペプチド鎖はタンパク質と呼ばれる。ゆえに、インスリンもタンパク質の一種。アミノ酸は主に20種類存在し、これらの連なる順番や数によってポリペプチド鎖の構造と機能が制御されている。
- インスリン製剤
膵臓の中に島状に散在し、内分泌機能を果たす細胞群であるランゲルハン島から分泌される血糖抑制に関わるタンパク質であり、糖尿病患者はインスリン分泌がうまくいかず、皮下注射によってインスリン製剤を投与する必要がある。インスリン製剤の合成では、①複数の保護基でシステインチオール基を保護し、段階的な脱保護と鎖間のジスルフィド架橋を行う化学的手法、②生合成機構を模倣し、A鎖とB鎖をリンカーペプチドで連結し、SS結合を架橋後、リンカー部位を切除する方法――の主に2つの複雑な合成戦略が用いられてきた。
- ジスルフィド(SS)結合
タンパク質の構造安定化因子の一つ。アミノ酸の一種であるシステインはチオール(SH)基という硫黄(S)を含む部位を持ち、2つのSH基が酸化することでSS結合が形成される。
- セレノインスリン
インスリンのA鎖とB鎖の間で架橋される1対のSS結合の硫黄原子を安定性に富んだセレン(Se)原子に置き換えた人工インスリン。立体構造と生理活性が天然のインスリンと同じでありながら、インスリン分解酵素(IDE)に分解されにくい性質を持つため、体内で薬効が長時間持続する新たなインスリン製剤として糖尿病治療などへの応用が期待されている。
- Native Chain Assembly; NCA
化学修飾などを持たない天然のインスリンA鎖とB鎖がSS結合の架橋を経て自己組織化(フォールディング)してインスリンの構造を構築すること。
- プロテインジスルフィド異性化酵素;PDI
細胞小器官の一つである小胞体内に存在する酸化還元酵素の一つ。生合成されたポリペプチド鎖は、一般的に小胞体内で特定の位置にSS結合が架橋されることで、天然立体構造を構築(フォールディング)し、タンパク質としての機能を発揮する。PDIは生体内および試験管内で、この過程におけるSS結合の架橋を効率よく促す機能を持つ。
- 高速液体クロマトグラフィー(HPLC)分析
溶液中のポリペプチド鎖の成分分析法の一つ。NCA反応溶液中で生成されるフォールディング中間体の化学的性質の違いを利用して、それぞれを分離することが可能である。混合溶液をHPLCに注入すると、一定流速下で各成分が分離され溶出時間に差がでる。検出されたピーク面積から各成分を定量評価する(どのくらいの量が溶けているか見積もる)こともできる。
