難治性血管炎の「免疫チェックポイント分子」を発見
セマフォリン4Dの研究が病態解明の手掛かりに
本研究成果のポイント
・好中球が関わる免疫難病、ANCA 関連血管炎の病態を解明する免疫チェックポイント分子を発見
・セマフォリン4D(SEMA4D)が好中球の活性を制御する機能を有していることおよびそのメカニズムを解明
・「好中球の免疫チェックポイント加療」による、血管炎治療への応用に期待
概要
大阪大学大学院医学系研究科の西出真之助教、熊ノ郷淳教授(呼吸器・免疫内科学)らの研究グループは、セマフォリン4D(SEMA4D)というタンパク質が好中球の活性を制御する免疫チェックポイント分子として働き、免疫難病のひとつであるANCA関連血管炎の病態に重要な役割を果たしていることを明らかにしました。
ANCA 関連血管炎(AAV)は発熱、体重減少といった全身症状の他、皮膚、神経、肺、腎臓などに重篤な臓器障害を生じる免疫難病であり、日本における患者数は約1万人と言われています。治療にはステロイドなどの強力な免疫抑制剤が用いられますが、副作用等の懸念から、より安全で、効果的な治療薬が求められています。
また、セマフォリン分子群は、神経発生、免疫、血管、骨疾患、神経変性疾患、がんの転移、浸潤などに関与する「ヒトの病気の鍵分子」であり、創薬ターゲットとして注目を集めているタンパク質群です。今回、本研究グループは、好中球上に発現しているSEMA4Dが「免疫チェックポイント分子」として好中球の不適切な活性化を阻止するブレーキ役として働いており、このブレーキが外れてしまうことがANCA関連血管炎の発症に関わっていることを解明しました (図1) 。本成果は、SEMA4Dを介した「好中球の免疫チェックポイント加療」による血管炎治療への応用が期待できます。
本研究成果は、リウマチ・自己免疫疾患の臨床・研究領域では最も権威があるとされる、欧州リウマチ学会誌「Annals of the Rheumatic Diseases」に、4月18日(火)午前0時(日本時間)に公開されました。
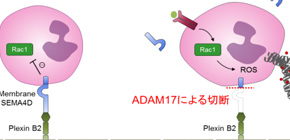
図1 AAV発症のメカニズム
血管に発現する「PlexinB2」と、好中球に発現する「セマフォリン4D」が結合し、好中球の暴走にブレーキをかけている。
AAV患者では、ADAM17という酵素の働きによって好中球のセマフォリン4Dが切断され、好中球のブレーキがはずれ、不適切に活性化している。
研究の背景
好中球細胞質抗体関連血管炎(ANCA関連血管炎:AAV)は好中球の細胞質成分(MPO/PR3)に対する自己抗体(抗好中球細胞質抗体、anti-neutrophil cytoplasmic antibody:ANCA)の出現を特徴とする、小型血管に炎症を生じる免疫難病です。発熱、体重減少といった全身症状のほか、皮膚、神経、肺、腎臓などに重篤な臓器障害を生じる免疫難病であり、日本における患者数は約1万人、好発年齢は60~70代、男女比1:1と言われています。また、セマフォリン分子群は神経軸索のガイダンス因子として発見された分子ですが、近年では血管新生、腫瘍免疫、骨代謝、自己免疫調節などにおいても重要な役割を果たしていることが明らかになっており、「ヒトの病気の鍵分子」であることから創薬ターゲットとして現在注目を集めているタンパク質群です。
免疫細胞の活性化にブレーキをかけるタンパク質は「免疫チェックポイント分子」と呼ばれています。Tリンパ球の免疫チェックポイント分子であるPD-1はがん免疫における治療標的分子として近年注目されていますが、最も数の多い白血球である好中球では、その免疫チェックポイント分子はこれまで不明でした。
本研究の成果
セマフォリン4D(SEMA4D)は、通常は膜型のタンパク質として存在しますが、細胞表面で切断されることにより、遊離型に変化して細胞内もしくは細胞間のシグナル伝達に関わっています。また、膜型SEMA4Dは、シグナルを「与える」だけではなく、Plexin-B2というタンパク質と結合し、シグナルを「受ける」受容体としても作用するユニークな分子です。
今回、本研究グループは、難治性の自己免疫疾患であるAAVの患者血清で、遊離型SEMA4D濃度の上昇と、血管炎の臨床スコアとが有意に相関していることを発見しました。また、血管炎患者の白血球は、好中球で特異的に膜型SEMA4Dが減少しており、好中球上ではADAM17という酵素による切断を受けて、膜型SEMA4Dの発現が低下していることが示唆されました。
さらに、SEMA4Dの役割を追究するため、SEMA4Dを発現しないノックアウトマウスの好中球を用いて実験を行いました。好中球と血管内皮細胞とを一緒に培養すると、通常のマウスの好中球では血管炎の病態に重要な好中球細胞外トラップ(NET)の形成が抑えられますが、SEMA4Dノックアウトマウスの好中球では、NET形成の抑制が見られませんでした。同研究グループは、さらに血管内皮細胞上のPlexin-B2という分子がSEMA4Dと結合してNET形成を抑制していることを発見し、Plexin-B2の作用下では、NET形成に必須とされる好中球の活性酸素(ROS)が、細胞内タンパク質であるRac1の非活性化によりほぼ完全に産生されなくなることを明らかにしました (図2) 。
これらの結果から、血清の遊離型SEMA4D濃度はANCA関連血管炎の病勢を反映するマーカーとして有用であり、また、好中球表面の膜型SEMA4Dは、好中球の活性化を制御する新たな治療ターゲットとなりうる可能性が示唆されました。
図2 ヒト好中球での活性酸素の産生に対するPlexinB2の影響
PlexinB2タンパク質を好中球に作用させると、好中球からの活性酸素の産生がほぼ完全に抑制される。
本研究成果が社会に与える影響(本研究成果の意義)
同研究グループは、セマフォリンが好中球の免疫チェックポイント分子として働き、好中球の活性化を制御していることを発見しました。好中球が関わる免疫難病であるANCA関連血管炎の病態に関わっていることが明らかになったセマフォリンは、その病態を反映するマーカーや、あるいは新しい治療ターゲットとして、今後さらに注目されます。
研究の進展によって、セマフォリンを介した「好中球の免疫チェックポイント加療」は、血管炎治療への応用が期待されます。
特記事項
本研究成果は、2017年4月18日(火)午前0時(日本時間)に欧州リウマチ学会誌「Annals of the Rheumatic Diseases」(オンライン)に掲載されました。
【タイトル】“Semaphorin 4D inhibits neutrophil activation and is involved in the pathogenesis of neutrophil-mediated autoimmune vasculitis.”
【著者名】Masayuki Nishide 1,2,3 , Satoshi Nojima 2,3,4 * , Daisuke Ito 2,3,5 , Hyota Takamatsu 1,2,3 , Shohei Koyama 1,2,3 , Sujin Kang 2,3,6 , Tetsuya Kimura 1,2,3 , Keiko Morimoto 1,2,3 , Takashi Hosokawa 1,2,3 , Yoshitomo Hayama 1,2,3 , Yuhei Kinehara 1,2,3 , Yasuhiro Kato 1,2,3 , Takeshi Nakatani 1,2,3 , Yoshimitsu Nakanishi 1,2,3 , Takeshi Tsuda 2,3,7 , Jeong Hoon Park 1 , Toru Hirano 1 , Yoshihito Shima 1 , Masashi Narazaki 1,2 , Eiichi Morii 4 , and Atsushi Kumanogoh 1,2,3 * ( * 責任著者)
1 大阪大学 大学院医学系研究科 呼吸器・免疫内科学
2 大阪大学 免疫学フロンティア研究センター 感染病態学
3 AMED-CREST
4 大阪大学 大学院医学系研究科 病態病理学
5 大阪大学 大学院医学系研究科 腎臓内科学
6 大阪大学 大学院医学系研究科 抗体医薬臨床応用学
7 大阪大学 大学院医学系研究科 耳鼻咽喉科・頭頸部外科学
本研究課題は、国立研究開発法人日本医療研究開発機構(AMED)、革新的先端研究開発支援事業(AMEDCREST)の研究開発領域「炎症の慢性化機構の解明と制御に向けた基盤技術の創出」(研究開発総括:宮坂昌之)における研究開発課題「慢性炎症におけるガイダンス因子の病的意義の解明とその制御」(研究開発代表者:熊ノ郷淳)の一環として行われました。なお、AMED-CREST研究開発領域は、平成27年4月の日本医療研究開発機構の発足に伴い、国立研究開発法人科学技術振興機構(JST)より移管されたものです。
研究者のコメント(西出助教)
免疫・アレルギー内科の臨床医として血管炎の患者様を診療する中で感じていた課題や問題点をスタート地点として、その病態解明の一助となる研究を行えたことを大変意義深く感じています。
今回の研究成果をさらに前進させることで、血管炎の新しい治療法の発展につなげたいと思っています。
参考URL
医学系研究科 呼吸器・免疫アレルギー内科感染病態グループ
http://www.med.osaka-u.ac.jp/pub/imed3/immunopathology/index.html
